Perbedaan antara reaksi spontan dan nonspontan
Itu perbedaan utama Antara reaksi spontan dan nonspontan adalah bahwa Reaksi spontan memiliki energi bebas Gibbs negatif sedangkan reaksi non-spontan memiliki energi bebas Gibbs yang positif.
Reaksi dapat berupa reaksi kimia atau reaksi biologis. Kita dapat membagi reaksi ini menjadi dua kategori sebagai reaksi spontan dan reaksi non-spontan. Reaksi spontan terjadi tanpa pengaruh eksternal. Tetapi reaksi non-spontan tidak dapat berkembang tanpa pengaruh eksternal. Mari kita bahas lebih detail tentang reaksi ini dan tabulasi perbedaan antara reaksi spontan dan nonspontan.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa reaksi spontan
3. Apa reaksi nonspontan
4. Perbandingan berdampingan - reaksi spontan vs nonspontan dalam bentuk tabel
5. Ringkasan
Apa reaksi spontan?
Reaksi spontan adalah reaksi kimia atau biologis yang terjadi tanpa pengaruh faktor eksternal apa pun. Selain itu, reaksi ini mendukung peningkatan entropi sambil mengurangi entalpi sistem termodinamika. Karena reaksi ini tidak membutuhkan faktor eksternal, mereka terjadi secara alami. Oleh karena itu reaksi ini mendukung pembentukan produk dalam kondisi di mana reaksi terjadi. Energi bebas Gibbs dari reaksi spontan adalah nilai negatif.
Sebagian besar reaksi spontan terjadi dengan cepat karena mendukung pembentukan produk daripada menjaga reaktan seperti itu. Mis: Pembakaran hidrogen. Tetapi beberapa reaksi terjadi dengan sangat lambat. Contoh: Konversi grafit menjadi berlian. Selain itu, dalam beberapa reaksi reversibel, satu arah reaksi disukai dari arah lain. Misalnya, dalam pembentukan karbon dioksida dan air dari asam karbonat, reaksi maju disukai; Pembentukan karbon dioksida dan air spontan.
H2BERSAMA3 ↔ co2 + H2HAI
Apa reaksi nonspontan?
Reaksi non-spontan adalah reaksi kimia atau biologis yang tidak dapat terjadi tanpa pengaruh faktor eksternal apa pun. Oleh karena itu, reaksi ini tidak mengalami pada kondisi alami.

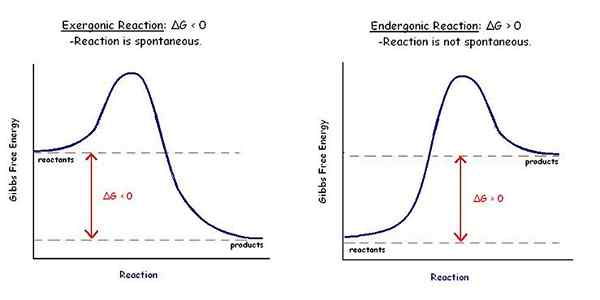
Gambar 01: Perbandingan reaksi spontan dan non-spontan
Dengan demikian, kita harus memberikan beberapa faktor eksternal untuk reaksi ini terhadap kemajuan. Contoh: Kami dapat memberikan panas, memberikan tekanan, menambahkan katalis, dll. Selain itu, energi bebas Gibbs positif untuk reaksi ini.
Hampir semua reaksi nonspontan adalah endotermik; Mereka melepaskan energi ke luar. Reaksi ini menyertai penurunan entropi. Contoh: Pembentukan nitrogen monoksida (tidak ada gas) dari reaksi antara oksigen dan nitrogen di atmosfer kita adalah nonspontan pada suhu normal dan kondisi tekanan. Namun, reaksi ini terjadi pada suhu yang sangat tinggi.
Apa perbedaan antara reaksi spontan dan nonspontan?
Reaksi spontan adalah reaksi kimia atau biologis yang terjadi tanpa pengaruh faktor eksternal apa pun. Mereka lebih menyukai meningkatkan entropi sambil mengurangi entalpi sistem termodinamika. Selain itu, energi bebas Gibbs dari reaksi spontan adalah nilai negatif. Sedangkan, reaksi non-spontan adalah reaksi kimia atau biologis yang tidak dapat terjadi tanpa pengaruh faktor eksternal apa pun. Mereka tidak menyukai peningkatan entropi atau mengurangi entalpi pada kondisi normal. Selain itu, energi bebas Gibbs dari reaksi non-spontan adalah nilai positif.

Ringkasan -reaksi spontan vs nonspontan
Semua reaksi milik dua jenis reaksi seperti reaksi spontan dan reaksi non-spontan. Perbedaan antara reaksi spontan dan nonspontan adalah bahwa reaksi spontan memiliki energi bebas Gibbs negatif sedangkan reaksi non-spontan memiliki energi bebas Gibbs yang positif.
Referensi:
1. Libretexts. “11.5: Reaksi spontan dan energi bebas.”Kimia Libretexts, Libretexts, 13 Juli 2018. Tersedia disini
2. Sains, CK12. “Reaksi spontan dan nonspontan.”CK-12 Foundation, CK-12 Foundation, 28 Mar. 2017. Tersedia disini
Gambar milik:
1.'Gibbs Free Energy'by Stephjc - Pekerjaan Sendiri, (Domain Publik) Melalui Commons Wikimedia


