Perbedaan antara aluminasi dan meta aluminasi

Itu perbedaan utama Antara aluminasi dan meta aluminasi adalah itu Aluminat adalah anion oksida, sedangkan meta aluminat adalah anion hidroksida.
Aluminasi dan meta aluminasi adalah dua jenis anion yang saling terkait tergantung pada struktur kimianya. Namun, atomisitas mereka berbeda satu sama lain. Ini karena anion aluminat hanya memiliki atom oksigen yang berhubungan dengan atom aluminium, sedangkan meta aluminat mengandung atom hidrogen dan oksigen dalam hubungan dengan atom aluminium.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu aluminasi
3. Apa itu meta aluminasi
4. Perbandingan berdampingan - aluminasi vs meta aluminasi dalam bentuk tabel
5. Ringkasan
Apa itu aluminasi?
Aluminat adalah oksiani aluminium yang memiliki formula kimia alo4-. Senyawa yang paling umum mengandung anion aluminat adalah natrium aluminasi. Selanjutnya, aluminasi natrium murni adalah senyawa anhidrat yang muncul sebagai padatan kristal putih. Sementara itu, aluminat natrium terhidrasi terjadi sebagai senyawa hidroksida. Dan, bentuk aluminasi natrium terhidrasi yang paling umum adalah tetrahydroxyaluminate dari natrium.

Gambar 01: Penampilan natrium aluminasi
Moreer, anion aluminat adalah anion politisomik yang mengandung atom aluminium di tengah anion dan empat atom oksigen yang melekat pada atom aluminium sentral ini melalui ikatan kovalen ini. Tuduhan anion adalah -1. Massa molar anion adalah 91 g/mol.
Apa itu meta aluminasi?
Meta aluminat adalah bentuk terhidrasi dari anion aluminasi. Oleh karena itu, aluminat adalah oksiani sementara meta aluminat adalah anion hidroksida. Formula kimia anion ini adalah al (OH)4-. Juga, massa molar dari anion ini adalah 95 g/mol. Selain itu, satu meta aluminasi anion terbentuk ketika dua molekul air menjadi terkait dengan anion aluminasi.
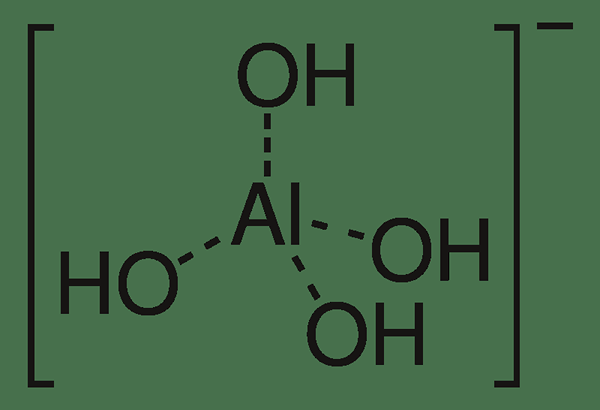
Gambar 02: Struktur kimia anion meta aluminasi
Biasanya, alo2- ion disebut "meta" sedangkan alo33- ion disebut senyawa "ortho". Konformasi orto, paragraf dan meta ion aluminasi berbeda satu sama lain tergantung pada derajat kondensasi. Istilah "meta" mengacu pada bentuk aluminasi natrium yang paling tidak terhidrasi.
Apa perbedaan antara aluminasi dan meta aluminasi?
Aluminasi dan meta aluminasi adalah dua bentuk anionik terkait. Perbedaan utama antara aluminat dan aluminasi logam adalah bahwa aluminat adalah anion oksida, sedangkan meta aluminat adalah anion hidroksida. Juga, formula kimia aluminat adalah alo4- Sedangkan formula kimia meta aluminasi adalah al (OH)4-.
Selain itu, anion aluminat adalah oksiani sedangkan meta aluminat adalah oksilasi terhidrasi. Jadi, ini adalah perbedaan lain antara aluminasi dan aluminasi logam. Selanjutnya, massa molar aluminat adalah 91 g/mol, sedangkan massa molar meta aluminasi adalah 95 g/mol.
Bergantung pada komposisi, kita dapat menyebut aluminasi oksiani (mengandung atom aluminium dan oksigen) sementara meta aluminat dapat dikategorikan sebagai hidroksiani (mengandung aluminium dalam kombinasi dengan atom oksigen dan hidrogen). Sodium Aluminate adalah contoh terkenal dari senyawa yang mengandung anion aluminat sedangkan natrium meta aluminat adalah contoh senyawa yang mengandung anion meta aluminat.
Infografis di bawah ini merangkum perbedaan antara aluminat dan aluminasi logam.
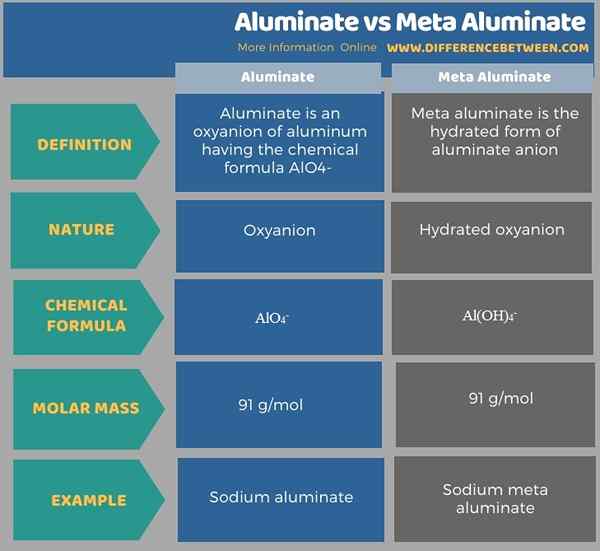
Ringkasan -Aluminat vs Meta Aluminate
Aluminasi dan meta aluminasi adalah dua bentuk anionik terkait. Perbedaan utama antara aluminat dan aluminasi logam adalah bahwa aluminat adalah anion oksida, sedangkan meta aluminat adalah anion hidroksida. Oleh karena itu, aluminat disebut oksyanion dan meta aluminat disebut hidroksionion. Formula kimia anion aluminasi adalah alo4- Sedangkan formula kimia anion meta aluminasi adalah al (OH)4-.
Referensi:
1. “Aluminasi."Wikipedia, Wikimedia Foundation, 4 September. 2019, tersedia di sini.
2. “Aluminasi."Informasi Nasional untuk Informasi Bioteknologi. Database senyawa pubchem, u.S. Perpustakaan Kedokteran Nasional, tersedia di sini.
3. “Sodium Aluminate."Informasi Nasional untuk Informasi Bioteknologi. Database senyawa pubchem, u.S. Perpustakaan Kedokteran Nasional, tersedia di sini.
Gambar milik:
1. "Naalo2" oleh Leiem - karya sendiri (CC BY -SA 4.0) Via Commons Wikimedia
2. “Ion Tetrahydroxoaluminate” oleh Leyo - karya sendiri (domain publik) melalui Commons Wikimedia


