Perbedaan antara amfolit dan amfoterik
Itu perbedaan utama antara amfolit dan amfoterik adalah itu Istilah amfoter berarti kemampuan molekul untuk bertindak sebagai asam atau basa sedangkan ampholyte adalah molekul, yang bersifat amfoterik.
Kami menemukan molekul, yang kami kategorikan sebagai dasar, asam atau netral. Solusi dasar menunjukkan nilai pH lebih tinggi dari 7 dan larutan asam menunjukkan nilai pH, yang lebih rendah dari 7. Solusi yang memiliki nilai pH 7 adalah solusi netral. Ada beberapa molekul, yang berbeda dari kategorisasi normal ini. Ampholytes adalah salah satu molekul seperti itu. Mereka memiliki sifat kimia asam dan basa.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu amfolit
3. Apa itu amfoter
4. Perbandingan Berdampingan - Ampholyte vs Amfoterik Dalam Bentuk Tabel
5. Ringkasan
Apa itu amfolit?
Ampholyte adalah molekul yang memiliki gugus basa dan asam. Contoh umum terbaik dan paling luas untuk amfolit adalah asam amino. Kita tahu bahwa semua asam amino memiliki -cooh, -nh2 kelompok dan A -H terikat pada karbon. Kelompok karboksilat (-COOH) bertindak sebagai gugus asam dalam asam amino, dan amina (-NH2) kelompok bertindak sebagai kelompok dasar. Selain ini, ada kelompok -r di setiap asam amino. Kelompok R berbeda dari satu asam amino ke yang lain. Asam amino paling sederhana dengan kelompok R adalah h adalah glisin.
Namun, kelompok R dalam beberapa asam amino mengandung gugus karboksilat tambahan atau gugus amina. Misalnya, lisin, histidin, dan arginin adalah asam amino yang memiliki gugus amina tambahan. Dan asam aspartat, asam glutamat mengandung gugus karboksilat tambahan. Lebih lanjut, beberapa di antaranya mengandung kelompok -OH, yang dapat bertindak sebagai basa atau asam dalam keadaan tertentu (tirosin). Karena kedua kelompok asam dan basa, mereka umumnya memiliki setidaknya dua nilai PKA (jika ada lebih dari satu -NH2 grup atau -cooh grup, maka akan ada lebih dari dua nilai pKa). Oleh karena itu, kurva titrasi amfolit kompleks dari kurva titrasi normal.
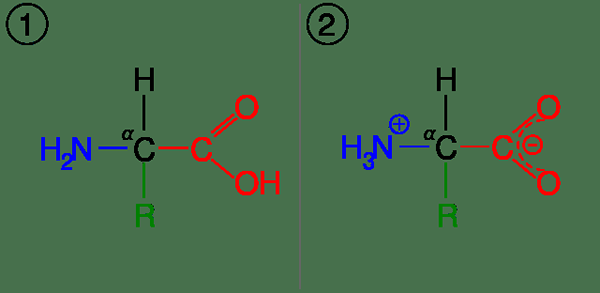
Gambar 01: Asam amino dalam bentuk (1) yang tidak diionisasi dan (2) zwitterionic
Kejadian
Dalam berbagai sistem, ampholyte terjadi dalam berbagai bentuk yang bermuatan tergantung pada pH. Misalnya, dalam larutan asam, gugus amina dari asam amino akan terjadi pada yang diisi secara positif dari, dan gugus karboksil akan ada sebagai -cooh. Dalam solusi pH dasar, kelompok karboksil akan ada dalam bentuk anion karboksilat (-coo-), dan kelompok amino akan hadir sebagai -nh2.
Dalam tubuh manusia, pH mendekati 7.4. Oleh karena itu, dalam pH ini, asam amino hadir sebagai zwitterions. Di sini, kelompok amino mengalami protonasi dan memiliki muatan positif, sedangkan kelompok karboksil memiliki muatan negatif. Oleh karena itu, muatan bersih molekul adalah nol. Pada titik ini, molekul mencapai titik isoelektriknya.
Apa itu amfoter?
Istilah amfoter berarti kemampuan molekul, ion atau senyawa kompleks lainnya untuk bertindak sebagai basa dan asam. Ada beberapa molekul, yang memiliki kedua sifat ini dalam keadaan tertentu. Selain itu, ada beberapa oksida logam dan hidroksida, yang amfoter.
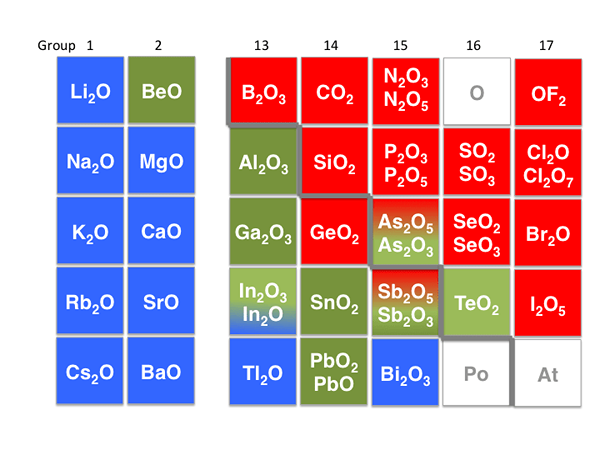
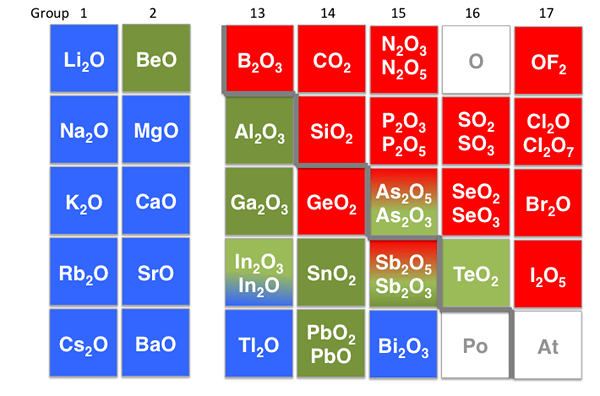
Gambar 02: Senyawa Amfoterik
Misalnya, seng oksida (ZnO), aluminium oksida (AL2HAI3), aluminium hidroksida (Al (OH)3), dan oksida timbal bersifat amfoter. Dalam media asam, mereka bertindak sebagai basa, dan dalam media basa, mereka bertindak sebagai asam. Molekul amfoterik yang paling umum dan terkenal adalah asam amino, yang dapat kita amati di semua sistem biologis.
Apa perbedaan antara amfolit dan amfoterik?
Amfolit adalah molekul yang memiliki gugus basa dan asam dan istilah amfoter berarti kemampuan molekul, ion atau senyawa kompleks lainnya untuk bertindak sebagai basa dan asam. Perbedaan utama antara ampholyte dan amfoterik adalah bahwa istilah amfoter berarti kemampuan molekul untuk bertindak sebagai asam atau basa sedangkan ampholyte adalah molekul yang amfoter.
Selain itu, seng oksida, aluminium oksida, aluminium hidroksida, dan oksida timbal bersifat amfoter, yang memiliki perilaku berbeda dalam larutan asam dan basa. Namun, ini bukan ampholytes karena mereka tidak memiliki kelompok asam dan basa dalam molekul tersebut. Ngomong -ngomong, asam amino adalah ampholyte, yang memiliki kelompok asam dan basa yang ada dalam satu molekul. Karenanya, itu juga amfoterik.

Ringkasan -Amfolit vs Amfoterik
Amfoter berarti kemampuan molekul untuk bertindak sebagai asam atau basa. Amfolit adalah molekul yang amfoter. Oleh karena itu, amfolit memiliki kelompok asam dan basa. Oleh karena itu, perbedaan utama antara amfolit dan amfoter adalah bahwa istilah amfoter berarti kemampuan molekul untuk bertindak sebagai asam atau basa sedangkan amfolit adalah molekul yang amfoter.
Referensi:
1. Helmenstine, Anne Marie, PH.D. “Definisi dan contoh amfoterik."Thoughtco, Jun. 22, 2018. Tersedia disini
2. Libretexts. “Amphoteric."Kimia Libretexts, National Science Foundation, 20 Feb. 2017. Tersedia disini
Gambar milik:
1."Amino Acid Zwitterions" oleh TimvickersVector (CC dengan 3.0) Via Commons Wikimedia
2."Amphoteric" oleh Tem5psu - karya sendiri, (CC BY -SA 3.0) Via Commons Wikimedia


