Perbedaan antara aksi buffer dan kapasitas buffer

Itu perbedaan utama Antara aksi buffer dan kapasitas buffer adalah itu Tindakan buffer mengacu pada kemampuan larutan untuk menahan perubahan pH sedangkan kapasitas buffer mengacu pada mol asam atau basa yang diperlukan untuk mengubah pH larutan suatu.
Larutan buffer adalah larutan berair yang terdiri dari asam lemah dan basa konjugatnya. Tindakan buffer istilah dan kapasitas buffer menggambarkan sifat solusi yang dapat bertindak sebagai buffer.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu tindakan buffer
3. Apa itu kapasitas penyangga
4. Perbandingan berdampingan - aksi buffer vs kapasitas buffer dalam bentuk tabel
5. Ringkasan
Apa itu tindakan buffer?
Tindakan buffer adalah kemampuan solusi untuk menahan perubahan pH. Penambahan sejumlah asam atau basa ke larutan buffer dapat mengubah pH larutan buffer. Tindakan penyangga mengacu pada kemampuan untuk tetap tidak berubah setelah penambahan sejumlah kecil asam atau basa. Solusi yang dapat menunjukkan kemampuan ini dikenal sebagai solusi buffer atau hanya sebagai buffer.
Selain itu, fenomena ini sangat penting; Jika kita mengambil air sebagai contoh, kemampuannya untuk tetap tidak berubah setelah penambahan asam atau basa sampai batas tertentu membantu menjaga nilainya dalam fungsi sistem biologis.
Apa itu kapasitas penyangga?
Kapasitas penyangga mengacu pada mol asam atau basa yang diperlukan untuk mengubah pH larutan. Ini adalah pengukuran kuantitatif mengenai resistensi terhadap perubahan pH pada penambahan atau pengurangan ion hidroksida atau ion hidrogen. Kami dapat menghitung nilai ini dengan membagi jumlah asam atau basa yang diperlukan untuk mengubah pH buffer dengan perubahan pH dan volume larutan buffer.
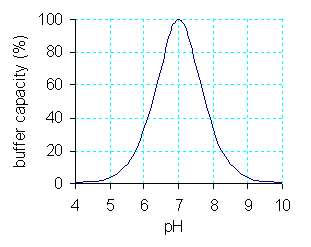
Gambar 01: Grafik sampel yang menunjukkan kapasitas buffer suatu sistem
Larutan memperoleh kemampuan ini karena konsumsi asam atau basa yang ditambahkan ke larutan buffer oleh agen buffering yang ada dalam larutan itu. Larutan buffer ini memiliki reaksi keseimbangan antara asam dan basa konjugat atau sebaliknya. Oleh karena itu, P-H tidak akan berubah secara drastis pada penambahan asam atau basa lebih lanjut sampai batas tertentu selama zat penyangga tidak sepenuhnya bereaksi (tetap dalam keseimbangan). Secara umum, kita dapat menghitung kapasitas buffering menggunakan metode titrimetri.
Apa perbedaan antara aksi buffer dan kapasitas buffer?
Larutan buffer adalah larutan berair yang terdiri dari asam lemah dan basa konjugatnya. Tindakan buffer istilah dan kapasitas buffer adalah istilah yang diterapkan pada solusi yang dapat bertindak sebagai buffer. Perbedaan utama antara aksi buffer dan kapasitas buffer adalah bahwa aksi buffer mengacu pada kemampuan solusi untuk menahan perubahan pH sedangkan kapasitas buffer mengacu pada mol asam atau basa yang diperlukan untuk mengubah pH larutan suatu larutan.
Di bawah infografis merangkum perbedaan antara aksi buffer dan kapasitas buffer.
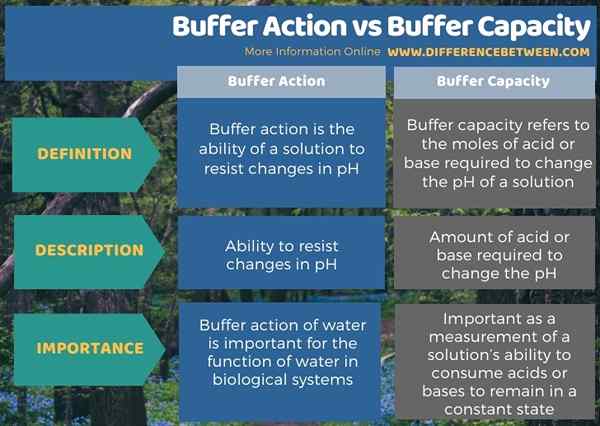
Ringkasan -Kapasitas aksi buffer vs buffer
Larutan buffer adalah larutan berair yang terdiri dari asam lemah dan basa konjugatnya. Istilah aksi buffer dan kapasitas buffer diterapkan terutama mengenai solusi yang dapat bertindak sebagai buffer. Perbedaan utama antara aksi buffer dan kapasitas buffer adalah bahwa aksi buffer mengacu pada kemampuan solusi untuk menahan perubahan pH sedangkan kapasitas buffer mengacu pada mol asam atau basa yang diperlukan untuk mengubah pH larutan suatu larutan.
Referensi:
1. Bosch, e., dan m. Rosés. “Kromatografi | Buffer untuk kromatografi dan elektroforesis.”Ensiklopedia Ilmu Pemisahan, 2007, PP. 1-12., doi: 10.1016/B978-012226770-3/10696-x.
2. Subirat, x., et al. “Buffer untuk kromatografi cair fase terbalik ☆.”Modul Referensi dalam Kimia, Ilmu Molekuler dan Teknik Kimia, 2015, doi: 10.1016/B978-0-12-409547-2.11547-1.
3. “Solusi buffer.”Wikipedia, Wikimedia Foundation, 12 Jan. 2020, tersedia di sini.
Gambar milik:
1. "3533039" (lisensi pixabay) melalui pixabay
2. "Kapasitas buffer" oleh Petersan (bicara). - I Petersan (Talk) menciptakan karya ini sepenuhnya oleh diri saya sendiri (domain publik) melalui Commons Wikimedia