Perbedaan antara Mendeleev dan Tabel Periodik Modern

Itu perbedaan utama Antara Mendeleev dan Tabel Periodik Modern adalah itu Dasar tabel periodik modern terutama adalah konfigurasi elektronik elemen, yang kami sebut sebagai nomor atom sedangkan, dalam tabel periodik Mendeleev, itu adalah massa atom dari elemen.
Mari kita lihat di sini apa itu tabel periodik Mendeleev dan apa itu tabel periodik modern, dan kemudian membandingkan keduanya untuk memahami perbedaan antara Mendeleev dan tabel periodik modern. Mendeleev adalah pelopor tabel periodik modern, setelah sejumlah perubahan pada versi lama dari tabel periodik. Kedua upaya ini sama pentingnya bagi komunitas ilmiah; Karena tanpa penemuan hubungan berkala dalam elemen, perkembangan modern dalam sains tidak akan mencapai era pembangunan seperti saat ini.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu tabel periodik Mendeleev
3. Apa itu Tabel Periodik Modern
4. Perbandingan Berdampingan - Mendeleev vs Tabel Periodik Modern dalam Bentuk Tabel
5. Ringkasan
Apa itu tabel periodik Mendeleev?
Pada tahun 1869, seorang ahli kimia Rusia Dmitri Mendeleev dan seorang ahli kimia Jerman Lothar Meyer mengusulkan tabulasi elemen periodik berdasarkan kekambuhan berkala sifat -sifatnya. Pada tahun 1864, sebelum Mendeleev, seorang ahli kimia Inggris John Newlands mengatur unsur -unsur dalam urutan massa atom di mana setiap delapan elemen memiliki sifat yang sama. Dia menyebut hubungan aneh sebagai "hukum oktaf". Namun, kami tidak dapat membuat hukumnya untuk unsur -unsur di luar kalsium. Oleh karena itu, komunitas ilmiah tidak menerimanya.

Gambar 01: Tabel Periodik Mendeleev
Dibandingkan dengan klasifikasi Newland, sistem klasifikasi Mendeleev memiliki peningkatan besar karena dua alasan. Faktor pertama adalah, itu mengelompokkan elemen bersama lebih akurat sesuai dengan sifatnya. Kedua, itu membuat prediksi kemungkinan sifat beberapa elemen yang belum ditemukan. Sebagai contoh, Mendeleev mengusulkan keberadaan elemen yang tidak diketahui yang disebut Eka-aluminium dan memprediksi sejumlah sifatnya. (Eka-Meaning in Sanskerta adalah 'pertama'. Dengan demikian Eka-aluminium adalah elemen pertama dalam kelompok aluminium). Ketika para ilmuwan menemukan gallium setelah empat tahun, sifat-sifatnya sangat cocok dengan sifat prediksi Eka-aluminium.
Dengan demikian, untuk menyebutkan ini adalah sebagai berikut;

Di tabel periodik Mendeleev, 66 elemen ada. Pada tahun 1900, 30 elemen lainnya ditambahkan ke dalam daftar, mengisi beberapa ruang kosong di tabel.
Apa itu Tabel Periodik Modern?
Tabel Periodik Modern mempertimbangkan konfigurasi elektron keadaan tanah terluar dari elemen. Menurut jenis subshell yang diisi dengan elektron, kita dapat membagi elemen menjadi kategori; Elemen representatif, gas mulia, elemen transisi (atau logam transisi) dan actinides. Elemen yang representatif adalah (kami menyebutnya elemen grup utama) kelompok -kelompok di IA hingga 7a, yang secara tidak sepenuhnya diisi oleh semua elemen S atau P subsksel dari nomor kuantum prinsip tertinggi. Dengan pengecualian helium (dia) semua elemen 8a telah mengisi p-subshell.
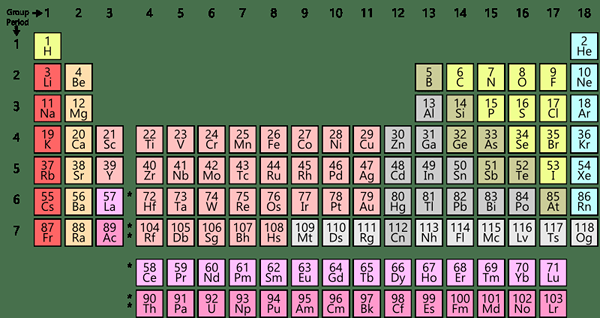
Gambar 02: Tabel Periodik Modern
Logam transisi adalah elemen 1b dan 3b hingga 8b, di mana molekul tidak sepenuhnya mengisi dubshell D. Lanthanides dan aktinida kadang-kadang disebut elemen f-block karena elemen-elemen tersebut tidak memiliki f-orbital yang tidak lengkap.
Apa perbedaan antara Mendeleev dan Tabel Periodik Modern?
Tabel periodik Mendeleev adalah dasar untuk tabel periodik modern yang kita gunakan saat ini. Ini memiliki 65 elemen yang diketahui, tetapi dengan elemen yang baru ditemukan, ada 103 elemen di tabel periodik modern. Perbedaan utama antara Mendeleev dan tabel periodik modern adalah bahwa dasar dari tabel periodik modern terutama adalah konfigurasi elektronik elemen, yang kita sebut sebagai nomor atom sedangkan tabel periodik Mendeleev mempertimbangkan massa atom dari elemen -elemen tersebut.
Infografis di bawah ini tabulasi perbedaan antara Mendeleev dan tabel periodik modern secara rinci.

Ringkasan -Mendeleev vs Tabel Periodik Modern
Elemen dengan sifat kimia dan fisik yang serupa berulang pada interval yang pasti dalam tabel periodik modern, dan memiliki sekitar 103 elemen. Ketika Mendeleev mengklasifikasikannya, hanya ada 66 elemen di tabel periodik. Namun, Mendeleev meninggalkan tempat kosong di meja berkala untuk elemen yang belum ditemukan. Dia juga mengasumsikan variasi periodik sifat dalam elemen. Perbedaan utama antara Mendeleev dan tabel periodik modern adalah bahwa dasar dari tabel periodik modern terutama adalah konfigurasi elektronik elemen, yang kita sebut sebagai nomor atom sedangkan tabel periodik Mendeleev mempertimbangkan massa atom dari elemen -elemen tersebut.
Referensi:
1. Libretexts. “3.1: Tabel periodik Mendeleev."Kimia Libretexts, Libretexts, 14 Okt. 2016. Tersedia disini
2. "Tabel periodik."Wikipedia, Wikimedia Foundation, 7 Okt. 2018. Tersedia disini
Gambar milik:
1."Tabel Berkala oleh Mendeleev, 1871" oleh Niknaks - karya sendiri, (domain publik) melalui Commons Wikimedia
2.”Sederhana Tabel Periodik -en” oleh Offnfopt - karya sendiri, (domain publik) via Commons Wikimedia


