Perbedaan antara sublimasi dan deposisi

Itu perbedaan utama antara sublimasi dan deposisi adalah itu Sublimasi adalah perubahan zat padat menjadi zat gas tanpa melalui fase cair sedangkan pengendapan adalah perubahan zat dari fase gas ke fase padat tanpa melewati keadaan cair.
Transisi fase mengacu pada mengubah fase suatu zat. Faktor eksternal seperti perubahan suhu dan tekanan mempengaruhi proses ini. Misalnya, cairan memadat ketika kita mengurangi suhu ke titik beku, dan mungkin masuk ke fase gas saat suhu berada pada titik didihnya. Transisi fase umumnya memiliki pesanan; Padatan masuk ke fase cair dan kemudian ke fase gas; atau jika itu adalah gas, ia harus melalui fase cair terlebih dahulu dan kemudian ke fase padat. Sublimasi dan deposisi adalah transisi fase, tetapi mereka sedikit berbeda dari transisi normal karena mereka tidak mengikuti pesanan ini.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu sublimasi
3. Apa itu deposisi
4. Perbandingan berdampingan - Sublimasi vs Deposisi dalam bentuk tabel
5. Ringkasan
Apa itu sublimasi?
Sublimasi adalah proses mengubah zat padat menjadi zat gas tanpa melalui fase cair. Dengan kata -kata sederhana, zat padat secara langsung menguap dan menjadi gas tanpa menjadi cairan terlebih dahulu. Namun, proses ini membutuhkan energi ekstra. Oleh karena itu, ini adalah proses endotermik. Dengan menghitung entalpi sublimasi, kita dapat menghitung energi yang dibutuhkan untuk proses ini: dengan menambahkan entalpi fusi dan entalpi penguapan bersama -sama.
Sublimasi terjadi pada suhu dan tekanan di bawah titik tiga zat. Misalnya, karbon dioksida padat sublim pada suhu yang sangat rendah (-78.5 ° C) dan pada tekanan atmosfer. Titik tiga karbon dioksida adalah 5.2 ATM dan -56.4 ° C, dan di atas titik ini, kita juga dapat memperoleh karbon dioksida cair. Es dan yodium juga dapat mengalami sublimasi.

Gambar 1: Sublimasi es kering
Dalam sublimasi, sifat kimia senyawa tetap tidak berubah, tetapi sifat fisik dapat berubah. Sublimasi berguna untuk berbagai tujuan. Misalnya, ini digunakan untuk memurnikan senyawa kimia.
Apa itu deposisi?
Deposisi adalah proses yang berlawanan dari sublimasi. Itu juga dikenal sebagai de-penerbitan. Di sini, suatu zat dalam fase gas berubah menjadi fase padat tanpa melewati keadaan cair menengah.

Gambar 2: Formasi Frost
Berbeda dengan proses sebelumnya, proses ini melepaskan energi; Oleh karena itu, ini adalah proses eksotermik. Selanjutnya, ini terjadi saat membentuk es atau embun beku. Dalam proses ini, uap air langsung masuk ke fase padat (membentuk es atau es). Ketika ini terjadi, mereka menghilangkan energi termal ke lingkungan eksternal.
Apa perbedaan antara sublimasi dan deposisi?
Sublimasi adalah kebalikan dari deposisi. Perbedaan utama antara sublimasi dan deposisi adalah bahwa sublimasi adalah perubahan zat padat menjadi zat gas tanpa melalui fase cair sedangkan pengendapan adalah perubahan zat dari fase gas ke fase padat tanpa melewati keadaan cair.
Selain itu, perbedaan yang signifikan antara sublimasi dan deposisi adalah bahwa sublimasi adalah endotermik sedangkan pengendapan adalah eksotermik.
Infografis di bawah ini memberikan rincian lebih lanjut tentang perbedaan antara sublimasi dan deposisi.
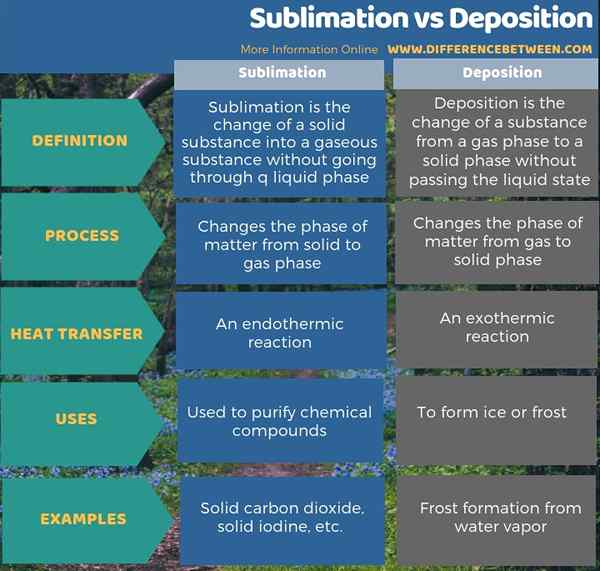
Ringkasan -Sublimasi vs Deposisi
Sublimasi adalah kebalikan dari deposisi. Namun, kedua proses ini tidak melibatkan fase cair. Perbedaan utama antara sublimasi dan deposisi adalah bahwa sublimasi mengubah zat padat menjadi zat gas tanpa melalui fase cair sedangkan deposisi mengubah zat dari fase gas ke fase padat tanpa melewati keadaan cair.
Referensi:
1. “Deposisi (transisi fase).”Wikipedia, Wikimedia Foundation, 27 Mar. 2019, tersedia di sini.
2. Helmenstine, Anne Marie, PH.D. “Definisi Sublimasi (Transisi Fase dalam Kimia)."Thoughtco, Jan. 13, 2019, tersedia di sini.
Gambar milik:
1. "Dryices Publimation" oleh Sarathtly - Foto yang diambil oleh saya (domain publik) melalui Commons Wikimedia
2. "Frost Patterns 4" oleh Schnobby - karya sendiri (CC BY -SA 3.0) Via Commons Wikimedia


