Perbedaan antara titanium oksida dan titanium dioksida

Itu perbedaan utama antara titanium oksida dan titanium dioksida adalah bahwa Titanium oksida mengandung satu anion oksigen per satu kation titanium sedangkan titanium dioksida mengandung dua anion oksigen per satu kation titanium.
Titanium adalah elemen kimia yang memiliki simbol kimia dan nomor atom 22. Ini adalah logam berkilau yang berada di bawah kategori logam transisi. Sebagai karakteristik utama, ia memiliki kekuatan tinggi dibandingkan dengan kepadatan rendah. Elemen ini dapat memiliki beberapa keadaan oksidasi, tetapi keadaan oksidasi yang paling stabil adalah +4. Ada beberapa oksida yang dapat terbentuk seperti titanium (II) oksida, titanium (III) oksida dan titanium dioksida.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu titanium oksida
3. Apa itu titanium dioksida
4. Perbandingan berdampingan - titanium oksida vs titanium dioksida dalam bentuk tabel
5. Ringkasan
Apa itu titanium oksida?
Titanium oksida adalah senyawa anorganik yang memiliki formula kimia. Kami menamai senyawa ini sebagai titanium monoksida atau titanium (II) oksida. Massa molar senyawa ini adalah 63.87 g/mol. Itu muncul sebagai kristal perunggu. Selain itu, ia memiliki titik leleh yang tinggi yaitu 1.750 ° C, dan kepadatannya adalah 4.95 g/cm3. Saat mempertimbangkan struktur kristal senyawa ini, ia memiliki struktur kubik.
Kita dapat menyiapkan senyawa ini dari titanium dioksida atau dari logam titanium juga. Tetapi kita harus melakukan reaksi ini pada suhu 1500 ° C. Selain itu, larutan asam dari senyawa ini stabil untuk waktu yang singkat, tetapi nanti akan terurai untuk memberikan hidrogen. Reaksi ini adalah sebagai berikut:
2Ti2+(aq) + 2h+(aq) → 2ti3+(aq) + h2(G)
Apa itu titanium dioksida?
Titanium dioksida adalah senyawa anorganik yang memiliki formula kimia tio2. Ini adalah oksida titanium yang terjadi secara alami. Selain itu, kami menyebutkan senyawa ini sebagai titanium (iv) oksida. Massa molar senyawa ini adalah 79.87 g/mol. Itu muncul sebagai padatan putih. Ini memiliki titik leleh yang tinggi yaitu 1.843 ° C. Kepadatan senyawa ini bervariasi sesuai dengan jenis struktur kristal di mana ia ada. Misalnya, kepadatan struktur kristal rutil adalah 4.23 g/cm3 sedangkan kepadatan struktur kristal anatase adalah 3.78 g/cm3.

Gambar 01: Titanium dioksida putih padat
Kami dapat menghasilkan senyawa ini dari pemrosesan pasir bantalan titanium seperti pasir mineral ilmenit. Saat mempertimbangkan aplikasi utama senyawa ini, itu termasuk produksi pigmen titanium dioksida yang penting untuk produksi cat, kertas, plastik, dll.
Apa perbedaan antara titanium oksida dan titanium dioksida?
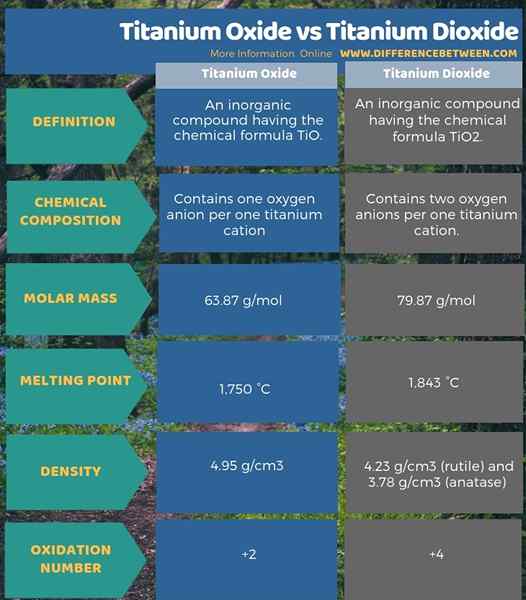
Titanium oksida adalah senyawa anorganik yang memiliki formula kimia sedangkan titanium dioksida adalah senyawa anorganik yang memiliki formula kimia tio2. Oleh karena itu, titanium oksida mengandung satu anion oksigen per satu kation titanium tetapi, titanium dioksida mengandung dua anion oksigen per satu kation titanium. Ini adalah perbedaan utama antara titanium oksida dan titanium dioksida. Juga, karena struktur ini, mereka memiliki massa molar yang berbeda dan titik leleh yang berbeda juga. Selain itu, jumlah oksidasi titanium di setiap senyawa berbeda satu sama lain; Jumlah oksidasi titanium dalam titanium oksida adalah +2 sedangkan jumlah oksidasi titanium dalam titanium dioksida adalah +4. Ini adalah perbedaan penting lainnya antara titanium oksida dan titanium dioksida.
Infografis di bawah ini tabulasi perbedaan antara titanium oksida dan titanium dioksida secara lebih rinci.
Ringkasan -Titanium oksida vs titanium dioksida
Titanium oksida dan titanium dioksida adalah oksida penting dari elemen kimia titanium. Perbedaan utama antara titanium oksida dan titanium dioksida adalah bahwa titanium oksida mengandung satu anion oksigen per satu kation titanium tetapi, titanium dioksida mengandung dua anion oksigen per satu kation titanium.
Referensi:
1. “Titanium (II) oksida.”Wikipedia, Wikimedia Foundation, 19 Agustus. 2018. Tersedia disini
2. "Titanium dioksida.”Wikipedia, Wikimedia Foundation, 26 Agustus. 2018. Tersedia disini
Gambar milik:
1.”Titanium (IV) Oxide” oleh Walkerma di Wikipedia Inggris. (Domain publik) via commons wikimedia


