Apa perbedaan antara amonia dan boron trifluoride
Itu Perbedaan utama antara amonia dan boron trifluoride adalah bahwa amonia adalah molekul polar, sedangkan boron trifluorida adalah molekul nonpolar.
Amonia dan boron trifluorida memiliki atomisitas yang sama dan konektivitas atom yang serupa, tetapi ada pasangan elektron tunggal pada atom nitrogen dalam molekul amonia sementara tidak ada elektron tunggal pada atom boron dalam boron trifluorida. Fakta ini menjadikan amonia molekul polar dan boron trifluorida molekul nonpolar.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu amonia
3. Apa itu boron trifluoride
4. Amonia vs boron trifluoride dalam bentuk tabel
5. Ringkasan
Apa itu amonia?
Amonia adalah senyawa anorganik yang memiliki formula kimia NH3. Ini adalah zat gas dan merupakan pnictogen hydride paling sederhana. Amonia terjadi sebagai gas tidak berwarna yang memiliki bau yang pedas dan menjengkelkan. Nama IUPAC amonia Azane. Massa molar amonia adalah 17.03 g/mol. Titik lelehnya adalah −77.73 ° C, dan titik didihnya adalah −33.34 ° C.
Saat mempertimbangkan terjadinya gas amonia, secara alami terjadi di lingkungan tetapi dalam jumlah jejak sebagai produk dari bahan hewan dan nabati nitrogen. Terkadang, kita juga dapat menemukan amonia di air hujan. Di dalam tubuh kita, ginjal mengeluarkan amonia untuk menetralkan asam berlebih.
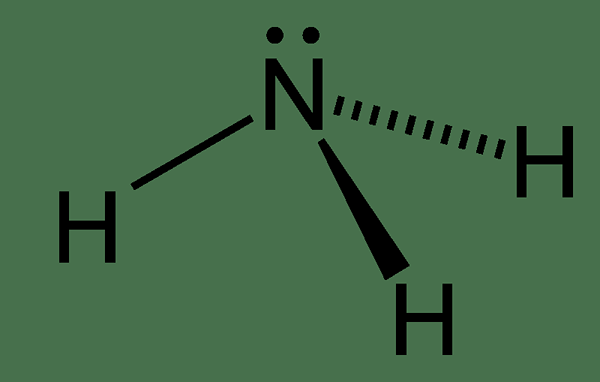
Gambar 01: amonia
Struktur kimia molekul amonia memiliki atom nitrogen yang terikat pada tiga atom hidrogen. Karena ada lima elektron dalam cangkang elektron terluar dari nitrogen, ada pasangan elektron tunggal pada atom nitrogen molekul amonia. Oleh karena itu, geometri molekul amonia adalah piramidal trigonal. Selain itu, kita dapat mencairkan senyawa ini dengan mudah. Ini karena mampu membentuk ikatan hidrogen antara molekul amonia karena ada ikatan N-H dan pasangan elektron sendirian juga.
Apa itu boron trifluoride?
Boron Trifluoride adalah senyawa anorganik yang memiliki formula kimia BF3. Itu adalah gas pedas yang tidak berwarna dan beracun. Itu bisa membentuk asap putih di udara lembab. Namun, ada dua bentuk utama boron trifluoride sebagai bentuk anhidrat dan bentuk dihidrat; Bentuk anhidrat adalah gas yang tidak berwarna, sedangkan bentuk dihidrat adalah cairan yang tidak berwarna. Saat mempertimbangkan kelarutannya dalam air, bentuk anhidrat cenderung mengalami dekomposisi eksotermik ketika ditambahkan ke air, sedangkan bentuk dihidrat sangat larut dalam air. Zat ini bersifat korosif, jadi kita perlu menggunakan stainless steel, monel, dan hastelloy untuk penyimpanan zat ini.

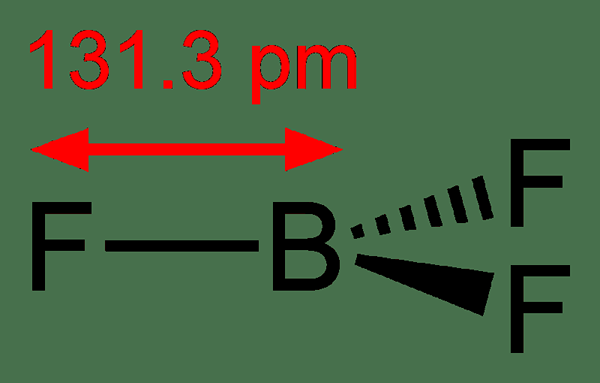
Gambar 02: Boron Trifluoride
Molekul boron trifluorida memiliki geometri planar trigonal. Itu tidak memiliki momen dipol karena simetri. Molekul ini adalah isoelektronik dengan anion karbonat. Secara umum, kami menyebut boron trifluorida spesies kimia yang kekurangan elektron. Ini memiliki reaktivitas eksotermik dengan pangkalan Lewis.
Dalam sintesis boron trifluorida, kita dapat menghasilkannya dari reaksi antara boron oksida dan hidrogen fluorida. Namun, dalam kebutuhan laboratorium, kami dapat menghasilkan boron trifluoride menggunakan boron trifluoride eterate (cairan yang tersedia secara komersial).
Apa perbedaan antara amonia dan boron trifluoride?
Amonia dan boron trifluorida adalah molekul 4-atom, keduanya memiliki atom sentral yang terikat pada tiga atom lainnya. Namun, tidak seperti di molekul boron trifluorida, ada pasangan elektron yang sendirian dalam molekul amonia, yang membuatnya polar. Oleh karena itu, perbedaan utama antara amonia dan boron trifluorida adalah bahwa amonia adalah molekul polar, sedangkan boron trifluorida adalah molekul nonpolar.
Infografis berikut mencantumkan perbedaan antara amonia dan boron trifluorida dalam bentuk tabel untuk perbandingan berdampingan.
Ringkasan -amonia vs boron trifluoride
Amonia adalah senyawa anorganik yang memiliki formula kimia NH3, sedangkan boron trifluorida adalah senyawa anorganik yang memiliki formula kimia BF3. Perbedaan utama antara amonia dan boron trifluorida adalah bahwa amonia adalah molekul polar, sedangkan boron trifluorida adalah molekul nonpolar.
Referensi:
1. “Sintesis Amonia: Proses & Reaksi." Belajar.com
Gambar milik:
1. "Ammonia-2D" oleh Radio89-karya sendiri (CC BY-SA 3.0) Via Commons Wikimedia
2. “Boron-Trifluoride-2D-Dimension” oleh Ben Mills-karya sendiri (domain publik) melalui Commons Wikimedia


