Apa perbedaan antara konduktansi yang setara dan konduktansi molar
Itu Perbedaan utama antara konduktansi yang setara dan konduktansi molar adalah bahwa konduktansi yang setara adalah konduktansi elektrolit yang dibagi dengan jumlah ekuivalen elektrolit per unit volume, sedangkan konduktansi molar adalah konduktansi elektrolit yang dibagi dengan jumlah mol elektrolit.
Konduktansi molar adalah konduktansi semua ion yang disediakan oleh satu mol elektrolit yang ada dalam volume yang pasti dari larutan. Konduktansi yang setara adalah konduktansi volume larutan yang terdiri dari satu berat setara zat terlarut ketika ditempatkan di antara dua elektroda paralel.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu konduktansi yang setara
3. Apa itu konduktansi molar
4. Konduktansi setara vs konduktansi dalam bentuk tabel
5. Ringkasan -Konduktansi setara vs konduktansi molar
Apa itu konduktansi yang setara?
Konduktansi yang setara adalah konduktansi volume larutan yang terdiri dari satu berat setara zat terlarut ketika ditempatkan di antara dua elektroda paralel. Elektroda ditempatkan dengan jarak 1 cm di antara mereka. Itu cukup besar untuk mengandung solusi di antara mereka. Dapat digambarkan sebagai konduktansi bersih dari setiap ion yang dihasilkan dari 1 gram yang setara dengan suatu zat tertentu. Perhitungan untuk parameter ini dilakukan sebagai berikut:
λ = kv
Dalam persamaan ini, λ adalah konduktansi yang setara, k adalah konstan, dan v adalah volume dalam mililiter yang diberikan untuk 1 gram setara dari elektrolit yang kami gunakan untuk penentuan ini.

Apa itu konduktansi molar?
Konduktansi molar adalah konduktansi semua ion yang disediakan oleh satu mol elektrolit yang ada dalam volume yang pasti dari larutan. Istilah konduktivitas molar mengacu pada sifat memiliki konduktansi molar.
Konduktivitas molar adalah konduktivitas larutan elektrolitik yang diukur per unit konsentrasi molar larutan. Kita dapat menentukan ini sebagai konduktivitas larutan elektrolitik dibagi dengan konsentrasi molar elektrolit. Oleh karena itu, kita dapat memberikan konduktivitas molar dalam persamaan berikut:
Konduktivitas molar = k/c
K adalah konduktivitas yang diukur dari larutan elektrolitik, dan C adalah konsentrasi larutan elektrolitik.
Saat mempertimbangkan pengukuran konduktivitas molar, unit Si untuk pengukuran properti ini adalah Siemens Meter kuadrat per mol. Maka unit diberikan sebagai s m2 mol-1. Namun, paling sering, unit untuk properti ini adalah cm2 mol-1.
Apa perbedaan antara konduktansi yang setara dan konduktansi molar?
Konduktansi molar adalah konduktansi semua ion yang disediakan oleh satu mol elektrolit yang ada dalam volume yang pasti dari larutan. Konduktansi yang setara, di sisi lain, adalah konduktansi volume larutan yang terdiri dari satu berat setara zat terlarut ketika ditempatkan di antara dua elektroda paralel. Perbedaan utama antara konduktansi yang setara dan konduktansi molar adalah bahwa konduktansi yang setara adalah konduktansi elektrolit yang dibagi dengan jumlah ekuivalen elektrolit per satuan volume, sedangkan konduktansi molar adalah konduktansi elektrolit yang dibagi dengan jumlah mol dari elektrolit.
Infografis di bawah ini menyajikan perbedaan antara konduktansi setara dan konduktansi molar dalam bentuk tabel untuk perbandingan berdampingan.
Ringkasan -Konduktansi setara vs konduktansi molar
Konduktansi setara dan konduktansi molar adalah dua jenis konduktivitas. Perbedaan utama antara konduktansi yang setara dan konduktansi molar adalah bahwa konduktansi yang setara adalah konduktansi elektrolit yang dibagi dengan jumlah ekuivalen elektrolit per satuan volume, sedangkan konduktansi molar adalah konduktansi elektrolit yang dibagi dengan jumlah mol dari elektrolit.
Referensi:
1. “Konduktivitas molar." Tinjauan umum | Topik ScienceDirect.
Gambar milik:
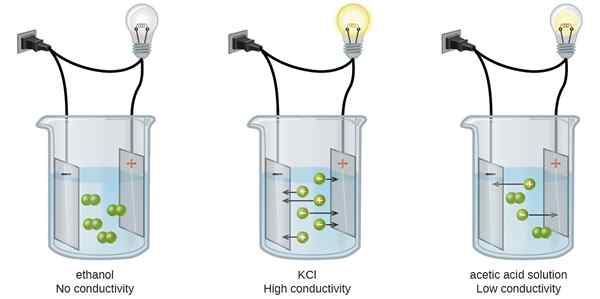
1. “Konduktivitas (Elektrolitik) 2” oleh Karishma50 - Karya Sendiri (CC BY -SA 4.0) Via Commons Wikimedia


