Apa perbedaan antara hukum konservasi massa dan hukum proporsi konstan
Itu Perbedaan utama antara hukum konservasi massa dan hukum proporsi konstan adalah bahwa hukum konservasi massa menjelaskan bahwa materi tidak dapat diciptakan atau dihancurkan tetapi diubah menjadi sesuatu yang lain, sedangkan hukum proporsi konstan menjelaskan bahwa senyawa kimia yang diberikan selalu mengandung elemen yang sama dalam proporsi yang sama persis dengan massa.
Hukum Konservasi Massa dan Hukum Proporsi Konstan adalah Hukum dalam Kimia yang Terkait dengan Massa.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa hukum konservasi massa
3. Apa hukum proporsi konstan
4. Hukum Konservasi Massa vs Hukum Proporsi Konstan dalam Bentuk Tabel
5. Ringkasan -Hukum Konservasi Massa vs Hukum Proporsi Konstan
Apa hukum konservasi massa?
Hukum konservasi massa adalah undang -undang yang menyatakan bahwa dalam sistem tertutup, yang tertutup untuk semua transfer materi dan energi, massa ini konstan dari waktu ke waktu. Ini berarti bahwa massa sistem tidak dapat berubah seiring waktu, sehingga jumlahnya tidak dapat ditambahkan atau dihapus. Dengan kata lain, massa dilestarikan dari waktu ke waktu. Ini juga dikenal sebagai prinsip konservasi massa.
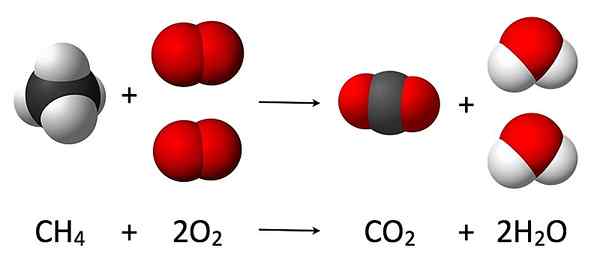
Menurut undang -undang ini, massa tidak dapat diciptakan atau dihancurkan meskipun dapat diatur ulang di luar angkasa. Selain itu, entitas yang terkait dengannya dapat mengubah formulir. E.G. Massa reaktan dalam reaksi kimia setara dengan massa produk. Oleh karena itu, dalam reaksi kimia dan proses termodinamika berenergi rendah yang terjadi dalam sistem yang terisolasi, total massa reaktan setara dengan massa produk.

Kita dapat merumuskan hukum konservasi massa dalam mekanika klasik di mana skala energi yang terkait dengan sistem yang terisolasi relatif lebih kecil dari MC2 (M adalah massa suatu objek, dan C adalah kecepatan cahaya). Ini harus diukur dalam kerangka referensi di mana objek sedang beristirahat.
Apa hukum proporsi konstan?
Hukum proporsi konstan menyatakan bahwa senyawa kimia yang diberikan selalu dapat terdiri dari elemen komponennya dalam rasio tetap dengan massa. Ini tidak tergantung pada sumber dan metode persiapannya. E.G. Dengan massa, air memiliki sekitar 8/9 oksigen dan 1/9 hidrogen.
Namun, undang -undang ini tidak benar secara universal. Misalnya, ada senyawa non-stoikiometrik yang memiliki komposisi unsur yang dapat bervariasi dari sampel ke sampel. Senyawa ini cenderung mengikuti hukum proporsi berganda. Misalnya, besi oksida wustit dapat mengandung atom besi dalam kisaran 0.83 hingga 0.95 untuk setiap atom oksigen (ini berarti non-stoikiometri). Meskipun formula kimianya yang ideal adalah FEO, eksperimen kristalografi memberikannya sebagai Fe0.95HAI.
Selain itu, komposisi isotop suatu elemen bervariasi tergantung pada sumbernya; Oleh karena itu, bahkan berkontribusi pada massa senyawa stoikiometrik murni yang dapat bervariasi. Variasi ini berguna dalam penanggalan radiometrik.
Apa perbedaan antara hukum konservasi massa dan hukum proporsi konstan?
Hukum Konservasi Massa dan Hukum Proporsi Konstan adalah Hukum dalam Kimia yang Terkait dengan Massa. Perbedaan utama antara hukum konservasi massa dan hukum proporsi yang konstan adalah bahwa hukum konservasi konservasi massa bahwa materi tidak dapat diciptakan atau dihancurkan tetapi diubah menjadi sesuatu yang lain, sedangkan hukum proporsi konstan menegaskan bahwa senyawa kimia yang diberikan selalu mengandung senyawa yang diberikan selalu mengandung senyawa yang diberikan selalu mengandung senyawa kimia yang diberikan tertentu yang diberikan yang diberikan yang diberikan selalu mengandung senyawa kimia yang diberikan tertentu yang diberikan tertentu tertentu yang diberikan tertentu elemen yang sama dalam proporsi yang sama persis dengan massa.
Di bawah ini adalah ringkasan dari perbedaan antara hukum konservasi massa dan hukum proporsi konstan dalam bentuk tabel untuk perbandingan berdampingan.
Ringkasan -Hukum Konservasi Massa vs Hukum Proporsi Konstan
Perbedaan utama antara hukum konservasi massa dan hukum proporsi konstan adalah hukum konservasi massa menjelaskan bahwa materi tidak dapat diciptakan atau dihancurkan tetapi diubah menjadi sesuatu yang lain, sedangkan hukum proporsi konstan menjelaskan bahwa senyawa kimia yang diberikan selalu mengandung hal yang sama elemen dalam proporsi yang sama persis dengan massa.
Referensi:
1. “Hukum Proust tentang proporsi konstan." Libreteks Kimia, Libretexts, 11 September. 2022.
Gambar milik:
1. "Reaksi Pembakaran Metana" oleh Jyntorobert a. Rohdejacek Fhjynto-Methane-3D-Space.SVGOXYGEN MOLECULE VDW.PNGCARBON-DIOXIDE-3D-VDW.SVGWATER MOLECULE 3D.SVG (domain publik) melalui Commons Wikimedia


