Perbedaan antara alkalinitas dan kesedihan
Perbedaan utama - alkalinitas vs. Basa
Dua istilah "alkalinitas" dan "kebusukan" cukup membingungkan. Sebagian besar orang tahu bahwa ada perbedaan antara dua parameter ini, tetapi hanya beberapa dari mereka yang dapat mendefinisikannya dengan benar. Itu perbedaan utama Di antara kedua istilah ini paling baik dijelaskan dalam definisi mereka. Basilisitas adalah ukuran yang secara langsung tergantung pada skala pH Dan Alkalinitas adalah berapa banyak asam yang diperlukan untuk menurunkan pH ke dalam nilai asam yang signifikan; itu juga dikenal sebagai kapasitas buffering badan air. Dengan kata lain, nilai pH solusi dasar bervariasi dari 7-14; di mana solusi dengan nilai pH tinggi lebih mendasar. Keduanya memiliki beberapa definisi, tetapi ide umumnya serupa.
Apa itu alkalinitas?
Alkalinitas adalah Salah satu parameter terpenting dalam tubuh akuatik, dan sangat penting bagi organisme akuatik. Alkalinitas mengukur kemampuan badan air untuk menetralkan asam dan basa. Dengan kata lain, ini adalah kapasitas buffering badan air untuk mempertahankan nilai pH pada nilai yang cukup stabil. Air yang mengandung bikarbonat (HCO3-), karbonat (CO32-) dan hidroksida (oh-) adalah buffer yang bagus; Mereka dapat bergabung dengan h+ ion dalam air untuk menaikkan pH (menjadi lebih mendasar) dari air. Saat alkalinitas terlalu rendah (kapasitas buffering rendah), asam apa pun yang ditambahkan ke badan air menurunkan pH ke nilai asam yang lebih tinggi.
 Apa itu Basa?
Apa itu Basa?
Basa Properti basis, diukur dalam skala pH. Basis adalah senyawa yang mengandung pH di atas 7; dari pH = 8 (kurang dasar) ke pH = 18 (lebih mendasar). Kebusukan senyawa dapat didefinisikan dalam tiga cara berbeda. Menurut teori arrhenius, basis adalah zat yang terdisosiasi dalam media berair yang menghasilkan oh- ion. Dalam teori lowry bronsted, akseptor proton disebut pangkalan. Menurut teori Lewis, donor pasangan elektron disebut basis. Basa adalah ionisasi kekuatan untuk menghasilkan OH- ion, kemampuan untuk menerima proton atau kemampuan untuk menyumbangkan elektron.

Thomas Martine Lowry - Teori Lowry Bronsted
Apa perbedaan antara alkalinitas dan kebasa?
Definisi Alkalinitas dan Basa:
Alkalinitas: Beberapa definisi ada.
Alkalinitas adalah kapasitas penetral asam zat terlarut dalam sampel air yang diukur dalam miliequivalents per liter.
Jumlah spesies kimia karbonat dan non -karbonat titratable dalam sampel air yang disaring.
Kapasitas air untuk menetralkan larutan asam.
Kapasitas buffering air untuk mempertahankan pH yang cukup stabil, tanpa mengubah nilai pH, saat asam ditambahkan.
Basa: Tiga teori digunakan untuk mendefinisikan keasaman dan kesedihan.
Arrenhius: Pangkalan adalah spesies yang terionisasi untuk menghasilkan oh- di dalam air. Basilisitas meningkat saat mereka lebih banyak mengionisasi, memberi oh- di dalam air.
Bronsted-Lowry: Proton (h+) akseptor disebut basis.
Lewis: Donor pasangan elektron disebut pangkalan.
Faktor -faktor yang mempengaruhi alkalinitas dan kebasaan:
Alkalinitas: Alkalinitas tidak tergantung pada nilai pH; Tubuh air dapat memiliki nilai pH yang lebih rendah (sangat asam) atau lebih tinggi (dasar) dengan nilai alkalinitas yang lebih tinggi. Alkalinitas ditentukan oleh beberapa faktor seperti batu, tanah, garam, dan aktivitas industri tertentu (Air limbah yang mengandung sabun dan deterjen adalah alkali) oleh manusia. Misalnya, area di mana batu kapur (Caco3) secara signifikan tersedia dapat memiliki lebih banyak air basa.
Basa: Faktor -faktor yang mempengaruhi kebasaan senyawa bervariasi tergantung pada definisi kebasa. Misalnya, ketersediaan pasangan elektron basa tergantung pada tiga faktor.
Elektronegativitas: Ch3-> nh2-> ho-> f-
Saat mempertimbangkan atom -atom di baris yang sama di tabel periodik, atom paling elektronegatif memiliki kesedihan yang lebih tinggi.
Ukuran: F-> cl-> br-> i-
Saat mempertimbangkan deretan tabel periodik, semakin besar atom memiliki kepadatan elektron yang lebih sedikit dan kurang mendasar.
Resonansi: Ro-> rco2-
Molekul yang memiliki lebih banyak struktur resonansi kurang mendasar, karena ketersediaan elektron yang kurang dari muatan negatif yang terlokalisasi.
Gambar milik:
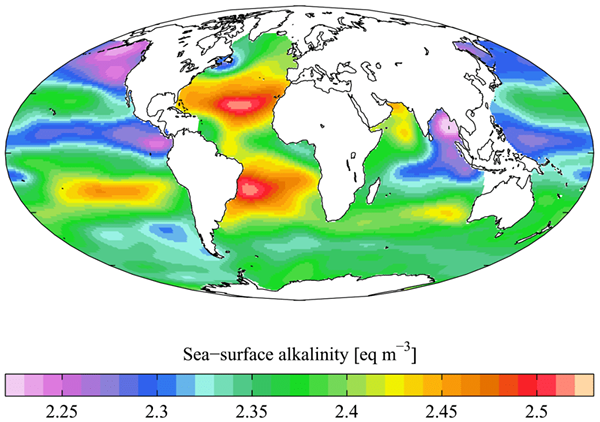
1. “WOA05 GlodaP PD ALK Ayool” oleh Plumbago - karya sendiri. [CC BY-SA 3.0] Via Commons
2. "Thomas Martin Lowry2" oleh Anonymous - Obituary oleh Faraday Soc. (1936). [Domain publik] via commons


