Perbedaan antara benzena dan fenil
Itu perbedaan utama antara benzena dan fenil adalah itu Benzene adalah hidrokarbon siklik dalam bentuk segi enam, hanya mengandung atom karbon dan hidrogen, sedangkan fenil adalah turunan dari benzena, diciptakan oleh penghilangan atom hidrogen. Oleh karena itu, benzena mengandung enam atom hidrogen sementara fenil mengandung lima atom hidrogen.
Benzene adalah hidrokarbon aromatik paling sederhana dan berfungsi sebagai senyawa induk untuk banyak senyawa aromatik penting. Fenil adalah molekul hidrokarbon dengan formula C6H5. Ini sebenarnya adalah turunan dari benzena dan oleh karena itu, memiliki sifat yang sama dengan benzena.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu benzena
3. Apa itu fenil
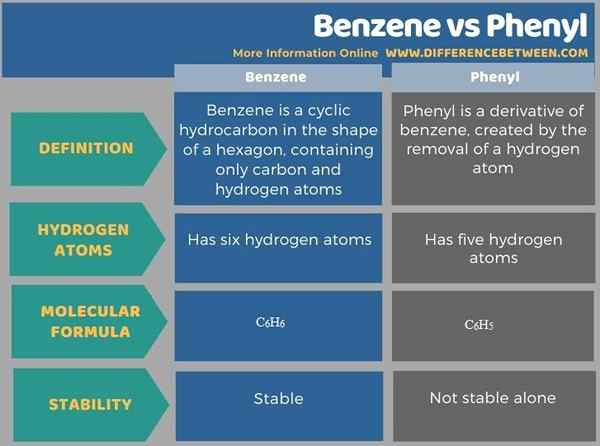
4. Perbandingan berdampingan - benzena vs fenil dalam bentuk tabel
5. Ringkasan
Apa itu benzena?
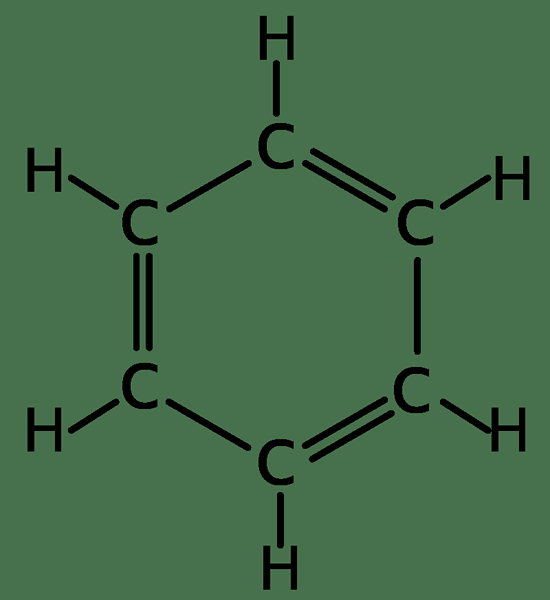
Benzene hanya memiliki atom karbon dan hidrogen yang diatur untuk memberikan struktur planar. Ini memiliki formula molekul C6H6. Struktur benzena ditemukan oleh Kekule pada tahun 1872. Karena aromatik, berbeda dari senyawa alifatik.

Strukturnya dan beberapa sifatnya adalah sebagai berikut.
Berat Molekul: 78 g Mole-1
Titik didih: 80.1 HaiC
Titik Melting: 5.5 HaiC
Kepadatan: 0.8765 g cm-3
Benzene adalah cairan yang tidak berwarna dengan bau manis. Itu mudah terbakar dan menguap dengan cepat saat terpapar. Benzena digunakan sebagai pelarut karena dapat melarutkan banyak senyawa non-polar. Namun, benzena sedikit larut dalam air. Struktur benzena unik dibandingkan dengan hidrokarbon alifatik lainnya; Oleh karena itu, benzena memiliki sifat unik.
Semua karbon di benzena memiliki tiga SP2 Orbital hibridisasi. Dua orbital hibridisasi SP2 dari karbon tumpang tindih dengan SP2 Orbital hibridisasi karbon yang berdekatan di kedua sisi. SP lainnya2 orbital hibridasi tumpang tindih dengan orbital hidrogen untuk membentuk ikatan σ. Elektron dalam orbital P karbon tumpang tindih dengan elektron atom karbon di kedua sisi, membentuk ikatan PI. Tumpang tindih elektron ini terjadi di semua enam atom karbon dan, oleh karena itu, menghasilkan sistem ikatan PI, yang tersebar di seluruh cincin karbon. Dengan demikian, elektron -elektron ini dikatakan didelokalisasi. Delokalisasi elektron berarti tidak ada ikatan ganda dan tunggal bergantian. Oleh karena itu, semua panjang ikatan C-C sama, dan panjangnya antara panjang ikatan tunggal dan rangkap. Karena delokalisasi cincin benzena stabil, ia enggan menjalani reaksi penambahan, tidak seperti alkena lainnya.
Apa itu fenil?
Fenil adalah molekul hidrokarbon dengan formula C6H5. Ini berasal dari benzena; Oleh karena itu, ia memiliki sifat yang sama seperti benzena. Namun, ini berbeda dari benzena karena kurangnya atom hidrogen dalam satu karbon. Oleh karena itu, berat molekul fenil adalah 77 g mol-1. Fenil disingkat pH. Biasanya, fenil melekat pada gugus fenil lain, atom atau molekul (bagian ini dikenal sebagai substituen).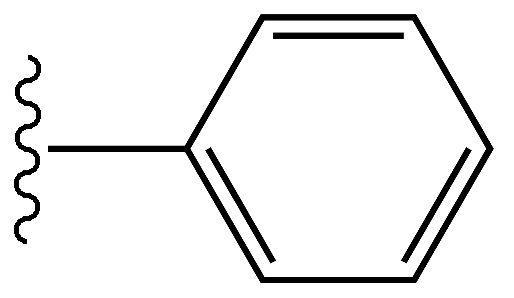
Atom karbon fenil adalah SP2 hibridisasi seperti di benzena. Semua karbon dapat membentuk tiga ikatan sigma. Dua ikatan sigma dibentuk dengan dua karbon yang berdekatan sehingga akan menimbulkan struktur cincin. Ikatan sigma lainnya dibentuk dengan atom hidrogen. Namun, dalam satu karbon di atas ring, ikatan sigma ketiga dibentuk dengan atom atau molekul lain daripada atom hidrogen. Elektron dalam orbital p tumpang tindih satu sama lain untuk membentuk awan elektron yang didelokalisasi. Oleh karena itu, fenil memiliki panjang ikatan C-C yang serupa antara semua karbon, terlepas dari memiliki ikatan tunggal dan rangkap bergantian. Panjang ikatan C-C ini sekitar 1.4 Å. Cincin itu planar dan memiliki sudut 120o antara ikatan di sekitar karbon.
Karena kelompok substituen fenil, polaritas dan sifat kimia atau fisik lainnya berubah. Jika substituen menyumbangkan elektron ke awan elektron yang terdelokalisasi, yang dikenal sebagai kelompok doning elektron (E.G. -OCH3, NH2). Jika substituen menarik elektron dari awan elektron, ia dikenal sebagai substituen yang menarik elektron. (E.G. -NO2, -COOH). Kelompok fenil stabil karena aromatiknya, sehingga mereka tidak mudah menjalani oksidasi atau pengurangan. Selanjutnya, mereka hidrofobik dan non-polar.
Apa perbedaan antara benzena dan fenil?
Pada dasarnya, fenil berasal dari benzena. Perbedaan utama antara benzena dan fenil adalah bahwa benzena adalah hidrokarbon siklik dalam bentuk segi enam, yang hanya mengandung atom karbon dan hidrogen, sedangkan fenil adalah turunan dari benzena, yang diciptakan oleh penghilangan atom hidrogen. Selain itu, formula molekul benzena adalah C6H6 dan, untuk fenil, itu c6H5. Fenil saja tidak stabil seperti benzena.
Ringkasan -benzena vs fenil
Perbedaan utama antara benzena dan fenil adalah bahwa benzena adalah hidrokarbon siklik dalam bentuk segi enam, yang hanya mengandung atom karbon dan hidrogen, sedangkan fenil adalah turunan dari benzena, yang diciptakan oleh penghilangan atom hidrogen.
Gambar milik:
1. "Diagram Struktural Benzene" oleh Vladsinger - karya sendiri (domain publik) melalui Commons Wikimedia
2. "Fenil Radical Group" oleh Samuele Madini - karya sendiri (domain publik) melalui Commons Wikimedia


