Perbedaan antara karbon tetrachloride dan natrium klorida

Itu perbedaan utama Antara karbon tetraklorida dan natrium klorida adalah itu karbon tetraklorida adalah senyawa kimia kovalen sedangkan natrium klorida adalah senyawa kimia ionik.
Baik karbon tetraklorida dan natrium klorida adalah senyawa kimia yang mengandung klorin. Namun, kedua senyawa kimia ini berbeda satu sama lain sesuai dengan struktur kimia, sifat dan aplikasi.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu karbon tetrachloride
3. Apa itu natrium klorida
4. Perbandingan berdampingan - karbon tetraklorida vs natrium klorida dalam bentuk tabel
5. Ringkasan
Apa itu karbon tetrachloride?
Karbon tetraklorida adalah senyawa kimia yang memiliki formula kimia CCL4. Itu umumnya disebut "tetrachloromethane". Karbon tetraklorida adalah cairan tidak berwarna yang memiliki aroma manis. Oleh karena itu, mudah untuk mendeteksi senyawa ini dari baunya bahkan pada tingkat rendah.
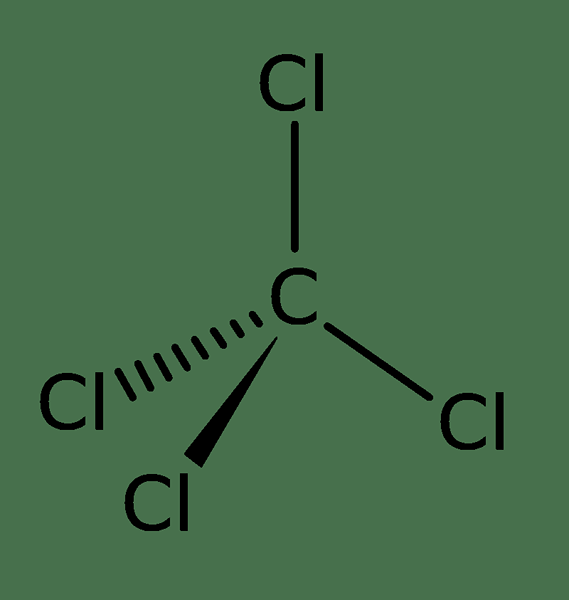
Gambar 01: Struktur karbon tetrachloride
Massa molar karbon tetrachloride adalah 153.81 g/mol. Ini memiliki titik leleh −22.92 ° C, dan titik didih adalah 76.72 ° C. Saat mempertimbangkan geometri molekul karbon tetraklorida, ia memiliki geometri tetrahedral. Ada empat atom klorin yang terikat pada atom karbon tunggal, dan sudut ikatan molekul sama. Oleh karena itu, kami menyebutnya "geometri simetris". Geometri ini membuat senyawa nonpolar. Ini menyerupai struktur molekul metana, yang memiliki empat atom hidrogen yang terikat pada atom karbon tunggal.
Ada banyak kegunaan karbon tetrachloride. Sebelum larangan, senyawa ini digunakan untuk menghasilkan CFC dalam skala besar. Saat ini, kami tidak menghasilkan CFC karena membahayakan lapisan ozon. Karbon tetraklorida adalah bahan utama dalam lampu lava. Setelah itu adalah pelarut yang populer, tetapi sekarang kami tidak menggunakannya karena efek kesehatannya yang merugikan. Selain itu, kami banyak menggunakannya dalam alat pemadam api, sebagai pendahulu untuk refrigeran dan sebagai agen pembersih.
Apa itu natrium klorida?
Sodium klorida adalah senyawa anorganik yang memiliki formula kimia NaCl. Massa molar senyawa ini adalah 58.44 g/mol. Pada suhu dan tekanan kamar, natrium klorida muncul dalam keadaan padat, sebagai kristal tidak berwarna. Selain itu, zat ini tidak berbau. Dalam bentuk murni, natrium klorida tidak dapat menyerap uap air, yang berarti, itu bukan higroskopis.

Gambar 02: Kristal Sodium Klorida
Sodium klorida adalah garam natrium, jadi itu adalah senyawa ionik. Senyawa ini mengandung satu atom chorine per setiap atom natrium molekul. Garam natrium klorida bertanggung jawab atas salinitas air laut. Titik leleh adalah 801◦C saat titik didih 1413◦C. Dalam kristal natrium klorida, setiap kation natrium dikelilingi dengan enam ion klorida dan sebaliknya. Oleh karena itu, kami menyebut sistem kristal sebagai sistem kubik yang berpusat pada wajah.
Sodium klorida larut dalam senyawa polar tinggi seperti air. Di sini, molekul air mengelilingi setiap kation dan anion. Setiap ion sering memiliki enam molekul air di sekitarnya. Namun, pH natrium klorida berair terletak di sekitar pH7 karena kesedihan yang lemah dari ion klorida. Kami mengatakan tidak ada efek natrium klorida pada pH larutan.
Apa perbedaan antara karbon tetraklorida dan natrium klorida?
Baik karbon tetraklorida dan natrium klorida adalah senyawa kimia yang mengandung klorin. Perbedaan utama antara karbon tetraklorida dan natrium klorida adalah bahwa karbon tetraklorida adalah senyawa kimia kovalen sedangkan natrium klorida adalah senyawa kimia ionik. Selain itu, karbon tetraklorida larut dalam pelarut nonpolar sementara natrium klorida larut dalam pelarut kutub.
Di bawah Infograhic merangkum perbedaan antara karbon tetraklorida dan natrium klorida dalam bentuk tabel.

Ringkasan -karbon tetraklorida vs natrium klorida
Karbon tetraklorida dan natrium klorida berbeda satu sama lain sesuai dengan struktur kimia, sifat dan aplikasinya. Perbedaan utama antara karbon tetraklorida dan natrium klorida adalah bahwa karbon tetraklorida adalah senyawa kimia kovalen sedangkan natrium klorida adalah senyawa kimia ionik.
Referensi:
1. Haskins, J. (2018, 29 September). Apa itu natrium klorida dan bagaimana cara digunakan? Diperoleh 14 Oktober 2020, tersedia di sini.
Gambar milik:
1. "Karbon Tetraklorida" oleh H Padleckas, diveksia oleh Maxdz8 - H Padleckas, diveksia oleh Maxdz8, domain publik) melalui Commons Wikimedia
2. “Sodium Chloride Crystals” oleh Stanislav.Nevyhosteny - Pekerjaan Sendiri (CC BY -SA 4.0) Via Commons Wikimedia


