Perbedaan antara pengurangan karbotermik dan metalotermik
Itu perbedaan utama Antara pengurangan karbotermik dan metalotermik adalah itu Dalam reduksi karbotermik, zat pereduksi adalah karbon, sedangkan, dalam reduksi metalotermik, zat pereduksi adalah logam.
Reduksi karbotermik dan reduksi metalotermik adalah reaksi yang sangat penting dalam mendapatkan logam murni. Reaksi ini diterapkan terutama dalam proses industri.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu pengurangan karbotermik
3. Apa itu pengurangan metalotermik
4. Perbandingan Berdampingan - Pengurangan Carbothermic vs Metallotermic dalam Bentuk Tabel
5. Ringkasan
Apa itu pengurangan karbotermik?
Reaksi reduksi karbotermik adalah jenis reaksi kimia di mana reduksi zat seperti logam oksida terjadi dengan adanya karbon. Di sini, karbon cenderung bertindak sebagai agen pereduksi. Biasanya, jenis reaksi kimia ini terjadi pada suhu yang sangat tinggi. Reaksi reduksi karbotermik ini sangat penting dalam produksi bentuk unsur dari banyak elemen. Kami dapat dengan mudah memprediksi kemampuan logam untuk berpartisipasi dalam reaksi karbotermik menggunakan diagram Ellingham.
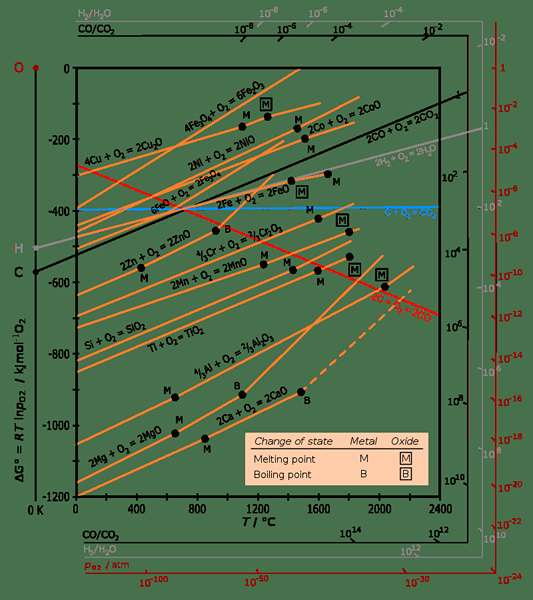
Diagram Ellingham adalah grafik yang menunjukkan ketergantungan suhu stabilitas senyawa. Secara umum, analisis ini berguna dalam meningkatkan kemudahan pengurangan oksida logam dan sulfida. Nama itu berasal dari penemuannya oleh Harold Ellingham pada tahun 1944.

Gambar 01: Diagram Ellingham
Reaksi reduksi karbotermik terkadang dapat menghasilkan karbon monoksida dan bahkan karbon dioksida. Kita dapat menggambarkan konversi reaktan menjadi produk mengenai perubahan entropi. Dalam reaksi ini, dua senyawa padat (logam oksida dan karbon) dikonversi menjadi senyawa padat baru (logam), dan gas (karbon monoksida atau karbon dioksida). Reaksi terakhir memiliki entropi tinggi.
Ada banyak aplikasi reaksi reduksi karbotermik, termasuk peleburan bijih besi sebagai aplikasi utama. Di sini, bijih besi berkurang di hadapan karbon sebagai zat pereduksi. Reaksi ini memberikan logam besi dan karbon dioksida sebagai produk. Contoh penting lainnya adalah proses LeBlanc di mana natrium sulfat bereaksi dengan karbon, memberikan natrium sulfida dan karbon dioksida.
Apa itu pengurangan metalotermik?
Reaksi reduksi metalotermik adalah jenis reaksi kimia yang dilakukan untuk mendapatkan logam target atau paduan dari bahan pakan seperti oksida atau klorida dengan menggunakan logam sebagai zat pereduksi. Sebagian besar logam reaktif diperoleh melalui proses reduksi ini. E.G. Titanium Metal.
Contoh umum dari jenis reaksi ini adalah pemurnian logam niobium. Dalam reaksi reduksi ini, niobium oksida dikurangi oleh logam aluminium untuk menghasilkan logam niobium dan aluminium oksida. Ini adalah reaksi eksotermik di mana pengotor oksida terak, dan kita dapat menghilangkannya dari logam niobium cair.
Apa perbedaan antara pengurangan karbotermik dan metalotermik?
Pengurangan karbotermik dan reduksi metalotermik adalah reaksi yang sangat penting dalam mendapatkan logam murni. Reaksi reduksi karbotermik adalah jenis reaksi kimia di mana reduksi zat seperti logam oksida terjadi dengan adanya karbon. Reaksi reduksi metalotermik, di sisi lain, adalah jenis reaksi kimia dilakukan untuk mendapatkan logam target atau paduan dari bahan pakan seperti oksida atau klorida dengan menggunakan logam sebagai zat pereduksi. Perbedaan utama antara pengurangan karbotermik dan metalotermik adalah bahwa dalam reduksi karbotermik zat pereduksi adalah karbon sedangkan dalam reduksi metalotermik zat pereduksi adalah logam.
Di bawah Infografis merangkum perbedaan antara pengurangan karbotermik dan metalotermik dalam bentuk tabel.

Ringkasan -Pengurangan karbotermik vs metallotermic
Pengurangan karbotermik dan reduksi metalotermik adalah reaksi yang sangat penting dalam mendapatkan logam murni. Perbedaan utama antara pengurangan karbotermik dan metalotermik adalah bahwa dalam reduksi karbotermik, zat pereduksi adalah karbon, sedangkan, dalam reduksi metalotermik, zat pereduksi adalah logam.
Referensi:
1. “Pengurangan metalotermik.Sains langsung, tersedia di sini.
Gambar milik:
1. “Ellingham Richardson-Diagram English” oleh Dersilberspiegel-buatan sendiri dengan sebagian besar data dari sini [1] (CC BY-SA 4.0) Via Commons Wikimedia


