Perbedaan antara senyawa dan larutan
Itu perbedaan utama Antara senyawa dan larutan adalah itu Senyawa mengandung dua atau lebih elemen yang secara kimia terikat bersama sedangkan larutan memiliki beberapa zat yang tidak terikat secara kimia bersama seperti senyawa.
Senyawa dan larutan adalah campuran elemen atau senyawa lainnya. Elemen tunggal hampir tidak stabil dalam kondisi alami. Mereka membentuk berbagai kombinasi di antara mereka atau dengan elemen lain agar ada. Ketika ini terjadi, sifat-sifat elemen tunggal bervariasi dan menimbulkan campuran baru-ke-novel.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu Senyawa
3. Apa itu solusi
4. Perbandingan berdampingan - senyawa vs larutan dalam bentuk tabel
5. Ringkasan
Apa itu Senyawa?
Senyawa adalah zat kimia yang mengandung dua atau lebih elemen kimia yang berbeda. Namun, kami tidak mempertimbangkan kombinasi dua atau lebih elemen kimia yang sama dengan senyawa; Mereka adalah molekul, bukan senyawa. Misalnya, molekul diatomik seperti O2, H2, N2 atau molekul polyatomik seperti p4 bukan senyawa, tetapi mereka adalah molekul. Beberapa contoh senyawa umum adalah NaCl, h2OH TIDAK3, dan C6H12HAI6.
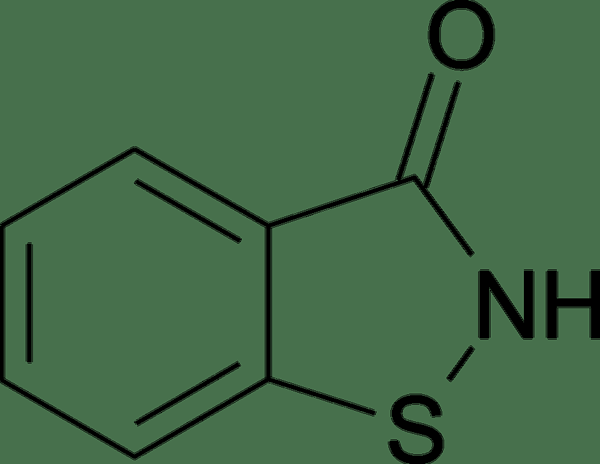
Gambar 01: Molekul yang memiliki lebih dari satu elemen kimia adalah senyawa
Oleh karena itu, senyawa adalah subset dari molekul; Dengan demikian, semua senyawa adalah molekul, tetapi tidak semua molekul adalah senyawa. Elemen dalam senyawa bergabung satu sama lain melalui ikatan kovalen, ikatan ionik, ikatan logam, dll. Struktur senyawa memberikan jumlah atom dalam senyawa dan rasio mereka. Dalam suatu senyawa, elemen hadir dalam proporsi yang pasti. Kita dapat menemukan detail ini dengan mudah dengan melihat formula kimia suatu senyawa. Selain itu, senyawanya stabil, dan mereka memiliki bentuk karakteristik, warna, sifat, dll.
Apa itu solusi?
Solusi adalah campuran homogen dari dua atau lebih zat. Kami menyebutnya campuran yang homogen karena komposisinya seragam di seluruh larutan. Komponen solusi terutama dari dua jenis sebagai zat terlarut dan pelarut. Pelarut melarutkan zat terlarut dan membentuk larutan yang seragam. Oleh karena itu, jumlah pelarut biasanya lebih tinggi dari jumlah zat terlarut.

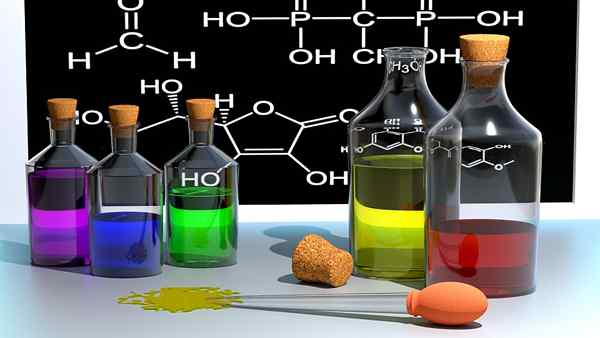
Gambar 02: Solusi yang berbeda
Selain itu, semua partikel dalam larutan memiliki ukuran molekul atau ion. Jadi, kita tidak dapat mengamatinya dengan mata telanjang. Juga, solusinya dapat memiliki warna jika pelarut atau zat terlarut dapat menyerap cahaya yang terlihat. Namun, solusi biasanya transparan.
Selain itu, campuran ini dapat terjadi dalam keadaan cair, gas atau padat. Tapi, pelarut yang paling umum adalah cairan. Juga, di antara cairan, kami menganggap air sebagai pelarut universal, karena dapat melarutkan banyak zat daripada pelarut lainnya. Selain itu, kita dapat melarutkan gas, padatan atau zat terlarut cair lainnya dalam pelarut cair. Namun, dalam pelarut gas, hanya zat terlarut gas yang akan larut.
Ada batasan jumlah zat terlarut yang dapat kami tambahkan ke sejumlah pelarut tertentu. Saat mencapai batas maksimum, solusinya menjadi jenuh. Tetapi, jika jumlah zat terlarut sangat rendah, solusinya menjadi encer. Jika ada jumlah zat terlarut yang tinggi dalam larutan, itu adalah solusi terkonsentrasi. Dengan mengukur konsentrasi larutan, kita bisa mendapatkan ide tentang jumlah zat terlarut dalam larutan.
Apa perbedaan antara senyawa dan larutan?
Senyawa adalah zat kimia yang mengandung dua atau lebih elemen kimia yang berbeda yang terikat satu sama lain. Sedangkan, solusi adalah campuran homogen dari dua atau lebih zat. Oleh karena itu, perbedaan utama antara senyawa dan larutan adalah bahwa suatu senyawa mengandung dua atau lebih elemen yang secara kimia terikat bersama sedangkan larutan memiliki beberapa zat yang tidak terikat secara kimia bersama seperti senyawa.
Selain itu, dalam suatu senyawa, elemen hadir dalam rasio yang ditentukan, tetapi dalam larutan, komponen di dalamnya tidak harus ada dalam jumlah yang pasti. Juga, perbedaan vital lain antara senyawa dan larutan adalah bahwa kita dapat memisahkan komponen dalam larutan dengan metode kimia dan fisik, tetapi kita dapat memisahkan komponen dalam senyawa dengan cara kimia saja saja.
Infografis di bawah ini tentang perbedaan antara senyawa dan larutan memberikan rincian lebih lanjut tentang perbedaan ini.

Ringkasan -Solusi senyawa vs
Senyawa dan larutan adalah campuran dari elemen kimia. Perbedaan utama antara senyawa dan larutan adalah bahwa suatu senyawa mengandung dua atau lebih elemen yang secara kimiawi terikat bersama sedangkan larutan memiliki beberapa zat yang tidak terikat secara kimia bersama seperti senyawa.
Referensi:
1. Helmenstine, Anne Marie, PH.D. “Definisi majemuk dalam kimia."Thoughtco, SEP. 11, 2018. Tersedia disini
2. Helmenstine, Anne Marie, PH.D. “Definisi Solusi dalam Kimia."Thoughtco, OCT. 5, 2018. Tersedia disini
Gambar milik:
1."147356" oleh openclipart-vektor (CC0) melalui Pixabay
2."740453" oleh Mastertux (CC0) melalui Pixabay


