Perbedaan antara deuterium dan tritium
Itu perbedaan utama antara deuterium dan tritium adalah itu Nukleus deuterium memiliki satu neutron sedangkan nukleus tritium memiliki dua neutron.
Hidrogen adalah elemen pertama dan terkecil dalam tabel periodik, yang kami tunjukkan sebagai h. Ini memiliki satu elektron dan satu proton. Kami dapat mengkategorikannya di bawah Grup 1 dan Periode 1 dalam tabel periodik karena konfigurasi elektronnya: 1S1. Hidrogen dapat mengambil elektron untuk membentuk ion bermuatan negatif, atau dapat dengan mudah menyumbangkan elektron untuk menghasilkan proton yang bermuatan positif. Jika tidak, itu dapat berbagi elektron untuk membuat ikatan kovalen. Karena kemampuan ini, hidrogen hadir dalam sejumlah besar molekul, dan itu adalah elemen yang sangat berlimpah di bumi. Hidrogen memiliki tiga isotop sebagai pratium-1H (tanpa neutron), deuterium-2h (satu neutron) dan tritium-3H (dua neutron). Protium adalah yang paling berlimpah di antara ketiganya, memiliki sekitar 99% kelimpahan relatif.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu deuterium
3. Apa itu Tritium
4. Perbandingan berdampingan - deuterium vs tritium dalam bentuk tabel
5. Ringkasan
Apa itu deuterium?
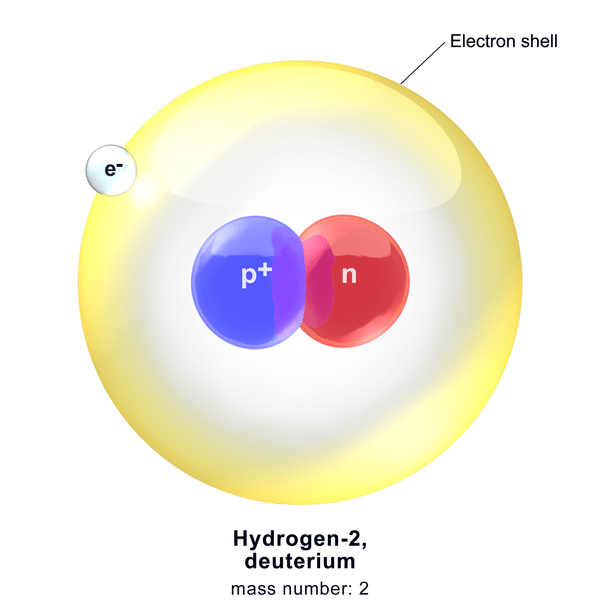
Deuterium adalah salah satu isotop hidrogen. Itu adalah isotop stabil dengan 0.015% kelimpahan alami. Ada proton dan neutron di inti deuterium. Oleh karena itu, jumlah massanya adalah dua, dan angka atom adalah satu. Kami menyebut isotop ini sebagai hidrogen berat dan ditampilkan sebagai 2H. Namun, paling umum, kami mewakili itu dengan D.

Gambar 1: Deuterium
Deuterium dapat ada sebagai molekul gas diatomik dengan formula kimia D2. Namun, kemungkinan bergabung dengan dua atom D di alam rendah karena kelimpahan yang lebih rendah. Oleh karena itu, isotop ini sebagian besar berikatan dengan atom 1 jam yang membuat gas -HD (hidrogen deuterida). Juga, dua atom deuterium dapat mengikat dengan oksigen untuk membentuk d2o analog air, yang kami sebut air tebal.
Selain itu, molekul dengan deuterium menunjukkan sifat kimia dan fisik yang berbeda dari analog hidrogen dari mereka. Misalnya, itu dapat menunjukkan efek isotop kinetik. Selain itu, senyawa deuterasi menunjukkan perbedaan karakteristik dalam NMR, IR dan spektroskopi massa; Oleh karena itu, kami dapat mengidentifikasinya menggunakan metode tersebut. Juga, deuterium memiliki putaran satu. Oleh karena itu, di NMR, kopling isotop ini memberikan kembar tiga. Selain itu, ia menyerap frekuensi IR yang berbeda dari hidrogen dalam spektroskopi IR. Karena perbedaan massa yang besar, dalam spektroskopi massa, deuterium dapat dibedakan dari hidrogen.
Apa itu Tritium?
Tritium adalah isotop hidrogen yang jumlah massanya tiga. Oleh karena itu, inti tritium memiliki satu proton dan dua neutron. Itu hanya ada dalam jumlah jejak di alam karena radioaktivitasnya. Karena alasan ini, itu harus diproduksi secara artifisial untuk penggunaan praktis.
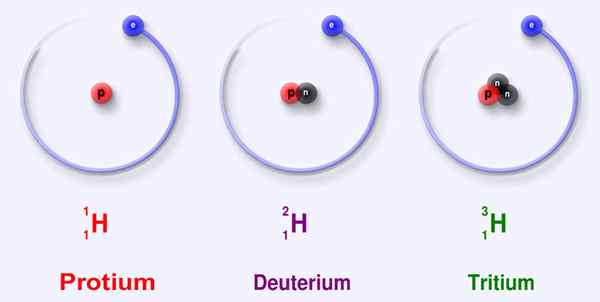
Gambar 02: Tiga isotop utama hidrogen
Tritium adalah isotop radioaktif (ini adalah satu -satunya isotop radioaktif hidrogen). Ini memiliki waktu paruh 12 tahun, dan meluruh dengan memancarkan partikel beta untuk menghasilkan helium-3. Massa atom isotop ini adalah 3.0160492. Selain itu, itu ada sebagai gas (HT) pada suhu dan tekanan standar. Juga, dapat membentuk oksida (HTO), yang kami sebut “air trisied.”Tritium berguna dalam membuat senjata nuklir dan sebagai pelacak dalam studi biologis dan lingkungan.
Apa perbedaan antara deuterium dan tritium?
Deuterium dan tritium adalah dua isotop hidrogen. Perbedaan utama antara deuterium dan tritium adalah bahwa nukleus deuterium memiliki satu neutron sedangkan nukleus tritium memiliki dua neutron. Selanjutnya, jumlah massa deuterium adalah 2.0135532 sedangkan jumlah massa tritium adalah 3.0160492. Jadi, ini adalah perbedaan signifikan lainnya antara deuterium dan tritium.
Selain itu, perbedaan lebih lanjut antara deuterium dan tritium adalah bahwa deuterium adalah isotop yang stabil dan kita dapat menemukannya di alam sedangkan tritium adalah isotop radioaktif yang tidak dapat kita temukan di alam. Namun, kita dapat memproduksinya secara artifisial untuk penggunaan praktis.

Ringkasan -Deuterium vs Tritium
Deuterium dan tritium adalah isotop dari elemen kimia hidrogen. Perbedaan utama antara deuterium dan tritium adalah bahwa deuterium nukleus memiliki satu neutron sedangkan nukleus tritium memiliki dua neutron. Selain itu, tritium bersifat radioaktif sedangkan deuterium adalah isotop yang stabil.
Referensi:
1. Helmenstine, Anne Marie, PH.D. “Fakta Deuterium."Thoughtco, Apr. 2, 2019, tersedia di sini.
Gambar milik:
1. “Blausen 0527 Hydrogen -2 Deuterium” oleh Bruceblaus - karya sendiri (CC oleh 3.0) Via Commons Wikimedia
2. “Protium Deuterium Tritium” oleh Lamiot untuk versi Prancis, dari Dirk Hünniger - Self, Terjemahan dari Dirk Hünniger (Jerman Wikipedia) (CC BY -SA 3.0) Via Commons Wikimedia


