Perbedaan antara heksana dan n-heksana
Itu perbedaan utamaE antara heksana dan n-heksana adalah itu Hexane memiliki struktur bercabang, sedangkan n-heksana adalah struktur heksana yang tidak bercabang.
Molekul organik adalah molekul yang terdiri dari karbon. Hidrokarbon adalah molekul organik yang hanya terdiri dari atom karbon dan hidrogen. Hidrokarbon bisa aromatik atau alifatik. Mereka terutama dibagi menjadi beberapa jenis sebagai alkana, alkena, alkin, sikloalkanes dan hidrokarbon aromatik. Heksana dan n-heksana adalah alkana, atau sebaliknya, dikenal sebagai hidrokarbon jenuh. Mereka memiliki jumlah atom hidrogen tertinggi yang dapat ditampung molekul. Semua ikatan antara atom karbon dan hidrogen adalah ikatan tunggal. Oleh karena itu, rotasi ikatan diperbolehkan antara atom apa pun. Mereka adalah jenis hidrokarbon yang paling sederhana. Hidrokarbon jenuh memiliki formula umum CNH2N+2. Kondisi ini sedikit berbeda untuk sikloalkana karena mereka memiliki struktur siklik.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu heksana
3. Apa itu n-heksana
4. Perbandingan berdampingan - heksana vs n -heksana dalam bentuk tabel
5. Ringkasan
Apa itu heksana?
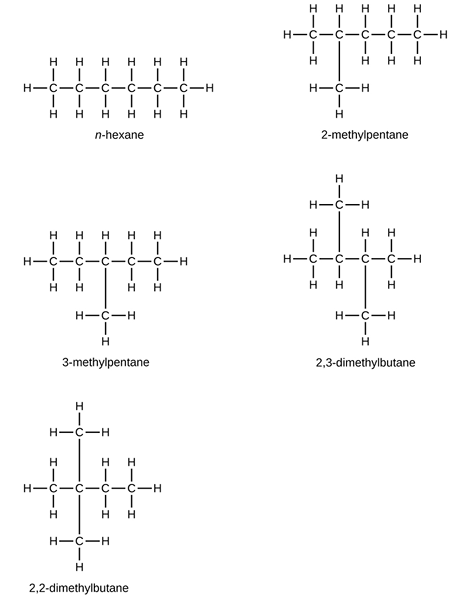
Seperti yang dinyatakan di atas, hidrokarbon adalah alkana jenuh. Ini memiliki enam atom karbon; Oleh karena itu, memiliki formula C6H14. Massa molar heksana adalah 86.18 g Mol−1. Hexane adalah nama umum yang digunakan untuk menunjukkan semua molekul dengan formula ini. Ada sejumlah isomer struktural yang dapat kita gambar agar sesuai dengan rumus ini tetapi, dalam nomenklatur IUPAC, kami menggunakan heksana secara khusus untuk menunjukkan molekul yang tidak bercabang, dan juga dikenal sebagai n-heksana. Isomer struktural lainnya seperti molekul yang dimetilasi dari pentana dan butana. Mereka dikenal sebagai isohexane dan neohexane. Mereka memiliki struktur berikut.

Dari struktur heksana ini, 2-methylpentane, 3-methylpentane dan 2,3-dimethylbutane adalah contoh isoheksana, sedangkan 2,2-dimethylbutane adalah contoh untuk neoheksana.
Hexane terutama diproduksi dalam proses pemurnian minyak mentah. Heksana diekstraksi saat minyak mendidih pada 65-70 ° C. Karena isomer heksana memiliki titik didih yang agak mirip, mereka menguap pada kisaran suhu yang sama. Namun, titik leleh mereka berbeda. Heksana dalam bentuk cair pada suhu kamar dan memiliki bau seperti bensin. Itu adalah cairan yang tidak berwarna. Heksana sedikit larut dalam air. Pada suhu kamar, cenderung menguap perlahan ke atmosfer. Uap heksana bisa menjadi eksplosif dan heksana itu sendiri sangat mudah terbakar. Hexane adalah pelarut non-polar, dan digunakan sebagai pelarut di laboratorium.
Tidak hanya heksana murni digunakan sebagai pelarut, tetapi ada berbagai jenis pelarut yang dibuat menggunakan heksana. Selain itu, heksana digunakan untuk membuat produk kulit, lem, untuk pembuatan tekstil, produk pembersih, dll. Heksana digunakan untuk mengekstraksi zat non-polar seperti minyak dan minyak saat menganalisis air dan tanah.
Apa itu n-heksana?
n -heksana atau heksana normal adalah struktur heksana yang tidak bercabang dengan rumus molekul C6H14. Titik mendidih N-heksana adalah 68.7 HaiC, sedangkan titik leleh adalah −95.3 HaiC. N-heksana digunakan dalam proses mengekstraksi minyak dari biji seperti safflower, kedelai dan kapas.
Apa perbedaan antara heksana dan n-heksana?
Heksana adalah campuran senyawa dengan rumus C6H14. Hexane memiliki struktur bercabang, sedangkan n-heksana adalah struktur heksana yang tidak bercabang. n-heksana adalah isomer struktural heksana. Selain itu, N-heksana memiliki titik didih yang lebih tinggi dibandingkan dengan heksan lainnya. Namun, secara keseluruhan, titik didih mereka jatuh dalam kisaran suhu yang kecil. Selain itu, N-heksana memiliki tekanan uap yang cukup besar pada suhu kamar.
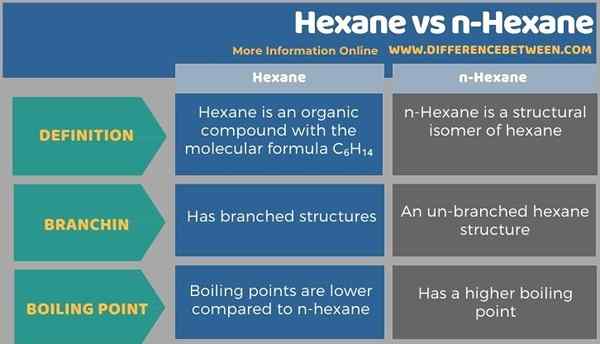
Ringkasan -Hexane vs N -Hexane
n-heksana adalah isomer struktural heksana. Perbedaan utama antara heksana dan n-heksana adalah bahwa heksana memiliki struktur bercabang, sedangkan n-heksana adalah struktur heksana yang tidak bercabang.
Gambar milik:
1. “CNX Chem 20 01 EX1 15 IMG” oleh OpenStax - (CC oleh 4.0) Via Commons Wikimedia


