Perbedaan antara titik isoelektrik dan isoionik
Perbedaan utama - isoelektrik vs isoionik Titik
Dua istilah titik isoelektrik dan titik isoionik menggambarkan konsep biokimia yang sama tentang asam amino; Titik isoelektrik atau titik isoionik adalah pH di mana muatan positif asam amino sama dengan muatan negatif dari asam amino yang sama. Jadi, ada tidak ada perbedaan Antara istilah titik isoelektrik dan titik isoionik.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa titik isoelektrik atau titik isoionik
3. Titik isoelektrik vs isoionik
4. Ringkasan
Apa titik isoelektrik atau titik isoionik?
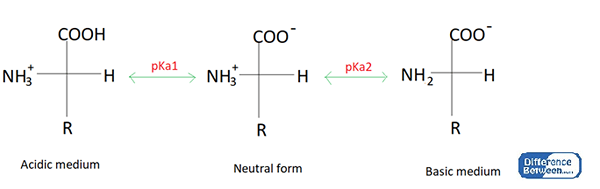
Titik isoelektrik atau titik isoionik asam amino adalah pH di mana muatan positif asam amino sama dengan muatan negatif dari asam amino yang sama. Itu dilambangkan dengan pi. Karena tidak ada muatan listrik bersih dalam asam amino, ia tidak dapat bermigrasi di medan listrik. Oleh karena itu, titik isoelektrik adalah titik di mana asam amino netral.
Pada titik isoelektrik, zwitterion terbentuk. Zwitterion adalah molekul dipolar yang memiliki lebih dari dua kelompok fungsional yang memiliki muatan positif dan negatif (kelompok fungsional bermuatan positif dan kelompok fungsional bermuatan negatif). Muatan positif pada kelompok fungsional harus sama dengan muatan negatif yang ada pada gugus fungsional asam amino. Ini membuat muatan listrik bersih dari Zwitterion Zero.

Gambar 01: Bentuk asam amino yang asam, basa dan netral
Pada titik isoionik, zwitterion adalah bentuk dominan dari asam amino. Nilai PI dapat diperoleh dengan menggunakan nilai PKA dari muatan positif bersih dan bentuk muatan negatif bersih dari asam amino dalam media asam dan basa.
- Jika tidak ada gugus fungsional yang diisi dalam rantai samping asam amino,
pi = ½ (pKa1 + PKA2) dimana pKa1 dan PKA2 adalah nilai PKA dari asam amino dalam media asam dan basa.
- Jika ada rantai samping asam, PI lebih rendah dari yang diharapkan.
- Jika ada rantai samping dasar, PI lebih tinggi dari yang diharapkan.
Apa perbedaan antara isoelektrik dan titik isoionik?
- Titik isoelektrik, juga dikenal sebagai titik isoionik, dari asam amino adalah pH di mana muatan positif asam amino sama dengan muatan negatif dari asam amino yang sama, yang dilambangkan dengan PI.
Ringkasan - Isoelektrik vs isoionik Titik
Tidak ada perbedaan antara istilah titik isoelektrik dan titik isoionik. Kedua istilah digunakan untuk memberi nama pH di mana tidak ada muatan listrik bersih dalam asam amino.
Referensi:
1. Berburu, Ian R. “Titik isoelektronik, pi." CH27: titik isoelektronik. Tersedia disini
2. “Titik isoionik.”Wikipedia, Wikimedia Foundation, 17 Feb. 2018. Tersedia disini
3. “Zwitterion.”Wikipedia, Wikimedia Foundation, 20 Mar. 2018. Tersedia disini


