Perbedaan antara isoelektronik dan isosteres
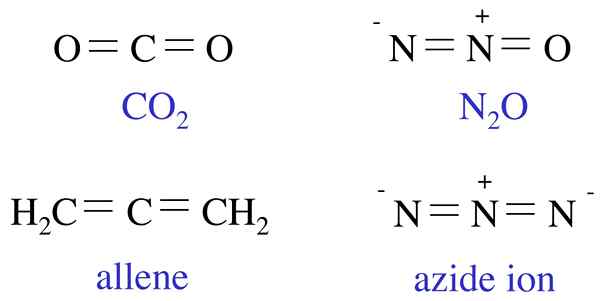
Itu perbedaan utama antara isoelektronik dan isosteres adalah bahwa Spesies kimia isoelektronik memiliki konfigurasi elektronik yang serupa sedangkan isosteres adalah spesies kimia yang memiliki ukuran yang sama, jumlah atom dan elektron valensi yang sama.
Awalan "iso" berarti bahwa dua atau lebih spesies kimia memiliki fitur karakteristik yang sama. Spesies isoelektronik dan isoster adalah dua jenis fitur seperti itu. Namun, kedua istilah ini berbeda satu sama lain, tergantung pada fitur yang dianggap dibandingkan antara dua atau lebih spesies kimia.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu isoelektronik
3. Apa itu isoster
4. Perbandingan berdampingan -isoelektronik vs isosteres dalam bentuk tabel
5. Ringkasan
Apa itu isoelektronik?
Istilah isoelektronik mengacu pada memiliki jumlah elektron yang sama atau konfigurasi elektronik yang sama. Spesies kimia yang kami pertimbangkan dalam konteks ini termasuk atom, ion atau molekul. Spesies kimia ini harus memiliki struktur elektronik yang sama dengan jumlah elektron valensi yang sama untuk menyebutkannya sebagai spesies isoelektronik. Dengan kata lain, istilah ini mengacu pada fitur "elektrik yang sama" atau "muatan yang sama". Biasanya, spesies kimia ini menunjukkan sifat kimia yang sama juga karena sifat kimia spesies kimia ditentukan oleh konfigurasi elektronik spesies kimia.
Saat mempertimbangkan beberapa contoh untuk spesies kimia isoelektronik, contoh umum adalah atom dan ion Li+ (lithium kation) di mana kedua spesies kimia memiliki dua elektron dalam atom/ionnya. Demikian pula, K+ (kation kalium) dan Ca+ 2 (kation kalsium) adalah isoelektronik karena kedua kation ini memiliki konfigurasi elektronik [NE] 4S1. Selain atom/ion, kami juga dapat memberikan beberapa contoh untuk molekul yang saling isoelektronik satu sama lain, termasuk molekul karbon monoksida dan molekul gas nitrogen.
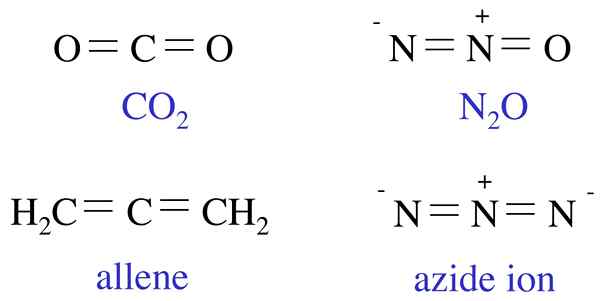
Gambar 01: Contoh molekul isoelektronik
Konsep sifat isoelektronik spesies kimia berguna dalam memprediksi sifat dan reaksi spesies kimia. Kami dapat menggunakan fitur ini untuk mengidentifikasi atom yang mirip dengan hidrogen yang memiliki satu elektron valensi dan karenanya isoelektronik untuk hidrogen. Selain itu, kita dapat menerapkan konsep ini untuk mengidentifikasi senyawa yang tidak diketahui atau langka tergantung pada kemiripan elektroniknya dengan spesies kimia yang diketahui/umum.
Apa itu isoster?
Istilah Isostere mengacu pada spesies kimia yang memiliki ukuran yang sama, jumlah atom yang sama dan jumlah elektron valensi yang sama. Spesies kimia yang kami pertimbangkan dalam konteks ini adalah molekul atau ion. Misalnya, benzena dan tiofena adalah molekul isosterik. Secara umum, molekul isosterik memiliki bentuk yang sama karena pengaturan elektron yang identik. Seringkali, spesies kimia ini memiliki sifat elektronik yang serupa juga. Konsep Isosteres pertama kali dikembangkan oleh Irving Langmuir pada tahun 1919. Kemudian, itu dimodifikasi oleh Grimm.
Apa perbedaan antara isoelektronik dan isosteres?
Perbedaan utama antara isoelektronik dan isosteres adalah bahwa spesies kimia isoelektronik memiliki konfigurasi elektronik yang sama sedangkan isosteres adalah spesies kimia yang memiliki ukuran yang sama, jumlah atom dan elektron valensi yang sama. Selain itu, atom, ion atau molekul yang menggambarkan isoelektronik sedangkan isoster menggambarkan ion atau molekul. Misalnya, gas karbon monoksida dan gas nitrogen adalah isoelektronik satu sama lain sementara benzena dan tiofena adalah isosteres.
Infografis berikut merangkum perbedaan antara isoelektronik dan isosteres dalam bentuk tabel untuk perbandingan berdampingan.
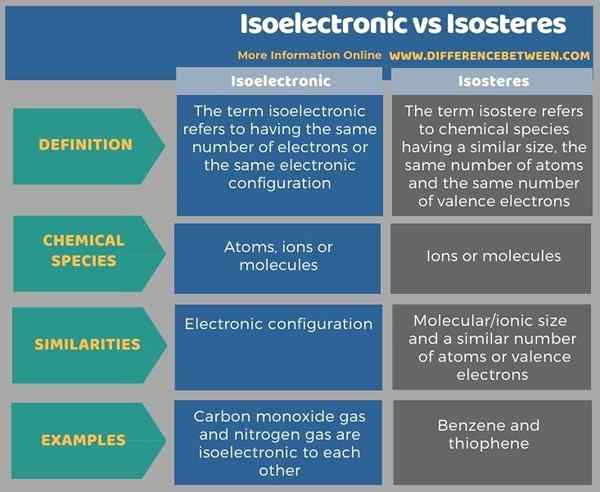
Ringkasan -Isoelectronic VS Isosteres
Istilah isoelektronik berbeda dari istilah isosteres karena mereka menggambarkan dua fitur spesies kimia yang berbeda. Perbedaan utama antara isoelektronik dan isosteres adalah bahwa spesies kimia isoelektronik memiliki konfigurasi elektronik yang sama sedangkan isosteres adalah spesies kimia yang memiliki ukuran yang sama, jumlah atom dan elektron valensi yang sama.
Referensi:
1. Helmenstine, Anne Marie. “Definisi isoelektronik."Thoughtco, Aug. 28, 2020, tersedia di sini.
Gambar milik:
1. “Molekul Isoelektronik” oleh Tem5psu - Karya Sendiri (CC BY -SA 3.0) Via Commons Wikimedia


