Perbedaan antara oksigen dan ozon

Itu perbedaan utama antara oksigen dan ozon adalah bahwa Oksigen adalah molekul gas diatomik dari unsur oksigen, sedangkan ozon adalah molekul triatomik oksigen.
Gas oksigen dan ozon adalah alotrop elemen oksigen yang paling akrab. Oksigen adalah gas yang sangat penting untuk organisme hidup; untuk respirasi mereka. Ozon juga melindungi kehidupan di bumi saat berada di atmosfer atas, tetapi di atmosfer yang lebih rendah, berbahaya.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu oksigen
3. Apa itu ozon
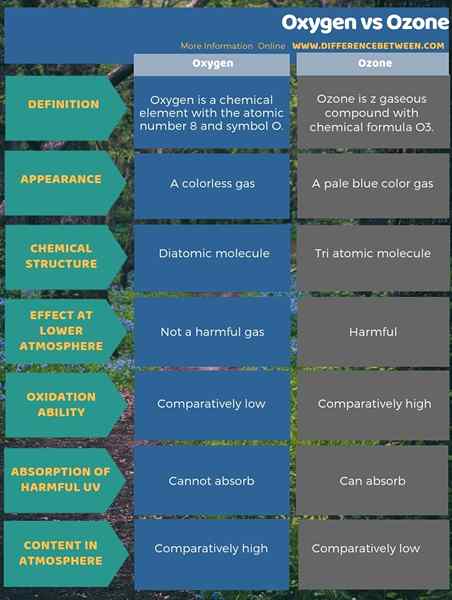
4. Perbandingan berdampingan - oksigen vs ozon dalam bentuk tabel
5. Ringkasan
Apa itu oksigen?
Oksigen adalah elemen kimia dengan nomor atom 8, yang ada di kelompok 16 dari tabel periodik. Ini memiliki konfigurasi elektron 1s2 2s2 2p4. Oksigen memiliki tiga isotop utama; 16HAI, 17HAI, 18HAI. Diantaranya, 16O adalah isotop yang paling berlimpah. Selain itu, atom oksigen memiliki delapan elektron, dan dapat memperoleh dua elektron lagi dari atom lain untuk membentuk anion bermuatan -2. Atau, dua atom oksigen dapat berbagi empat elektron untuk membentuk ikatan kovalen yang memberikan molekul diatomik (O2).
Berat molekul O2 adalah 32 g mol-1. Ini adalah gas yang tidak berwarna, tidak berbau, dan tidak berasa. Ada sekitar 21% oksigen di atmosfer bumi. Selanjutnya, tidak larut dalam air dan sedikit lebih berat dari udara. Oksigen memiliki sifat magnetik juga. Saat gas oksigen mengembun pada -183 ° C, itu menjadi cairan warna kebiruan.

Gambar 01: Untuk keperluan pengelasan, kita membutuhkan oksigen untuk menghasilkan api oksi-asetilena
Juga, gas ini bereaksi dengan semua elemen untuk membentuk oksida kecuali gas inert. Oleh karena itu, ini adalah agen pengoksidasi yang baik. Oksigen sangat penting dalam respirasi organisme hidup. Kami menggunakan gas ini di rumah sakit, pengelasan, dan di banyak industri lain.
Apa itu ozon?
Bentuk oksigen tiga atom adalah ozon, dan itu adalah bentuk oksigen yang umum. Segera setelah kami mendengar nama ozon, kami memikirkan lapisan ozon. Lapisan ozon hadir di stratosfer pada tingkat atmosfer yang lebih tinggi, dan menyerap radiasi UV yang berbahaya, sehingga membatasinya untuk sampai ke permukaan bumi.
Namun, ozon berbahaya pada tingkat atmosfer yang lebih rendah. Itu bertindak sebagai polutan udara (bertanggung jawab untuk kabut asap fotokimia) dan dapat menyebabkan penyakit pernapasan bagi manusia dan hewan. Selain itu, itu merusak tanaman juga. Ozon kurang stabil daripada gas oksigen, karenanya; pecah menjadi gas oksigen yang lebih stabil.
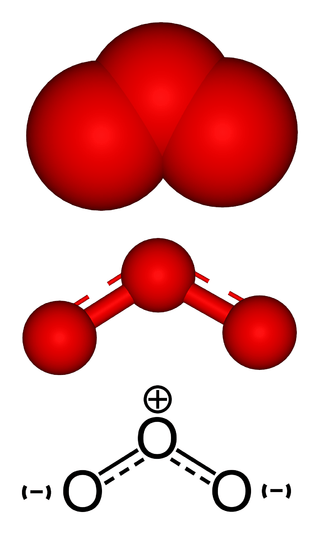
Gambar 02: Struktur hibrida molekul gas ozon
Gas ozon adalah gas warna biru pucat dengan bau yang tajam. Lebih larut dalam pelarut non-polar dan kurang larut dalam air. Selain itu, dua atom oksigen dalam ozon mengikat bersama dengan ikatan rangkap, dan ada ikatan datif antara satu atom oksigen dengan atom oksigen lain.
Namun, ini menunjukkan stabilisasi resonansi; Dengan demikian, struktur aktual molekul ini adalah struktur hibrida. Di sana, panjang ikatan O-O serupa antara tiga atom. Atom oksigen pusat memiliki SP2 hibridisasi dengan satu pasangan tunggal. Selain itu, ozon memiliki geometri yang bengkok. Juga, ini adalah molekul kutub. Dan, karena itu adalah agen pengoksidasi yang kuat, ozon sangat reaktif. Selain itu, gas ini terbentuk dari oksigen saat ada sinar matahari.
Apa perbedaan antara oksigen dan ozon?
Oksigen adalah elemen kimia dengan nomor atom 8 dan simbol O dan ozon adalah senyawa gas dengan formula kimia O3. Secara umum, ketika kita mengatakan oksigen, kita merujuk pada gas oksigen. Oleh karena itu, perbedaan utama antara oksigen dan ozon adalah bahwa gas oksigen adalah molekul gas diatomik dari elemen oksigen, sedangkan ozon adalah molekul gas triatomik oksigen. Selain itu, ada perbedaan antara oksigen dan ozon dalam warnanya juga. Itu adalah; Oksigen adalah gas yang tidak berwarna, tetapi ozon adalah gas biru pucat.
Selain itu, perbedaan signifikan lainnya antara oksigen dan ozon adalah bahwa gas ozon dapat berbahaya pada tingkat atmosfer yang lebih rendah tetapi, oksigen bukanlah gas berbahaya. Selain itu, di atmosfer, gas oksigen terjadi dalam jumlah yang jauh lebih tinggi daripada ozon. Selain itu, ozon kurang stabil daripada oksigen. Oleh karena itu, kemampuan oksidasi ozon lebih tinggi dari oksigen.
Infografis di bawah ini tentang perbedaan antara oksigen dan ozon menunjukkan perbedaan dalam bentuk tabel.
Ringkasan -oksigen vs ozon
Oksigen dan ozon adalah dua senyawa gas utama dari oksigen elemen kimia. Perbedaan utama antara oksigen dan ozon adalah bahwa oksigen adalah molekul gas diatomik elemen oksigen, sedangkan ozon adalah molekul triatomik oksigen.
Referensi:
1. "Ozon."Informasi Nasional untuk Informasi Bioteknologi. Database senyawa pubchem, u.S. Perpustakaan Kedokteran Nasional. Tersedia disini
2. "Oksigen."Informasi Nasional untuk Informasi Bioteknologi. Database senyawa pubchem, u.S. Perpustakaan Kedokteran Nasional. Tersedia disini
Gambar milik:
1.”Gmaw.pengelasan.af.NCS ”oleh William M. Piring jr. (Domain publik) via commons wikimedia
2."Ozon-Montage" (domain publik) melalui Commons Wikimedia