Perbedaan antara protonasi dan ionisasi
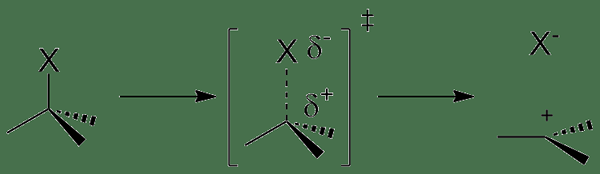
Itu perbedaan utama antara protonasi dan ionisasi adalah itu Protonasi adalah penambahan proton ke spesies kimia, sedangkan ionisasi adalah penghapusan atau mendapatkan elektron dari spesies kimia.
Protonasi dan ionisasi adalah dua konsep kimia yang penting dalam menggambarkan perilaku ionik spesies kimia.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu protonasi
3. Apa itu ionisasi
4. Perbandingan berdampingan - protonasi vs ionisasi dalam bentuk tabel
5. Ringkasan
Apa itu protonasi?
Protonasi adalah penambahan proton ke spesies kimia seperti atom, molekul, atau ion. Ini membentuk asam konjugat dari spesies kimia yang sesuai. Protonasi dapat digambarkan sebagai reaksi kimia mendasar, dan ini merupakan langkah penting dalam banyak proses stoikiometri dan katalitik.
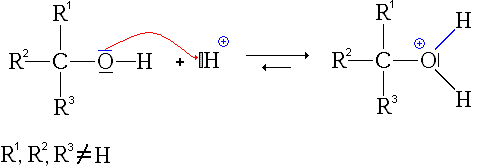
Gambar 01: Reaksi Protonasi
Ada dua jenis proses protonasi yang dikenal sebagai protonasi monobasik dan protonasi polibasic. Protonasi monobasic adalah protonasi tunggal yang terjadi di beberapa ion dan molekul. Tetapi dalam beberapa ion dan molekul, mungkin ada lebih dari satu protonasi, dan kita dapat menyebutkannya sebagai spesies kimia polibasic. Sifat polibasic ini benar bagi banyak makromolekul biologis.
Apa itu ionisasi?
Ionisasi adalah proses kimia di mana atom atau molekul mendapatkan muatan positif atau negatif. Proses ini terjadi karena masing -masing menghilangkan atau mendapatkan elektron dari atom atau molekul. Dalam proses ionisasi, kita dapat menyebutkan ion yang dihasilkan sebagai anion dan kation, tergantung pada muatan yang mereka miliki, saya.e. kation adalah ion dan anion yang bermuatan positif adalah ion yang bermuatan negatif. Pada dasarnya, hilangnya elektron dari atom netral atau molekul membentuk kation, dan gain elektron dari atom netral memberikan muatan negatif, membentuk anion.
Saat elektron dikeluarkan dari atom gas netral dengan penambahan energi, ia membentuk kation monovalen. Ini karena atom netral memiliki jumlah elektron dan proton yang sama, menghasilkan tidak ada muatan bersih; Saat kita menghapus elektron dari atom itu, ada satu proton berlebih yang tidak memiliki elektron untuk menetralisir muatannya. Oleh karena itu, atom itu mendapat muatan +1 (itu adalah muatan proton). Jumlah energi yang dibutuhkan untuk ini adalah energi ionisasi pertama dari atom itu.
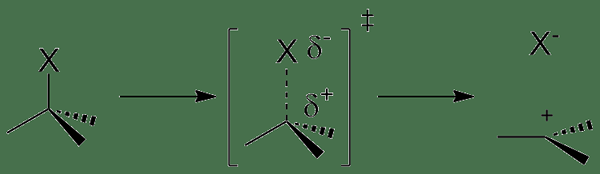
Gambar 02: Reaksi ionisasi
Selain itu, ionisasi yang terjadi dalam larutan cair adalah pembentukan ion dalam larutan. Misalnya, ketika molekul HCl larut dalam air, ion hidronium (H3O+) terbentuk. Di sini, HCL bereaksi dengan molekul air dan membentuk ion hidronium bermuatan positif dan klorida bermuatan negatif (CL-) ion.
Selanjutnya, ionisasi dapat terjadi melalui tabrakan. Tetapi jenis ionisasi ini terjadi terutama pada gas ketika arus listrik melewati gas. Jika elektron dalam arus memiliki jumlah energi yang cukup yang diperlukan untuk menghilangkan elektron dari molekul gas, mereka akan memaksa keluar elektron dari molekul gas, menghasilkan pasangan ion yang terdiri dari ion positif individu dan elektron negatif negatif. Di sini, ion negatif juga terbentuk karena beberapa elektron cenderung menempel pada molekul gas daripada menarik elektron keluar.
Selain itu, ionisasi terjadi ketika energi radiasi atau partikel bermuatan yang cukup energik melewati padatan, cairan atau gas; Misalnya, partikel alfa, partikel beta, dan radiasi gamma dapat mengionisasi zat; Karena itu, kami menamai mereka radiasi pengion.
Apa perbedaan antara protonasi dan ionisasi?
Protonasi dan ionisasi adalah konsep kimia penting dalam kimia. Perbedaan utama antara protonasi dan ionisasi adalah bahwa protonasi adalah penambahan proton ke spesies kimia, sedangkan ionisasi adalah penghapusan atau mendapatkan elektron dari spesies kimia.
Infografis di bawah ini merangkum perbedaan antara protonasi dan ionisasi dalam bentuk tabel.
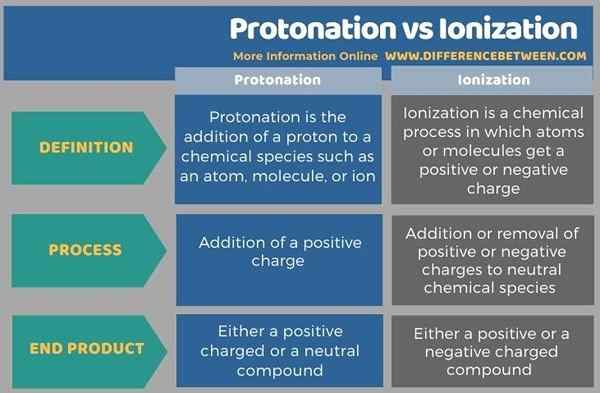
Ringkasan -Protonasi vs ionisasi
Protonasi dan ionisasi saling berlawanan karena protonasi mengacu pada penambahan sementara ionisasi sebagian besar mengacu pada pemecahan ikatan. Perbedaan utama antara protonasi dan ionisasi adalah bahwa protonasi adalah penambahan proton ke spesies kimia, sedangkan ionisasi adalah penghapusan atau mendapatkan elektron dari spesies kimia.
Referensi:
1. "Ionisasi." Encyclopædia Britannica, Encyclopædia Britannica, Inc., Tersedia disini.
Gambar milik:
1. "Protonation d'un alcool Tertiaire" oleh pengunggah asli adalah Rhadamante di Wikipedia Prancis. - Ditransfer dari fr.Wikipedia ke Commons oleh Bloody-Libu Menggunakan CommonShelper. (CC BY-SA 3.0) Via Commons Wikimedia
2. “Reaksi Ionisasi” oleh CSEIZERT - Karya Sendiri (CC BY -SA 3.0) Via Commons Wikimedia


