Perbedaan antara ruthenium dan rhodium

Itu perbedaan utama antara ruthenium dan rhodium adalah itu Ruthenium mengandung tujuh elektron di cangkang elektron D paling terluar sedangkan rhodium mengandung delapan elektron di cangkang elektron D terluar.
Baik rutenium dan rhodium adalah elemen kimia dalam periode 5 tabel periodik. Tetapi mereka memiliki angka atom yang berbeda; Oleh karena itu, elemen kimia ini memiliki sifat kimia dan fisik yang berbeda seperti yang dijelaskan di bawah ini.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu Ruthenium
3. Apa itu Rhodium
4. Perbandingan berdampingan - ruthenium vs rhodium dalam bentuk tabel
5. Ringkasan
Apa itu Ruthenium?
Ruthenium adalah elemen kimia yang memiliki nomor atom 44. Simbol kimia untuk ruthenium adalah RU, dan ini adalah logam transisi yang langka. Kita dapat menemukan ruthenium di kelompok 8 dan periode 5 dari tabel elemen periodik. Oleh karena itu, ini adalah elemen blok D, dan konfigurasi elektronik elemen ini adalah [kr] 4d75S1. Pada suhu dan tekanan kamar, elemen kimia ini terjadi dalam keadaan padat dan memiliki titik leleh yang sangat tinggi (sekitar 2.300 Celcius) dan titik didih yang sangat tinggi (sekitar 4400 Celcius). Keadaan oksidasi rutenium yang paling umum dan stabil adalah +3 dan +4. Itu dapat membentuk oksida asam ringan.

Ruthenium secara alami terjadi dalam keadaan purba. Zat padat ini muncul sebagai logam putih keras polivalen. Struktur kristal dari rutenium padat adalah struktur heksagonal yang ditutup. Selain itu, Ruthenium mengandung elektron yang tidak berpasangan, yang membuatnya paramagnetik. Selain itu, ruthenium hanya memiliki satu elektron di cangkang elektron terluar sedangkan semua elemen grup 8 lainnya mengandung dua elektron. Ini adalah fitur unik ruthenium.
Apa itu Rhodium?
Rhodium adalah elemen kimia yang memiliki nomor atom 45. Simbol kimia elemen ini adalah RH. Ini adalah logam transisi langka yang ada di kelompok 9 dan periode 5 dari tabel elemen periodik. Rhodium muncul sebagai logam putih keperakan. Ini adalah logam keras yang tahan korosi dan inert secara kimia. Oleh karena itu, kita dapat mengklasifikasikannya sebagai logam mulia. Hanya ada satu isotop rhodium yang terjadi secara alami (RH-103). Kita dapat menemukan logam ini secara alami sebagai logam gratis karena sifatnya yang lembam. Terkadang itu terjadi sebagai paduan dengan logam yang sama, dan jarang terjadi sebagai senyawa kimia dalam mineral. E.G. Bowieite. Keadaan oksidasi rhodium yang paling umum adalah +3. Itu dapat membentuk oksida amfoterik.
Saat mempertimbangkan kejadian alami rhodium, itu adalah primordial, dan dalam keadaan padatnya, rhodium memiliki struktur kristal kubik yang berpusat pada wajah. Logam ini paramagnetik karena memiliki elektron yang tidak berpasangan. Titik lebur dan titik didih sangat tinggi (masing -masing sekitar tahun 1900 dan 3600 Celcius).
Rhodium adalah logam keras yang memiliki reflektansi tinggi. Biasanya, itu tidak membentuk oksida bahkan setelah pemanasan. Itu dapat menyerap oksigen hanya pada titik membiarkan logam. Setelah pemadatan, oksigen yang diserap ini benar -benar dilepaskan. Kebanyakan asam tidak dapat menyerang logam rhodium. E.G. tidak larut dalam asam nitrat.
Apa perbedaan antara ruthenium dan rhodium?
Ruthenium adalah elemen kimia yang memiliki nomor atom 44 sedangkan rhodium adalah elemen kimia yang memiliki nomor atom 45. Keduanya adalah elemen periode 5. Perbedaan utama antara ruthenium dan rhodium adalah bahwa ruthenium mengandung tujuh elektron di cangkang elektron D terluar sedangkan rhodium mengandung delapan elektron di cangkang elektron D terluar paling.
Tabel di bawah ini menyajikan perbandingan terperinci dari kedua elemen untuk membedakan perbedaan antara ruthenium dan rhodium.
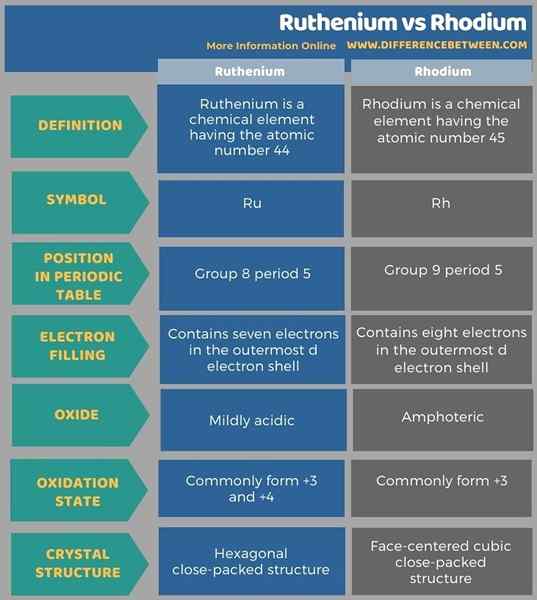
Ringkasan -Ruthenium vs Rhodium
Baik ruthenium dan rhodium berada dalam periode yang sama dalam tabel elemen periodik, tetapi mereka berada dalam kelompok yang berbeda karena mereka memiliki angka atom yang berbeda. Perbedaan utama antara ruthenium dan rhodium adalah bahwa ruthenium mengandung tujuh elektron di cangkang elektron D terluar sedangkan rhodium mengandung delapan elektron di cangkang elektron D terluar paling.
Referensi:
1. Pedersen, Traci. “Fakta tentang Rhodium." LiveScience, Beli, 13 Mar. 2018, tersedia di sini.
Gambar milik:
1. "Ruthenium A Half Bar" oleh Alchemist-HP (Talk) (www.PSE-Mendelejew.de) - pekerjaan sendiri, fal) via commons wikimedia
2. "Rhodium Powder Pressed Melted" oleh Alchemist-HP (Talk) www.PSE-Mendelejew.Pekerjaan Dederivatif: Purpy Pupple (Talk) - Pekerjaan Sendiri (CC BY -SA 3.0 de) via commons wikimedia


