Perbedaan antara natrium klorit dan natrium hipoklorit

Perbedaan utama - natrium klorit vs natrium hipoklorit
Natrium klorit dan natrium hipoklorit adalah garam natrium umum yang digunakan dalam industri. Kedua senyawa ini sangat penting karena agen pemutihan dan desinfektan. Tetapi mereka sangat berbeda satu sama lain ketika sifat kimianya seperti massa molar dan sifat fisik dipertimbangkan. Natrium klorit terutama digunakan dalam pembuatan kertas dan sebagai desinfektan. Sodium hipoklorit digunakan sebagai desinfektan dengan melarutkannya dalam air untuk membentuk "pemutih cair". Perbedaan utama antara natrium klorit dan natrium hipoklorit adalah bahwa Sodium klorit mengandung atom klorin yang memiliki +3 keadaan oksidasi Sedangkan natrium hipoklorit mengandung atom klor yang memiliki keadaan oksidasi +1.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu natrium klorit
3. Apa itu natrium hipoklorit
4. Kesamaan antara natrium klorit dan natrium hipoklorit
5. Perbandingan berdampingan - natrium klorit vs natrium hipoklorit dalam bentuk tabel
6. Ringkasan
Apa itu natrium klorit?
Sodium Klorit adalah senyawa kimia anorganik yang memiliki formula kimia Naclo2. Massa molar senyawa ini adalah 90.438 g/mol saat anhidrat. Ada bentuk hidrat juga (terdiri dari tiga molekul air yang terkait dengan molekul natrium klorit yang massa molarnya 144.48 g/mol). Senyawa ini juga disebut asam chlorous. Ini adalah senyawa ionik yang mengandung kation natrium (NA+) dan anion klorit (clo2-).

Gambar 1: Botol yang diisi dengan natrium klorit
Ini tersedia sebagai bubuk kristal putih yang tidak berbau. Pembakaran natrium klorit sulit, tetapi dapat mempercepat pembakaran senyawa organik. Oleh karena itu, natrium klorit dapat digunakan untuk membuat campuran eksplosif dengan bahan yang mudah terbakar. Sodium klorit terurai sekitar 180-200◦C.
Sodium klorit kurang larut dalam air tetapi lebih larut dalam metanol dan etanol. Struktur kristal senyawa adalah monoklinik. Natrium klorit terutama digunakan dalam pembuatan kertas dan juga sebagai desinfektan. Ini adalah agen pengoksidasi yang baik; Karenanya digunakan untuk memutihkan berbagai jenis bahan seperti kayu, minyak, dll.
Asam chlorous bebas (HCLO2) sangat tidak stabil dan tidak memiliki pentingnya dalam industri. Tetapi garam natrium asam ini sangat stabil dan juga murah. Sebagian besar waktu, natrium klorit berasal dari natrium klorat, yang memiliki formula kimia naclo3. Proses produksi adalah metode tidak langsung di mana klorin dioksida (clo2) diproduksi pada awalnya. Klorin dioksida sangat eksplosif dan dibuat dengan mengurangi natrium klorat dalam asam kuat dengan adanya zat pereduksi seperti natrium sulfit. Klorin dioksida yang diproduksi kemudian diserap ke larutan alkali bersama dengan reduksi oleh hidrogen peroksida (H2HAI2). Ini menghasilkan natrium klorit.
Apa itu natrium hipoklorit?
Sodium hipoklorit adalah senyawa anorganik yang memiliki formula kimia Naclo. Rasio atom antara natrium, klorin dan oksigen adalah 1: 1: 1. Senyawa ini terdiri dari kation natrium yang terikat pada anion hipoklorit. Oleh karena itu adalah garam natrium asam hipoklor. Saat natrium hipoklorit dilarutkan dalam air, ia dikenal sebagai pemutih cair karena sifat pemutihannya.
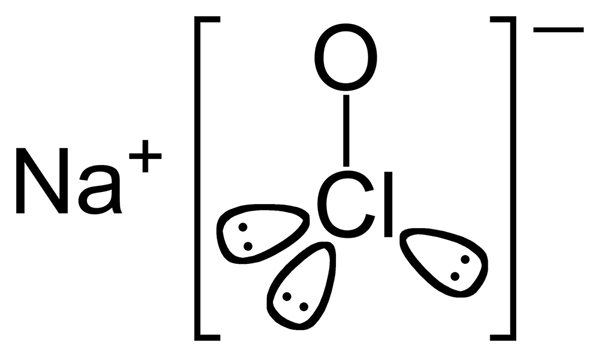
Gambar 2: Struktur kimia natrium hipoklorit
Massa molar natrium hipoklorit adalah 74.44 g/mol. Penampilan senyawa ini dapat digambarkan sebagai padatan kuning kehijauan. Itu juga memiliki bau manis. Titik lebur natrium hipoklorit adalah 18 ° C dan titik didih adalah 101◦C.
Sodium hipoklorit terutama digunakan sebagai desinfektan dan sebagai zat pemutih. Hampir semua cairan pemutih yang kami gunakan dalam rumah tangga mengandung sekitar 3-8% natrium hipoklorit. Senyawa ini memiliki sifat de-pewarnaan; Oleh karena itu digunakan untuk menghilangkan noda cetakan, noda gigi, dll. Sodium hipoklorit adalah desinfektan yang baik karena memiliki berbagai aktivitas anti-mikroba yang luas.
Produksi natrium hipoklorit dilakukan melalui proses pelacur. Ini adalah metode industri skala besar. Di sini, natrium hipoklorit diproduksi dengan melewati gas klorin ke dalam larutan natrium hidroksida yang dingin dan encer. Produk lain yang diberikan dengan metode ini adalah natrium klorida (NaCl).
Apa kesamaan antara natrium klorit dan natrium hipoklorit?
- Natrium klorit dan natrium hipoklorit terdiri dari atom Na, CL dan O.
- Keduanya adalah desinfektan yang bagus.
Apa perbedaan antara natrium klorit dan natrium hipoklorit?
Natrium klorit vs natrium hipoklorit | |
| Sodium Klorit adalah senyawa kimia anorganik yang memiliki formula kimia Naclo2. | Sodium hipoklorit adalah senyawa anorganik yang memiliki formula kimia Naclo. |
| Atomisitas | |
| Natrium klorit memiliki satu atom natrium, satu atom klor dan dua atom oksigen. | Natrium hipoklorit memiliki satu atom natrium, atom klorin dan atom oksigen. |
| Keadaan oksidasi klorin | |
| Keadaan oksidasi klorin dalam natrium klorit adalah +3. | Keadaan oksidasi klorin dalam natrium hipoklorit adalah +1. |
| Penampilan | |
| Natrium klorit adalah bubuk kristal putih. | Natrium hipoklorit adalah padatan kuning kehijauan. |
| Bau | |
| Natrium klorit tidak berbau. | Natrium hipoklorit memiliki bau manis. |
| Masa molar | |
| Massa molar natrium klorit adalah 90.438 g/mol. | Massa molar natrium hipoklorit adalah 74.44 g/mol. |
| Titik lebur dan titik didih | |
| Sodium klorit terurai sekitar 180-200◦C. | Titik lebur adalah 18◦C dan titik didih adalah 101◦C. |
| Senyawa induk | |
| Natrium klorit adalah garam natrium asam chlorous. | Natrium hipoklorit adalah garam natrium asam hipoklor. |
| Produksi | |
| Natrium klorit diproduksi secara tidak langsung dari natrium klorat. | Sodium hipoklorit diproduksi dari proses hooker. |
Ringkasan -natrium klorit vs natrium hipoklorit
Natrium klorit adalah naclo2 dan natrium hipoklorit adalah naclo. Perbedaan utama antara natrium klorit dan natrium hipoklorit adalah bahwa natrium klorit mengandung atom klorin yang memiliki keadaan oksidasi +3 sedangkan natrium hipoklorit mengandung atom klorin yang memiliki keadaan oksidasi +1 oksidasi +1.
Referensi:
1. “Sodium hipoklorit."Informasi Nasional untuk Informasi Bioteknologi. Database senyawa pubchem, u.S. Perpustakaan Kedokteran Nasional, tersedia di sini.
2. Croswell, Jonathan. “Apa itu natrium klorit?”Livestrong.Com, grup daun, 3 Okt. 2017, tersedia di sini.
3. “Sodium hipoklorit.”Wikipedia, Wikimedia Foundation, 17 Feb. 2018, tersedia di sini.
Gambar milik:
1. "Sodium Klorit 450g" oleh W. Oelen -(CC BY -SA 3.0) Via Commons Wikimedia
2. “Sodium-Hypochlorite” oleh Benjah-BMM27-Karya Sendiri (Domain Publik) Via Commons Wikimedia


