Perbedaan antara valensi dan elektron valensi
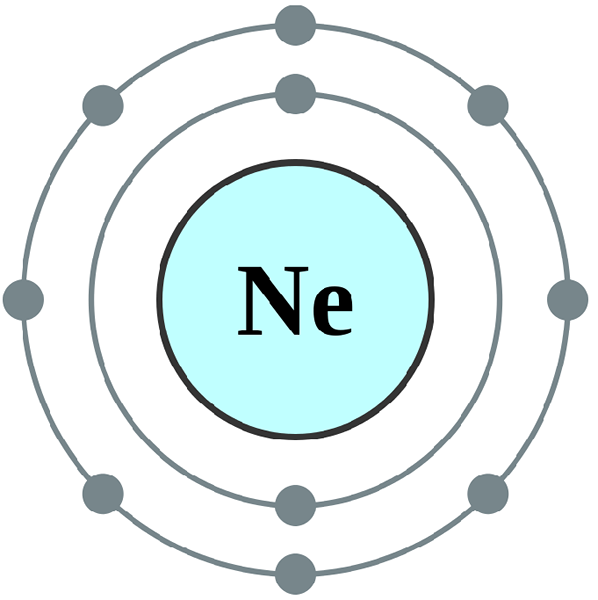
Perbedaan utama - elektron valensi vs valensi
Elektron valensi dan elektron valensi adalah istilah yang saling terkait, dan perbedaan utama Antara valensi dan elektron valensi paling baik dijelaskan dalam definisi mereka; elektron valensi adalah elektron di kulit terluar elemen sedangkan elektron valensi adalah jumlah elektron yang harus diterima atau dilepas untuk mencapai konfigurasi gas mulia terdekat. Itu adalah elektron dalam cangkang terluar yang biasanya berkontribusi untuk membentuk ikatan kimia. Dalam beberapa atom, jumlah elektron valensi sama dengan jumlah elektron valensi.
Apa itu vElektron Alence?
Jumlah elektron dalam cangkang terluar dari sebuah atom disebut "elektron valensi". Karena alasan ini, cangkang terluar dari sebuah atom disebut "cangkang valensi". Sebagian besar waktu, ini adalah elektron, yang mengambil bagian dalam ikatan kimia. Saat elemen membentuk kation, mereka menghilangkan elektron dari shell valensi. Jumlah elektron valensi dalam suatu elemen menentukan kelompok dalam tabel periodik.
Apa itu elektron valensi?
Jumlah elektron yang diperlukan untuk mendapatkan atau kehilangan untuk mengisi cangkang terluar dari sebuah atom disebut "elektron valensi". Untuk atom tertentu, jumlah elektron valensi tergantung pada jumlah elektron valensi dalam atom. Untuk natrium, valensi sama dengan 1, karena menghilangkan elektron terakhir di cangkang terluar untuk mencapai struktur oktet dari gas mulia terdekat.
|
Apa perbedaan antara elektron valensi dan valensi?
Definisi elektron valensi dan valensi
Valence Electron: Elektron dalam cangkang terluar dari atom disebut "elektron valensi". Untuk elemen grup "S" dan "P", jumlah elektron valensi sama dengan nomor kelompok mereka.
Contoh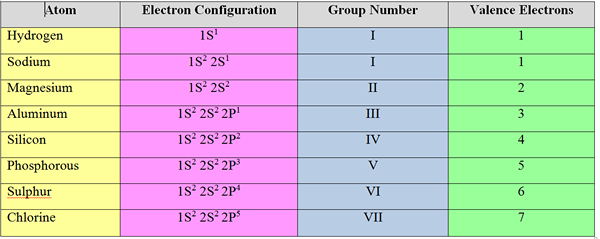
Elektron Valency: Jumlah elektron yang harus diterima atau dilepas untuk mencapai konfigurasi elektron gas mulia terdekat disebut "elektron valensi" atau "valensi" atom.
Secara umum, untuk elemen logam (elemen dalam kelompok I, II dan III), jumlah elektron valensi sama dengan jumlah elektron valensi; mereka menghilangkan elektron dalam cangkang valensi untuk mencapai struktur oktet.
Tapi, elemen non-logam menerima elektron untuk mencapai konfigurasi elektron gas mulia terdekat. Oleh karena itu, valensi elemen non-logam dihitung dengan mengurangi total elektron valensi dari 8.
Untuk klorin, jumlah elektron valensi = 8-7 = 1
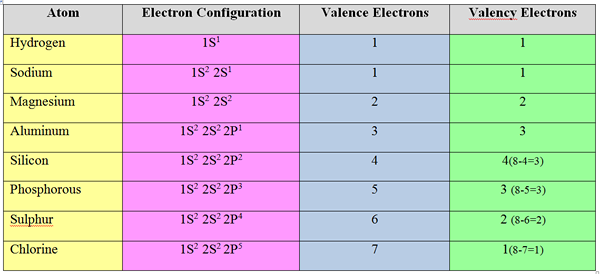
Karakteristik elektron valensi dan valensi
Elektron valensi dan valensi elektron grup VIII
Valence Electron: Elemen Grup VIII adalah gas mulia, dan mereka stabil secara kimiawi. Cangkang luarnya lengkap, dan mengandung delapan elektron di cangkang terluar (kecuali helium -He); Jadi elektron grup VIII memiliki delapan elektron valensi.
Elektron Valency: Valensi adalah ukuran kemampuan untuk membentuk ikatan dengan elemen atau molekul lain. Gas mulia tidak menerima atau menghilangkan elektron untuk mencapai aturan oktet karena mereka telah menyelesaikan cangkang terakhir. Oleh karena itu, valensi elemen grup VII sama dengan nol.
Gambar milik:
“Electron Shell 010 Neon - No Label” oleh Commons: Pengguna: Pumbaa (Pekerjaan Asli oleh Commons: Pengguna: Greg Robson) - http: // commons.Wikimedia.org/wiki/kategori: electron_shell_diagrams (versi berlabel yang sesuai).(CC BY-SA 2.0 uk) via commons

