Apa perbedaan antara polarisasi konsentrasi dan polarisasi kinetik
Itu Perbedaan utama antara polarisasi konsentrasi dan polarisasi kinetik adalah bahwa polarisasi konsentrasi berasal dari perubahan konsentrasi elektrolit, sedangkan polarisasi kinetik adalah perubahan dalam permitivitas statis.
Polarisasi konsentrasi dan polarisasi kinetik dapat digambarkan sebagai kontribusi terhadap potensi overspotensial suatu sistem. Dalam kedua ini, kelebihan potensi diperlukan untuk reaksi dan untuk transfer elektron melintasi interfase elektroda-elektrolit.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu polarisasi konsentrasi
3. Apa itu polarisasi kinetik
4. Polarisasi konsentrasi vs polarisasi kinetik dalam bentuk tabel
5. Ringkasan - Polarisasi Konsentrasi vs Polarisasi Kinetik
Apa itu polarisasi konsentrasi?
Polarisasi konsentrasi adalah bagian dari polarisasi sel elektrolitik yang dihasilkan dari perubahan konsentrasi elektrolit yang disebabkan oleh lewatnya arus melalui antarmuka elektroda/larutan. Kami menggunakan istilah ini di bidang seperti elektrokimia dan ilmu membran.
Dalam konteks ini, kita dapat memahami istilah polarisasi sebagai pergeseran perbedaan potensial elektrokimia di seluruh sel dari nilai keseimbangan yang kita peroleh untuk sistem ini. Oleh karena itu, istilah ini setara dengan potensi overpotensial konsentrasi.
Ketika ada spesies kimia yang berpartisipasi dalam reaksi elektroda elektrokimia yang memiliki pasokan pendek, kita dapat mengamati penurunan konsentrasi spesies ini di permukaan, yang juga menyebabkan difusi. Kita dapat menambahkan difusi ke transportasi migrasi ke permukaan untuk menjaga keseimbangan konsumsi dan untuk memberikan spesies.
Selain itu, kita dapat mengamati bahwa polarisasi konsentrasi mengarah pada peningkatan kebocoran garam melalui membran dan meningkatkan probabilitas skala/pengembangan pengotoran. Oleh karena itu, kita juga dapat mengamati bahwa selektivitas pemisahan dan masa pakai masa pakai membran memburuk.

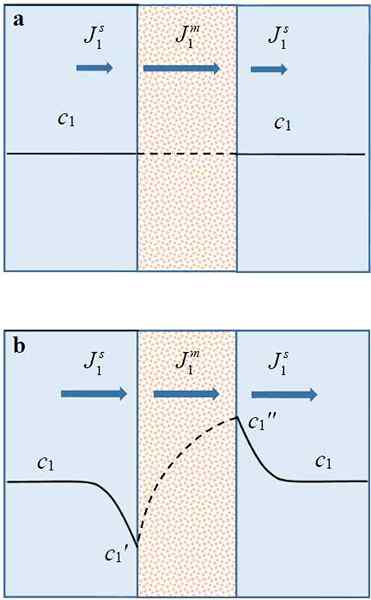
Gambar 01: Polarisasi Konsentrasi
Gambar 1 menunjukkan fluks dan profil konsentrasi dalam membran tertentu dengan larutan di sekitarnya. Gambar (a) menunjukkan penerapan kekuatan pendorong ke sistem pada keadaan awal keseimbangan. Di sini, fluks spesies selektif merembes di membran lebih besar dari fluks dalam larutan. Gambar (b) menunjukkan konsentrasi yang menimbulkan transportasi difusi yang pada gilirannya meningkatkan fluks total dalam larutan, mengurangi fluks dalam membran.
Apa itu polarisasi kinetik?
Polarisasi kinetik dapat digambarkan sebagai perubahan permitivitas statis dari solusi sehubungan dengan pelarut murni. Istilah penting mengenai polarisasi kinetik adalah defisiensi polarisasi kinetik, yang mengacu pada pengurangan permitivitas statis dari solusi dibandingkan dengan pelarut murni. Biasanya, penurunan faktor ini sebanding dengan produk waktu relaksasi dielektrik pelarut dan konduktivitas frekuensi rendah dari larutan.
Polarisasi kinetik adalah suatu kondisi di mana arus dibatasi oleh laju di mana elektron transfer antara permukaan elektroda dan reaktan dalam larutan.
Apa perbedaan antara polarisasi konsentrasi dan polarisasi kinetik?
Polarisasi konsentrasi dan polarisasi kinetik dapat digambarkan sebagai kontribusi terhadap potensi overspotensial suatu sistem. Perbedaan utama antara polarisasi konsentrasi dan polarisasi kinetik adalah bahwa polarisasi konsentrasi berasal dari perubahan dalam konsentrasi elektrolit, sedangkan polarisasi kinetik adalah perubahan permitivitas statis statis.
Ringkasan -Polarisasi Konsentrasi vs Polarisasi Kinetik
Polarisasi konsentrasi adalah bagian dari polarisasi sel elektrolitik yang dihasilkan dari perubahan konsentrasi elektrolit yang disebabkan oleh lewatnya arus melalui antarmuka elektroda/larutan. Polarisasi kinetik adalah perubahan permitivitas statis dari solusi sehubungan dengan pelarut murni tentang. Perbedaan utama antara polarisasi konsentrasi dan polarisasi kinetik adalah bahwa polarisasi konsentrasi adalah hasil dari perubahan konsentrasi elektrolit, sedangkan polarisasi kinetik adalah perubahan dalam permitivitas statis statis.
Referensi:
1. “Polarisasi konsentrasi." An Ikhtisar | Topik ScienceDirect.
2. “Polarisasi konsentrasi dalam proses yang digerakkan tekanan." Filtrasi synder.
Gambar milik:
1. “Polarisasi Konsentrasi Fig1” oleh ERAR1 - Karya Sendiri (CC BY -SA 3.0) Via Commons Wikimedia


