Apa perbedaan antara hukum gay-lussac dan hukum Avogadro
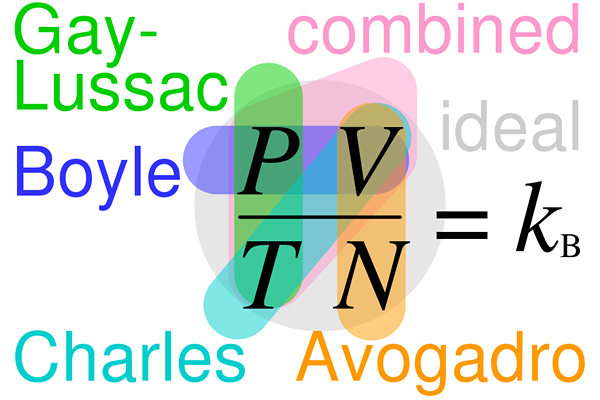
Itu Perbedaan utama antara hukum Gay-Lussac dan Hukum Avogadro adalah bahwa hukum gay-lussac menunjukkan bahwa volume gas berbanding lurus dengan suhu gas, sedangkan hukum Avogadro menyatakan bahwa volume gas berbanding lurus dengan jumlah molekul dalam gas.
Hukum Gay-Lussac menggambarkan berbagai tekanan massa gas tertentu secara langsung dengan suhu absolut gas pada volume konstan. Hukum Avogadro adalah undang -undang gas eksperimental yang menyatakan bahwa volume gas terkait dengan jumlah gas zat yang ada dalam sampel yang diberikan.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu Hukum Gay-Lussac
3. Apa itu Hukum Avogadro
4. Hukum Gay-Lussac vs Hukum Avogadro dalam bentuk tabel
5. Ringkasan -Hukum Gay -Lussac vs Hukum Avogadro
Apa itu Hukum Gay-Lussac?
Hukum Gay-Lussac menggambarkan berbagai tekanan massa gas tertentu secara langsung dengan suhu absolut gas pada volume konstan. Kadang -kadang dinamai Hukum Amonton. Kita dapat memberikan ekspresi matematika untuk undang -undang ini sebagai berikut:
P/t = k
Dalam persamaan ini, P mengacu pada tekanan, T mengacu pada suhu absolut, dan k adalah konstan. Kita dapat mengatakan bahwa ini adalah kasus khusus hukum gas ideal.
Turunan dari undang-undang ini adalah hukum suhu tekanan, yang menggambarkan hubungan antara tekanan dan suhu massa gas tertentu pada volume konstan.
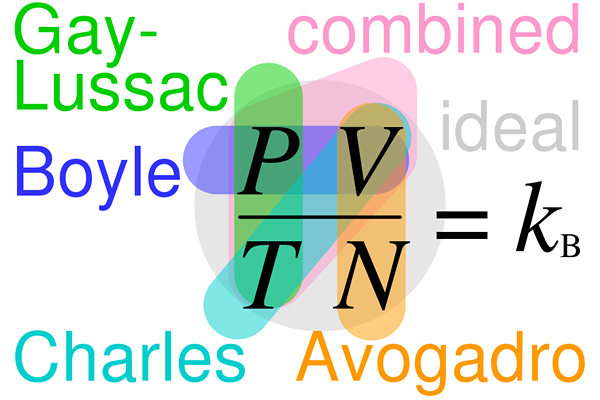
Menurut hukum menggabungkan volume, gas bereaksi satu sama lain dengan volume, dan mereka bereaksi dalam rasio bilangan bulat sederhana pada suhu konstan dan kondisi tekanan. Dengan kata lain, rasio antara volume gas reaktan dan produk gas dapat diberikan dalam bilangan bulat sederhana. Gay Lussac adalah salah satu ilmuwan pertama yang menemukan hubungan ini, yang menyebabkan derivasi hukum Avogadro.
Apa itu Hukum Avogadro?
Hukum Avogadro adalah undang -undang gas eksperimental yang menyatakan bahwa volume gas terkait dengan jumlah gas zat yang ada dalam sampel yang diberikan. Itu juga bernama Hipotesis Avogadro atau Prinsip Avogadro. Ini adalah bentuk khusus dari hukum gas ideal. Undang -undang ini dinamai Amedeo Avogadro pada tahun 1812.
Menurut deskripsi modern, hukum Avogadro menyatakan bahwa volume yang sama dari semua gas yang berada dalam kondisi suhu dan tekanan yang sama memiliki jumlah molekul yang sama. Sebagai contoh, volume gas hidrogen yang sama dan gas nitrogen terdiri dari jumlah atom yang sama ketika kedua gas ini berada dalam suhu dan tekanan yang sama. Secara praktis, gas nyata menunjukkan penyimpangan kecil dari perilaku gas ideal di mana hukum hanya memiliki kira -kira akurat. Namun, ini masih merupakan perkiraan penting bagi para ilmuwan. Secara matematis, hukum adalah sebagai berikut:
V/n = k
Di mana v adalah volume gas, n adalah jumlah zat gas dalam sampel, dan k adalah nilai konstan yang diberikan untuk suhu dan tekanan tertentu.
Perbedaan antara Hukum Gay-Lussac dan Hukum Avogadro
Hukum Gay-Lussac dan Hukum Avogadro adalah dua hukum gas penting. Perbedaan utama antara hukum gay-Lussac dan hukum Avogadro adalah bahwa hukum gay-Lussac menunjukkan bahwa volume gas berbanding lurus dengan suhu gas, sedangkan hukum Avogadro menyatakan bahwa volume gas berbanding lurus dengan angka tersebut molekul dalam gas.
Tabel berikut merangkum perbedaan antara hukum gay-lussac dan hukum Avogadro.
Ringkasan -Hukum Gay -Lussac vs Hukum Avogadro
Hukum Gay-Lussac dan Hukum Avogadro adalah dua hukum gas penting. Perbedaan utama antara hukum gay-Lussac dan hukum Avogadro adalah bahwa hukum gay-Lussac menunjukkan bahwa volume gas berbanding lurus dengan suhu gas, sedangkan hukum Avogadro menyatakan bahwa volume gas berbanding lurus dengan angka tersebut molekul dalam gas.
Referensi:
1. “Hukum Gay -Lussac - Pernyataan, Formula, Penjelasan Detail." Byjus, 25 Mar. 2021.
Gambar milik:
1. “Hubungan Hukum Gas Ideal” oleh CMGLEE - Karya Sendiri (CC BY -SA 4.0) Via Commons Wikimedia


