Apa perbedaan antara gugus fosforil dan kelompok fosfat
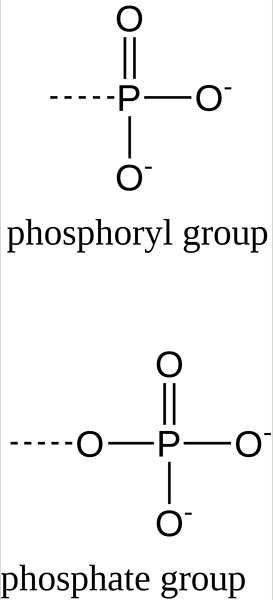
Itu Perbedaan utama antara gugus fosforil dan gugus fosfat adalah bahwa gugus fosforil mengandung satu atom fosfor yang terikat pada tiga atom oksigen dan muatan -2, sedangkan gugus fosfat mengandung satu atom fosfor yang terikat pada empat atom oksigen dan muatan -3.
Kelompok fosforil adalah ion kimia yang memiliki formula kimia P+HAI32- Sementara gugus fosfat adalah anion yang memiliki formula kimia PO4-3.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu kelompok fosforil
3. Apa itu kelompok fosfat
4. Kelompok fosforil vs gugus fosfat dalam bentuk tabel
5. Ringkasan -gugus fosforil vs gugus fosfat
Apa itu kelompok fosforil?
Kelompok fosforil adalah ion kimia yang memiliki formula kimia P+HAI32-. Oleh karena itu, ion ini mengandung atom fosfor dan oksigen. Itu bisa ada di negara protonasi yang berbeda. Istilah ini digunakan terutama untuk senyawa kimia yang terdiri dari gugus fosforil yang melekat pada atom lain, seperti senyawa fosforil klorida, yang mengandung gugus fosforil yang melekat pada anion klorida. Istilah ini juga berguna dalam menggambarkan mekanisme katalitik seperti fosforilasi.
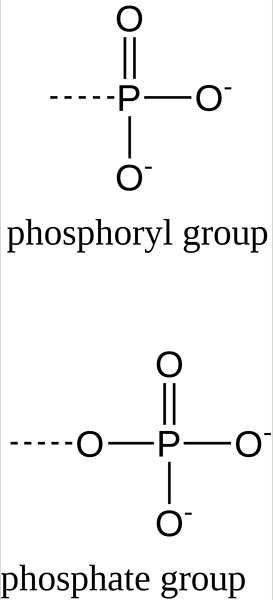
Gambar 01: Formula kimia gugus fosforil dan gugus fosfat
Saat mempertimbangkan proses biokimia, jika gugus fosfat terlibat dalam suatu reaksi, gugus fosforil biasanya ditransfer antara senyawa substrat. Reaksi ini dikenal sebagai reaksi transfer fosforil. Namun, kelompok fosforil bukanlah kelompok fosfat.
Apa itu kelompok fosfat?
Gugus fosfat adalah anion yang memiliki formula kimia PO4-3. Istilah ini dapat digunakan untuk memberi nama AM anion, senyawa garam yang mengandung gugus fosfat, gugus fungsional dan ester yang mengandung gugus fosfat. Paling umum, kami menyebut anion ini anion ortofosfat karena terbentuk dari asam ortofosfat.
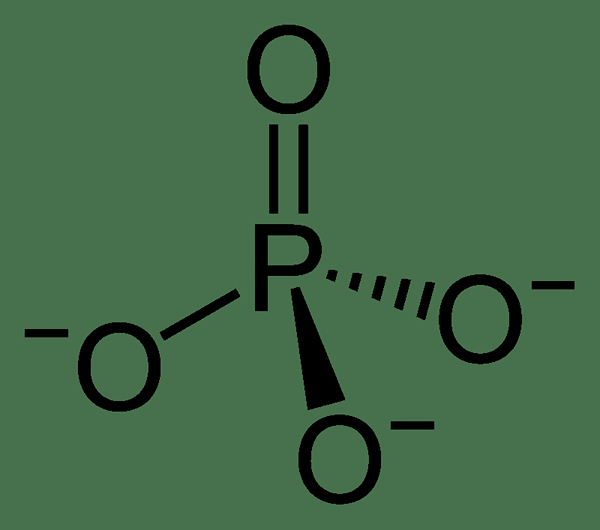
Gambar 02: Struktur kimia gugus fosfat
Anion ini terbentuk dari asam fosfat melalui pengangkatan tiga proton. Penghapusan satu proton membentuk anion dihidrogen fosfat, sedangkan penghapusan dua proton membentuk anion hidrogen fosfat. Nama -nama ini dapat digunakan untuk merujuk pada senyawa garam yang sesuai.
Massa molar anion fosfat adalah 94.97 g/mol. Ada atom fosfor sentral yang terikat pada empat atom oksigen, dan anion memiliki geometri tetrahedral. Sebagian besar senyawa yang mengandung fosfat adalah zat yang larut dalam air pada suhu dan tekanan kamar. Beberapa senyawa fosfat juga tidak larut dalam air.
Dalam sistem biologis, kita terutama dapat menemukan gugus fosfat dalam bentuk fosfat anorganik. Kita dapat menemukan anion fosfat bebas dalam solusi dalam sistem biologis. Jika tidak, anion fosfat terjadi terikat pada molekul organik dalam bentuk organofosfat. Umumnya, fosfat dapat ditemukan sebagai ester dalam nukleotida, dalam DNA dan dalam RNA.
Apa perbedaan antara gugus fosforil dan kelompok fosfat?
Kelompok fosforil adalah ion kimia yang memiliki formula kimia P+HAI32- sedangkan gugus fosfat adalah anion yang memiliki formula kimia PO4-3. Perbedaan utama antara gugus fosforil dan gugus fosfat adalah bahwa gugus fosforil mengandung satu atom fosfor yang terikat pada tiga atom oksigen dan muatan -2, sedangkan gugus fosfat mengandung satu atom fosfor yang terikat pada empat atom oksigen dan -3 muatan.
Gambar berikut menyajikan perbedaan antara gugus fosforil dan gugus fosfat dalam bentuk tabel.
Ringkasan -gugus fosforil vs gugus fosfat
Kelompok fosforil adalah ion kimia yang memiliki formula kimia P+HAI32-. Sementara itu, gugus fosfat adalah anion yang memiliki formula kimia PO4-3. Perbedaan utama antara gugus fosforil dan gugus fosfat adalah bahwa gugus fosforil mengandung satu atom fosfor yang terikat pada tiga atom oksigen dan muatan -2, sedangkan gugus fosfat mengandung satu atom fosfor yang terikat pada empat atom oksigen dan -3 muatan.
Referensi:
1. “Kelompok Fosfat: Definisi & Penjelasan." Belajar.com.
Gambar milik:
1. “Fosforl-Group-and-Fosfat-Group” oleh Strater-Dihasilkan dengan ChemDraw (CC BY-SA 3.0) Via Commons Wikimedia
2. "Fosfat -ion" oleh Neurotiker ⇌ - karya sendiri (domain publik) melalui Commons Wikimedia


