Perbedaan antara keadaan kompleks dan transisi teraktivasi
Keadaan transisi kompleks vs teraktivasi | Kompleks transisi vs kompleks aktivasi
Ketika satu atau lebih reaktan mengkonversi menjadi produk, mereka dapat melalui berbagai modifikasi dan perubahan energi. Ikatan kimia dalam reaktan pecah, dan ikatan baru dibentuk untuk menghasilkan produk, yang sama sekali berbeda dari reaktan. Modifikasi kimia ini dikenal sebagai reaksi kimia. Ada banyak variabel yang mengendalikan reaksi. Untuk reaksi terjadi, harus ada energi yang diperlukan. Molekul reaktan mengalami perubahan di seluruh reaksi dengan asumsi berbagai konfigurasi atom. Keadaan kompleks dan transisi yang diaktifkan adalah dua terminologi yang digunakan untuk mengidentifikasi kompleks menengah ini dan sebagian besar waktu kedua istilah ini digunakan secara bergantian.
Apa yang diaktifkan kompleks?
Molekul harus diaktifkan sebelum mereka dapat menjalani reaksi. Molekul biasanya tidak memiliki banyak energi dengan mereka, hanya kadang -kadang beberapa molekul berada dalam keadaan energi untuk menjalani reaksi. Di mana ada dua reaktan, agar reaksi terjadi, reaktan harus bertabrakan satu sama lain dalam orientasi yang tepat. Meskipun reaktan hanya bertemu satu sama lain, sebagian besar pertemuan tidak mengarah pada reaksi. Pengamatan ini telah memberikan gagasan memiliki penghalang energi untuk reaksi. Reaktan dengan keadaan energi yang lebih tinggi dalam campuran reaksi dapat dianggap sebagai kompleks teraktivasi. Tidak semua kompleks yang diaktifkan dapat digunakan untuk produk, mereka dapat jatuh kembali ke reaktan jika mereka tidak memiliki energi yang cukup.
Apa itu keadaan transisi?
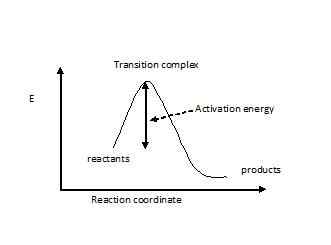
Keadaan transisi dipikirkan di mana molekul yang bereaksi tegang atau terdistorsi atau memiliki konfigurasi elektronik yang tidak menguntungkan. Molekul harus melewati keadaan transisi berenergi tinggi ini sebelum reaksi akan terjadi. Kesenjangan energi dikenal sebagai energi aktivasi. Ini adalah penghalang energi tertinggi untuk reaksi terjadi. Jika aktivasi untuk reaksi terlalu tinggi, hanya sebagian kecil molekul yang akan memiliki energi yang cukup untuk mengatasinya, sehingga konsentrasi produk yang diharapkan tidak akan diperoleh. Susunan atom dari semua molekul dalam reaksi, yang memiliki energi aktivasi, disebut kompleks transisi. Kompleks transisi memiliki komponen dengan ikatan yang rusak sebagian dan sebagian membuat ikatan baru. Oleh karena itu, ia memiliki muatan negatif dan positif parsial. Keadaan transisi ditampilkan dengan tanda belati ganda (‡). Jika keadaan keadaan transisi dari suatu reaksi dapat diturunkan, maka reaksi harus jauh lebih cepat dan akan membutuhkan energi rendah untuk melanjutkan. Untuk reaksi eksotermik, berikut adalah kurva energi.
 Sangat penting untuk mengetahui struktur keadaan transisi terutama saat merancang obat untuk penghambatan enzim.
Sangat penting untuk mengetahui struktur keadaan transisi terutama saat merancang obat untuk penghambatan enzim.
|
Apa perbedaan antara keadaan kompleks dan transisi teraktivasi? • Keadaan transisi adalah pengaturan atom dengan energi tertinggi saat reaktan pergi ke produk. Kompleks yang diaktifkan adalah semua konfigurasi lain di jalur reaksi, yang memiliki energi lebih tinggi dari molekul normal. • Ada kemungkinan tinggi kompleks keadaan transisi untuk pergi ke produk. Namun, kompleks aktivasi dapat kembali membentuk reaktan daripada pergi ke produk.
|


