Perbedaan antara alkoksida dan fenoksida
Itu perbedaan utama antara alkoksida dan fenoksida adalah itu Alkoksida terbentuk ketika atom hidrogen dari gugus alkohol dihilangkan, sedangkan fenoksida terbentuk ketika kita menghilangkan atom hidrogen dari kelompok -OH molekul fenol.
Baik alkoksida dan fenoksida adalah anion, dan mereka penting sebagai kelompok fungsional dalam reaksi sintesis kimia. Anion alkoksida adalah dasar konjugat dari alkohol apa pun, tetapi anion fenoksida adalah dasar konjugat fenol.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu alkoksida
3. Apa itu fenoksida
4. Perbandingan berdampingan - alkoksida vs fenoksida dalam bentuk tabel
5. Ringkasan
Apa itu alkoksida?
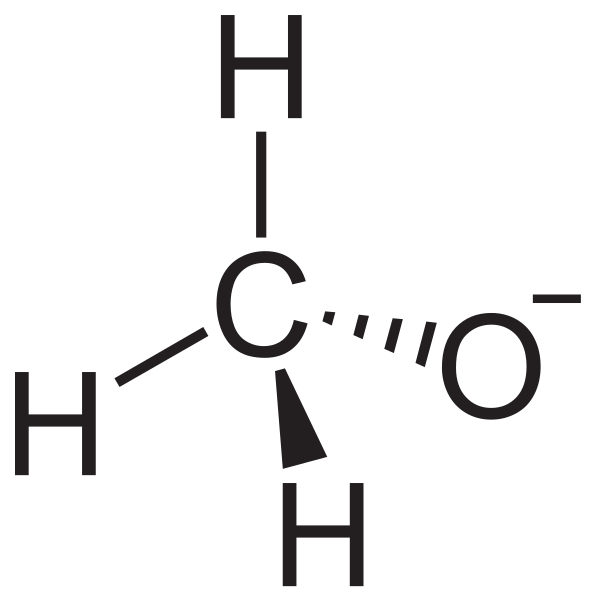
Alkoksida adalah anion yang terbentuk saat kita menghilangkan atom hidrogen dari kelompok -OH alkohol. Oleh karena itu, itu adalah basis alkohol konjugat. Kita bisa menulis struktur umum alkoksida sebagai ro-. R adalah substituen organik. Misalnya, jika kita memiliki gugus metil di sana, maka alkoksida dinamai metoksida.

Gambar 01: Struktur anion metoksida
Alkoksida dapat bertindak sebagai basis yang kuat. Ketika kelompok R adalah kelompok alkil sederhana (bukan kelompok besar), alkoksida dapat bertindak sebagai nukleofil yang baik dan sebagai ligan. Namun, anion ini tidak terlalu stabil dalam pelarut protik, saya.e. air.
Biasanya, alkali logam alkoksida terjadi sebagai senyawa polimer jika kelompok R kecil. Selain itu, anion alkoksida dapat bertindak sebagai ligan menjembatani yang baik juga. Ada beberapa cara agar kita dapat menyiapkan alkoksida. Sebagai contoh, kita dapat memproduksinya dari pengurangan logam, klorida elektrofilik, reaksi metatesis, dan melalui proses elektrokimia, dll. Saat mempertimbangkan penggunaan, logam transisi yang mengandung alkoksida berguna dalam pelapis dan sebagai katalis.
Apa itu fenoksida
Fenoksida adalah anion yang terbentuk ketika kita menghilangkan atom hidrogen dari kelompok -OH dari fenol. Oleh karena itu, itu adalah dasar konjugat fenol. Jika kita mengganti atom hidrogen ini dari atom lain, kita bisa mendapatkan senyawa baru. Misalnya, jika kita mengganti atom hidrogen dari atom natrium, kita mendapatkan natrium fenoksida.
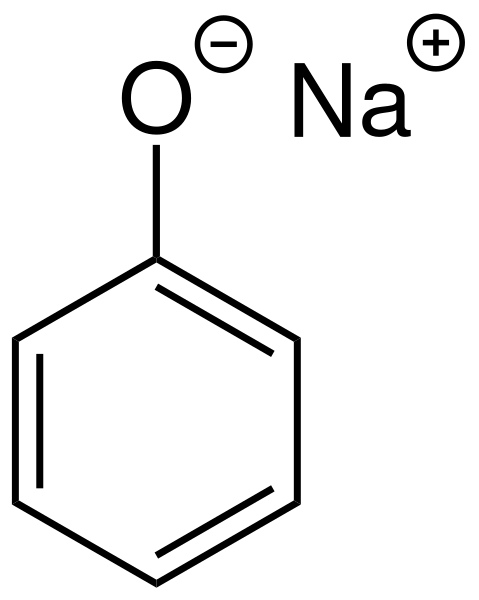
Gambar 02: Struktur anion fenoksida dengan natrium; Sodium fenoksida
Formula kimia umum untuk anion ini adalah C6H5HAI-. Fenol bersifat asam, tetapi fenoksida adalah dasar karena cenderung menerima proton karena muatan negatif pada atom oksigen dari anion fenoksida.
Apa perbedaan antara alkoksida dan fenoksida?
Baik alkoksida dan fenoksida adalah anion dan penting sebagai kelompok fungsional dalam reaksi sintesis kimia. Perbedaan utama antara alkoksida dan fenoksida adalah bahwa alkoksida terbentuk ketika atom hidrogen dari gugus alkohol dihilangkan, sedangkan fenoksida terbentuk ketika kita menghilangkan atom hidrogen dari kelompok -OH dari molekul fenol fenol. Oleh karena itu, anion alkoksida adalah dasar konjugat dari alkohol apa pun, tetapi anion fenoksida adalah dasar konjugat fenol.
Kedua anion ini adalah senyawa dasar karena cenderung mendapatkan proton dari luar untuk menetralkan muatan negatif mereka. Selain itu, anion alkoksida berguna sebagai ligan menjembatani. Sementara itu, fenoksida berguna dalam reaksi sintesis organik untuk menambahkan cincin benzena ke bagian kimia lain. Formula kimia umum untuk anion alkoksida adalah ro-, sedangkan untuk anion fenoksida formula kimia umum adalah c6H5HAI-.
Di bawah infografis merangkum perbedaan antara alkoksida dan fenoksida.

Ringkasan -alkoksida vs fenoksida
Singkatnya, baik alkoksida dan fenoksida adalah anion, dan mereka penting sebagai kelompok fungsional dalam reaksi sintesis kimia. Perbedaan utama antara alkoksida dan fenoksida adalah bahwa alkoksida terbentuk ketika atom hidrogen dari gugus alkohol dihilangkan, sedangkan fenoksida terbentuk ketika kita menghilangkan atom hidrogen dari kelompok -OH dari molekul fenol fenol.
Referensi:
1. Helmenstine, Anne Marie. “Definisi alkoksida dalam kimia."Thoughtco, Nov. 19, 2019, tersedia di sini.
2. “Ion fenoksida.”Kimia Libretexts, Libretexts, 5 Juni 2019, tersedia di sini.
Gambar milik:
1. “Methanolat -ion” oleh NeuroTiker - karya sendiri (domain publik) melalui Commons Wikimedia
2. “Formula Struktural Sodium Phenoxide” oleh Chem Sim 2001 - Karya Sendiri (Domain Publik) Via Commons Wikimeida


