Perbedaan antara azeotropik dan distilasi ekstraktif
Perbedaan Utama - Azeotropik VS Ekstraktif Distilasi
Itu perbedaan utama antara azeotropik dan distilasi ekstraktif adalah dalam distilasi azeotropik, Pembentukan azeotrope diperlukan untuk memisahkan komponen campuran sedangkan, dalam distilasi ekstraktif, tidak ada pembentukan azeotrope yang terjadi.
Distilasi adalah proses pemurnian cairan dengan proses pemanasan dan pendinginan. Dalam distilasi azeotropik, azeotrope terbentuk sebelum pemisahan komponen dari campuran. Sebuah Azeotrope adalah campuran komponen yang memiliki titik didih yang konstan. Dalam proses distilasi ekstraktif, tidak perlu membentuk azeotrope. Dalam metode itu, komponen ketiga ditambahkan ke campuran biner. Komponen ketiga ini dapat mempengaruhi volatilitas komponen yang ada.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu distilasi azeotropik
3. Apa itu distilasi ekstraktif
4. Perbandingan Berdampingan - Distilasi Azeotropik Vs Ekstraktif dalam Bentuk Tabel
5. Ringkasan
Apa itu distilasi azeotropik?
Distilasi azeotropik adalah teknik pemisahan yang digunakan untuk memisahkan komponen campuran dengan membentuk azeotrope. Azeotrop adalah campuran komponen dengan titik didih yang konstan. Jenis campuran ini tidak dapat dipisahkan menjadi komponen dengan distilasi sederhana karena semua komponen memiliki titik didih yang sama. Saat campuran azeotropik direbus, proporsi komponen dalam cairan dan fase uapnya sama.
Dalam metode distilasi azeotropik, komponen baru (dikenal sebagai entrainer) ditambahkan ke campuran azeotropik untuk membentuk azeotrope baru yang mendidih pada suhu yang lebih rendah daripada azeotrope yang ada yang ada yang ada. Kemudian sistem ini memiliki dua fase cair yang tidak bercampur dengan titik didih yang berbeda (heterogen).

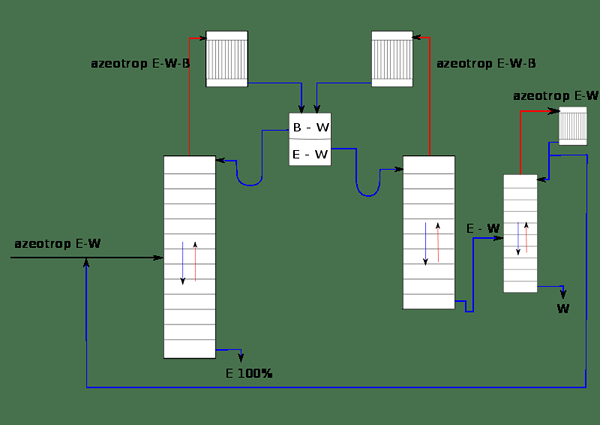
Gambar 01: Sistem pemisahan etanol (E) dari air (w) menggunakan benzena (b)
Misalnya, mari kita pertimbangkan campuran etanol dan air. Itu dikenal sebagai a Biner Azeotrope Karena ada dua komponen yang tidak mungkin dalam campuran. Jika benzena ditambahkan sebagai entrainer ke campuran ini, ia dapat mempengaruhi volatilitas komponen lain dalam campuran. Campuran sekarang disebut tersier azeotrope karena ada tiga komponen dalam campuran. Saat campuran ini disuling, dikenal sebagai distilasi azeotropik.
Apa itu distilasi ekstraktif?
Distilasi ekstraktif adalah teknik pemisahan yang mencakup penambahan komponen ketiga ke dalam campuran biner untuk memungkinkan pemisahan kedua komponen. Namun, komponen ketiga tidak menguap selama proses distilasi; Komponen ketiga harus kurang mudah menguap. Atau yang lain, harus memiliki titik didih yang lebih tinggi.
Jika campuran biner memiliki dua komponen dengan titik didih yang relatif mirip, maka komponen ini tidak dapat dipisahkan dengan distilasi sederhana. Ini terjadi karena kedua komponen akan diuapkan pada suhu yang hampir sama (resolusi buruk).
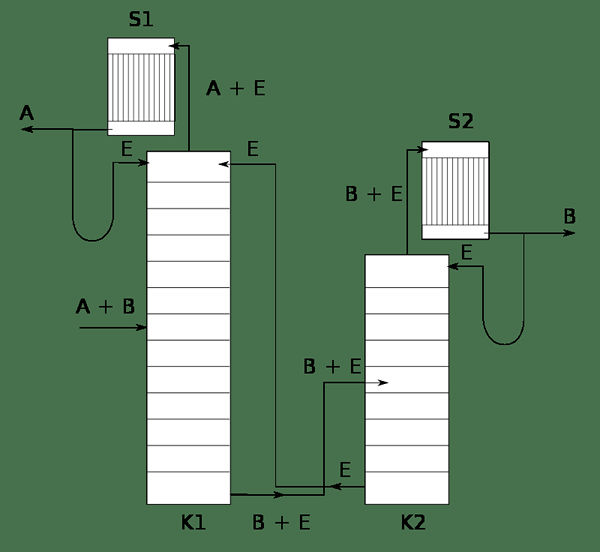
Gambar 02: Suatu sistem yang menunjukkan distilasi ekstraktif campuran A dan B menggunakan pelarut E
Selama proses distilasi ekstraktif, azeotrope tidak terbentuk. Proses ini melibatkan pelarut dengan volatilitas yang sangat rendah karena pelarut campuran komponen. Itu dikenal sebagai pelarut pemisahan. Selama distilasi, komponen dengan volatilitas tertinggi akan mudah diuapkan sebagai produk teratas. Sisanya adalah pelarut dan komponen lainnya (dalam campuran biner). Karena pelarut tidak membentuk azeotrope dengan komponen kedua, itu juga dapat dipisahkan dengan mudah dengan metode yang tersedia.
Misalnya, ekstraksi toluena dari parafin dapat dilakukan dalam metode distilasi ekstraktif. Campuran toluena dan iso-oktan memiliki berat molekul yang hampir sama. Oleh karena itu, pemisahan toluena dari campuran ini sangat sulit. Tetapi ketika fenol ditambahkan ke dalam campuran ini, titik didih meningkatnya iso-oktan. Ini membuatnya mudah untuk memisahkan toluena dari campuran ini.
Apa perbedaan antara azeotropik dan distilasi ekstraktif?
Distilasi azeotropik vs ekstraktif | |
| Distilasi azeotropik adalah teknik pemisahan yang digunakan untuk memisahkan komponen campuran dengan membentuk azeotrope. | Distilasi ekstraktif adalah teknik pemisahan yang mencakup penambahan komponen ketiga ke dalam campuran biner untuk memungkinkan pemisahan kedua komponen. |
| Teknik | |
| Dalam teknik distilasi azeotropik, pembentukan azeotrop sebelum distilasi adalah penting. | Dalam teknik distilasi ekstraktif, komponen non-volatil ditambahkan ke dalam campuran yang dapat mempengaruhi volatilitas komponen dalam campuran. |
| Pemisahan | |
| Distilasi azeotropik memisahkan komponen ke dalam fase uap yang memiliki komposisi kimia yang sama seperti pada fase cair. | Distilasi ekstraktif memisahkan komponen dari matriks zat. |
Ringkasan - Azeotropik vs Ekstraktif Distilasi
Distilasi adalah teknik kimia yang digunakan untuk pemisahan komponen yang berbeda dalam campuran. Ada banyak jenis teknik distilasi, distilasi sederhana menjadi tipe yang paling sederhana. Distilasi azeotropik dan distilasi ekstraktif adalah dua jenis distilasi penting. Perbedaan antara distilasi azeotropik dan ekstraktif adalah bahwa pembentukan azeotrope diperlukan untuk memisahkan komponen campuran sedangkan, dalam distilasi ekstraktif, tidak ada pembentukan azeotrope yang terjadi.
Referensi:
1. “Distilasi azeotropik.”Wikipedia, Wikimedia Foundation, 4 Apr. 2018. Tersedia disini
2. “Distilasi ekstraktif.”Wikipedia, Wikimedia Foundation, 14 Jan. 2018. Tersedia disini
3. “Azeotrope.”Wikipedia, Wikimedia Foundation, 8 Apr. 2018. Tersedia disini
Gambar milik:
1.'Distil Extract'by Joanna Kośmider - karya sendiri, (domain publik) via commons wikimedia
2.'Azeotr Distill2'by Joanna Kośmider - karya sendiri, (domain publik) via Commons Wikimedia


