Perbedaan antara butana dan isobutane

Butana vs isobutane
Molekul organik adalah molekul yang terdiri dari karbon. Hidrokarbon adalah molekul organik, yang hanya terdiri dari atom karbon dan hidrogen. Hidrokarbon bisa aromatik atau alifatik. Mereka terutama dibagi menjadi beberapa jenis sebagai alkana, alkena, alkin, sikloalkanes dan hidrokarbon aromatik. Heksana dan n-heksana adalah alkana atau sebaliknya, dikenal sebagai hidrokarbon jenuh. Mereka memiliki jumlah atom hidrogen tertinggi, yang dapat ditampung oleh molekul. Semua ikatan antara atom karbon dan hidrogen adalah ikatan tunggal. Karena itu, rotasi ikatan diizinkan antara atom apa pun. Mereka adalah jenis hidrokarbon yang paling sederhana. Hidrokarbon jenuh memiliki formula umum CNH2n+2. Kondisi ini sedikit berbeda untuk sikloalkana karena mereka memiliki struktur siklik.
Butana
Seperti yang dinyatakan di atas, hidrokarbon butana adalah alkana jenuh. Ia memiliki empat atom karbon; Oleh karena itu, memiliki formula molekul C4H10. Massa molar butana adalah 58.12 g Mol−1. Titik lebur butana adalah 133-139 K, dan titik didihnya adalah 272-274 K. Butana adalah nama umum yang digunakan untuk menunjukkan semua molekul dengan formula ini. Ada dua isomer struktural yang dapat kita gambar agar sesuai dengan rumus ini tetapi, dalam nomenklatur IUPAC, kami menggunakan butana secara khusus untuk menunjukkan molekul yang tidak bercabang, yang juga dikenal sebagai n-butana. Itu memiliki struktur berikut.

Isomer struktural lainnya seperti molekul propana yang dimetilasi. Itu dikenal sebagai isobutane. Butana adalah gas yang tidak berwarna. Itu bisa dengan mudah dicairkan. Gas butana sangat mudah terbakar. Butana adalah komponen gas alam, dan diproduksi saat bensin disempurnakan. Setelah pembakaran total, butana menghasilkan karbon dioksida dan air. Namun, jika tidak ada cukup gas oksigen untuk pembakaran, ia menghasilkan karbon monoksida dan air dari pembakaran parsial. Butana digunakan sebagai bahan bakar. Saat memproduksi gas LP, butana dicampur dengan propana dan hidrokarbon lainnya. Ini digunakan untuk tujuan memasak di rumah tangga. Ini juga digunakan dalam pemantik.
Isobutane
Isobutane adalah isomer struktural butana. Ini memiliki formula molekul yang sama dengan butana, tetapi formula struktural berbeda. Ini juga dikenal sebagai methylpropane. Itu memiliki struktur berikut.
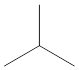
Isobutane memiliki karbon tersier, dan itu adalah molekul paling sederhana dengan karbon tersier. Isobutane adalah gas transparan yang tidak berwarna. Titik lebur isobutan adalah 40-240 K, dan titik didihnya adalah 260-264 K. Ini terutama digunakan sebagai refrigeran. Bentuk murni isobutan digunakan dalam lemari es. Selanjutnya, ini digunakan sebagai propelan dalam semprotan aerosol.
| Apa perbedaan antara butana dan isobutane? • isobutan adalah isomer struktural butana. • butana tidak bercabang, dan isobutane bercabang. • Keduanya memiliki formula molekul yang sama, tetapi formula struktural berbeda. • butana memiliki empat atom karbon dalam rantai lurus, sedangkan isobutan hanya memiliki tiga atom karbon dalam rantai lurus. • Sifat fisik butana dan isobutane berbeda. Misalnya, mereka memiliki titik leleh yang berbeda, titik didih, kepadatan, dll. • Isobutan murni terutama digunakan sebagai refrigeran |


