Perbedaan antara kalsium klorida dan magnesium klorida

Itu perbedaan utama Antara kalsium klorida dan magnesium klorida adalah itu Kalsium klorida mengandung kation kalsium dengan dua anion klorida sedangkan magnesium klorida mengandung kation magnesium dengan dua anion klorida.
Baik kalsium klorida dan magnesium klorida adalah senyawa garam yang mengandung kation dan anion. Ini adalah padatan pada suhu kamar yang sangat larut dalam air. Selain itu, keduanya digunakan untuk pengendalian debu. Mari kita bicarakan lebih detail tentang mereka.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu kalsium klorida
3. Apa itu magnesium klorida
4. Perbandingan berdampingan - kalsium klorida vs magnesium klorida dalam bentuk tabel
5. Ringkasan
Apa itu kalsium klorida?
Kalsium klorida adalah garam anorganik yang memiliki ion kalsium yang terkait dengan dua ion klorida. Formula kimia senyawa ini adalah CaCl2. Massa molar adalah 110.9 g/mol. Pada suhu kamar, itu ada sebagai padatan putih kristal. Apalagi higroskopis dan mudah larut dalam air. Oleh karena itu kita bisa menggunakannya sebagai pengeringan. Ini tersedia sebagai bentuk anhidrat atau bentuk terhidrasi. Titik leleh dan mendidih kalsium klorida anhidrat masing -masing adalah 775 ° C dan 1.935 ° C. Metode utama memproduksi kalsium klorida adalah sebagai produk sampingan dari proses solvay. Itu menggunakan batu kapur.
2 NaCl + Caco3 → Na2BERSAMA3 + CACL2
Salah satu aplikasi utama senyawa ini adalah sebagai agen de-icing. Itu de-ice dengan titik beku air yang menyedihkan.

Gambar 01: Kristal kalsium klorida
Aplikasi terbesar kedua adalah digunakan sebagai agen pengendali debu. Karena sifat higroskopisnya, larutan terkonsentrasi dapat menjaga lapisan cair di tanah permukaan jalan. Oleh karena itu mengendalikan debu. Apalagi ini dapat meningkatkan kekerasan air. Mis: Untuk meningkatkan kekerasan air di kolam renang.
Apa itu magnesium klorida?
Magnesium klorida adalah garam anorganik yang memiliki ion magnesium yang terkait dengan dua ion klorida. Formula kimia senyawa ini adalah mgcl2. Massa molar adalah 95 g/mol. Titik lebur dan titik didih masing -masing adalah 714 ° C dan 1.412 ° C. Pada suhu kamar, itu ada sebagai padatan kristal putih atau tidak berwarna. Sangat larut dalam air dan tersedia dalam bentuk terhidrasi juga. Kita dapat mengekstrak bentuk hidrat dari air garam atau air laut. Ada beberapa hidrat dari senyawa ini yang mengandung 2, 4, 6, 8 atau 12 molekul air. Hidrat ini kehilangan molekul air ini setelah pemanasan. Kita dapat menghasilkan senyawa ini melalui proses Dow. Di sana, magnesium klorida regenerat dari magnesium hidroksida setelah reaksi dengan asam klorida.
Mg (oh)2(S) + 2 HCL → MGCL2 (aq) + 2 h2HAI(l)
Aplikasi utama magnesium klorida anhidrat adalah berguna sebagai prekursor untuk menghasilkan logam magnesium.

Gambar 02: Kristal magnesium klorida
Kami dapat menghasilkan logam ini melalui elektrolisis MGCL2. Selain itu, kita dapat menggunakan senyawa ini untuk pengendalian debu, stabilisasi padat, mitigasi erosi angin, dll. Sebagai penting lainnya, kami menggunakan MGCL2 sebagai dukungan katalis untuk Ziegler-Natta Catalyst.
Apa perbedaan antara kalsium klorida dan magnesium klorida?
Kalsium klorida adalah garam anorganik yang memiliki ion kalsium yang terkait dengan dua ion klorida. Oleh karena itu, formula kimia senyawa ini adalah CaCl2. Massa molarnya adalah 110.9 g/mol. Selain itu, titik leleh dan mendidih kalsium klorida anhidrat masing -masing adalah 775 ° C dan 1.935 ° C. Magnesium klorida adalah garam anorganik yang memiliki ion magnesium yang terkait dengan dua ion klorida. Oleh karena itu formula kimia dari senyawa ini adalah mgcl2. Massa molarnya adalah 95 g/mol. Selain itu, titik leleh dan titik didih magnesium klorida anhidrat masing -masing adalah 714 ° C dan 1.412 ° C. Senyawa ini memiliki aplikasi yang berbeda, tetapi satu kesamaan; keduanya adalah agen pengendali debu yang penting.
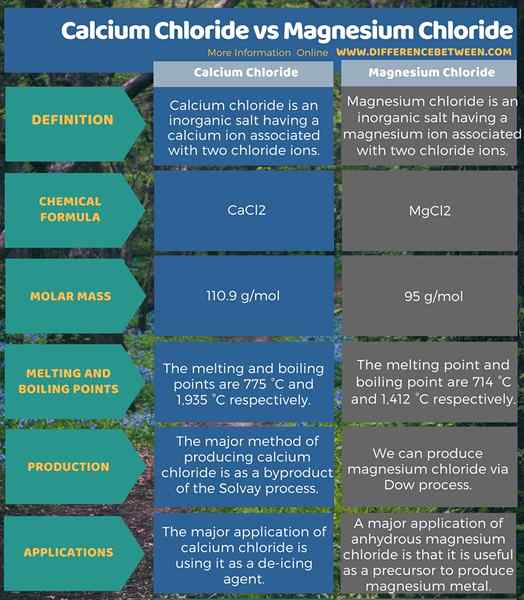
Ringkasan -kalsium klorida vs magnesium klorida
Baik kalsium dan magnesium klorida penting sebagai agen kontrol debu. Perbedaan antara kalsium klorida dan magnesium klorida adalah bahwa kalsium klorida mengandung kation kalsium dengan dua anion klorida sedangkan magnesium klorida mengandung kation magnesium dengan dua anion klorida.
Referensi:
1. "Kalsium klorida.”Wikipedia, Wikimedia Foundation, 23 Juli 2018. Tersedia disini
2. “Magnesium klorida."Informasi Nasional untuk Informasi Bioteknologi. Database senyawa pubchem, u.S. Perpustakaan Kedokteran Nasional. Tersedia disini
Gambar milik:
1.'Kalsium klorida CaCl2'by tidak ada penulis yang dapat dibaca mesin yang disediakan. (CC BY-SA 3.0) Via Commons Wikimedia
2.'Magnesium Chloride' (domain publik) via Commons Wikimedia


