Perbedaan antara asam kromik dan kromium trioksida

Itu perbedaan utama Antara asam kromik dan kromium trioksida Asam kromik adalah larutan asam yang kuat yang dibuat dengan menggabungkan asam sulfat pekat dengan dikromat, sedangkan kromium trioksida adalah anhidrida asam asam kromik.
Asam kromik dan kromium trioksida adalah dua zat terkait; Asam kromik dapat dibuat dari hidrasi kromium trioksida. Ini adalah zat anorganik yang mengandung elemen kimia kromium.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu asam krom
3. Apa itu kromium trioksida
4. Perbandingan berdampingan - asam kromik vs kromium trioksida dalam bentuk tabel
5. Ringkasan
Apa itu asam krom?
Asam kromat adalah larutan asam yang kuat yang mengandung molekul H2CRO4. Namun, asam ini biasanya dibuat dari kombinasi asam sulfat pekat dan dikromat. Oleh karena itu, asam ini dapat mengandung berbagai senyawa, termasuk kromium padat trioksida. Asam kuat ini berguna dalam pembersihan bahan kaca. Atom kromium dalam asam kromat molekul berada dalam keadaan oksidasi +6. Asam ini dianggap sebagai asam yang kuat dan sangat korosif.
Secara umum, asam kromik dapat diamati sebagai kristal merah gelap. Asam kromat molekul memiliki fitur umum dengan molekul asam sulfat. Mereka memiliki pola deprotonasi yang serupa dan kekuatan asam.
Asam kromik adalah zat pengoksidasi yang penting, dan dapat mengoksidasi senyawa organik seperti alkohol menjadi asam dan keton karboksilat, alkohol primer dan sekunder menjadi aldehida dan keton yang sesuai, dll.

Gambar 01: Asam Kromik
Saat mempertimbangkan penggunaan asam kuat ini, penting sebagai perantara dalam proses pelapisan kromium, berguna dalam glasir keramik dan kaca berwarna, sebagai agen pengoksidasi yang kuat, berguna dalam membersihkan gelas laboratorium, dalam industri perbaikan alat musik karenanya karena itu Kemampuan untuk mencerahkan bahan kuningan, berguna dalam pembuatan pewarna rambut, sebagai pemutih dalam pemrosesan pembalikan fotografi hitam dan putih, dll.
Apa itu kromium trioksida?
Chromium trioxide adalah senyawa anorganik yang memiliki formula kimia CRO3. Itu adalah bentuk asam kromi anhidrat asam. Oleh karena itu, kedua zat ini terkadang tersedia di pasaran dengan nama yang sama. Kita dapat mengamati zat ini sebagai padatan gelap, berwarna ungu di bawah kondisi anhidratnya, dan ketika zat terhidrasi, muncul dalam warna oranye. Zat ini disiapkan terutama untuk proses elektroplating. Selain itu, kromium trioksida adalah pengoksidasi yang sangat kuat; Oleh karena itu, itu juga merupakan karsinogen.

Gambar 02: kromium basah trioksida
Selain proses pelapisan krom, ada penggunaan kromium trioksida lain seperti generasi film kromat yang dilewati yang tahan terhadap korosi, berguna dalam produksi rubi sintetis, berguna dalam menerapkan jenis lapisan anodik ke aluminium, dll.
Apa perbedaan antara asam kromik dan kromium trioksida?
Asam kromat adalah larutan asam yang kuat yang mengandung molekul H2CRO4. Chromium trioxide adalah senyawa anorganik yang memiliki formula kimia CRO3. Asam kromik dan kromium trioksida adalah senyawa anorganik. Perbedaan utama antara asam kromat dan kromium trioksida adalah bahwa asam kromik adalah larutan asam yang kuat yang dibuat dengan menggabungkan asam sulfat pekat dengan dikromat, sedangkan kromium trioksida adalah anhidrida asam dari asam kromik.
Di bawah ini mencantumkan lebih banyak perbedaan antara asam kromik dan kromium trioksida.
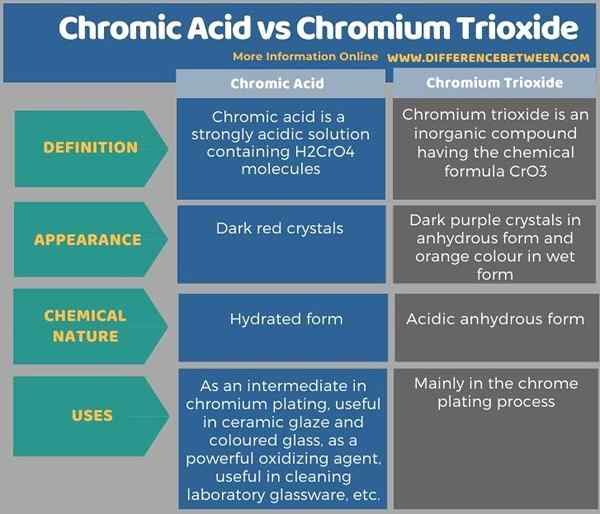
Ringkasan -Asam Kromik vs Chromium Trioxide
Kromik dapat disiapkan dengan hidrasi kromium trioksida. Perbedaan utama antara asam kromat dan kromium trioksida adalah bahwa asam kromik adalah larutan asam yang kuat yang dibuat dengan menggabungkan asam sulfat pekat dengan dikromat, sedangkan kromium trioksida adalah anhidrida asam dari asam kromik.
Referensi:
1. “Oksidasi dengan asam kromik." Libreteks Kimia, 13 September. 2020, tersedia di sini.
Gambar milik:
1. “Chromic-Acid-Photo” oleh Himstakan-Karya Sendiri (CC BY-SA 4.0) Via Commons Wikimedia
2. “Reaksi antara kalium dikromat dan asam sulfat (1)” oleh Rando Tuvikene - karya sendiri (CC BY -SA 4.0) Via Commons Wikimedia