Perbedaan antara kovalensi dan keadaan oksidasi
Perbedaan utama - kovalensi vs Keadaan oksidasi
Atom dari berbagai elemen kimia terikat satu sama lain membentuk senyawa kimia yang berbeda. Dalam pembentukan suatu senyawa, atom -atom diikat satu sama lain melalui ikatan ionik atau ikatan kovalen. Keadaan kovalensi dan oksidasi adalah dua istilah yang menggambarkan keadaan atom -atom ini dalam senyawa kimia. Kovalensi adalah jumlah ikatan kovalen yang dapat dibentuk oleh atom. Oleh karena itu, kovalensi tergantung pada jumlah elektron yang dapat dibagikan atom dengan atom lainnya. Keadaan oksidasi atom adalah jumlah elektron yang diperoleh atau hilang oleh atom tertentu saat membentuk ikatan kimia. Itu perbedaan utama Antara kovalensi dan keadaan oksidasi adalah bahwa Kovalensi atom adalah jumlah ikatan kovalen yang dapat dibentuk atom sedangkan keadaan oksidasi atom adalah jumlah elektron yang hilang atau diperoleh dengan atom saat membentuk ikatan kimia.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu kovalensi
3. Apa keadaan oksidasi
4. Perbandingan berdampingan - kovalensi vs keadaan oksidasi dalam bentuk tabel
5. Ringkasan
Apa itu kovalensi?
Kovalensi adalah jumlah ikatan kovalen yang dapat dibentuk oleh atom dengan atom lainnya. Oleh karena itu, kovalensi ditentukan oleh jumlah elektron yang ada di orbital terluar atom. Namun, istilah valensi dan kovalensi tidak boleh bingung karena mereka memiliki makna yang berbeda. Valensi adalah kekuatan kombinasi atom. Terkadang, kovalensi sama dengan valensi. Namun, itu tidak selalu terjadi.
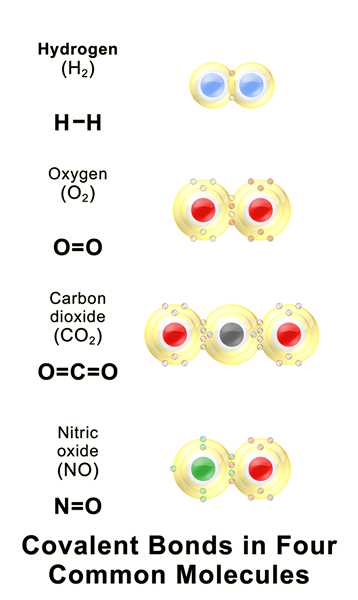
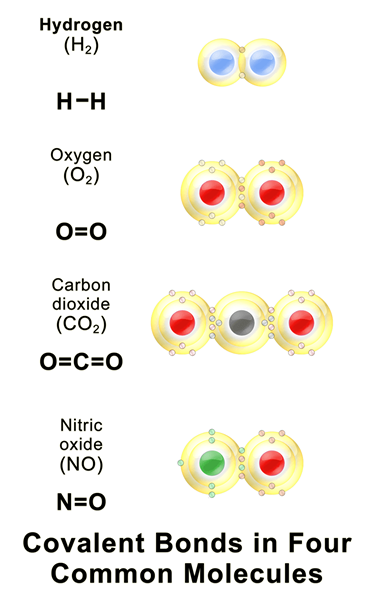
Gambar 01: Beberapa senyawa kovalen umum
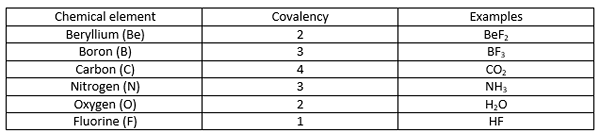
Ikatan kovalen adalah ikatan kimia yang terbentuk ketika dua atom berbagi elektron tidak berpasangan terluar untuk menyelesaikan konfigurasi elektron. Ketika sebuah atom memiliki kerang elektron atau orbital yang tidak lengkap, atom itu menjadi lebih reaktif karena konfigurasi elektron yang tidak lengkap tidak stabil. Oleh karena itu, atom -atom ini baik gain/elektron longgar atau berbagi elektron untuk mengisi cangkang elektron. Tabel berikut menunjukkan beberapa contoh elemen kimia dengan nilai kovalensi yang berbeda.
Apa keadaan oksidasi?
Keadaan oksidasi atom adalah jumlah elektron yang hilang, diperoleh atau dibagikan oleh atom dengan atom lain. Jika elektron hilang atau diperoleh, muatan listrik atom diubah sesuai. Elektron bermuatan negatif partikel subatomik yang muatannya dinetralkan oleh muatan positif proton dalam atom itu. Saat elektron hilang, atom mendapat muatan positif sedangkan ketika elektron diperoleh, atom mendapat muatan negatif bersih. Ini terjadi karena ketidakseimbangan muatan positif proton dalam nukleus. Muatan ini dapat diberikan sebagai keadaan oksidasi atom itu.
Keadaan oksidasi atom dilambangkan dengan bilangan bulat dengan tanda positif (+) atau negatif (-). Tanda ini menunjukkan apakah atom telah mendapatkan atau kehilangan elektron. Seluruh bilangan memberikan jumlah elektron yang telah dipertukarkan antara atom.
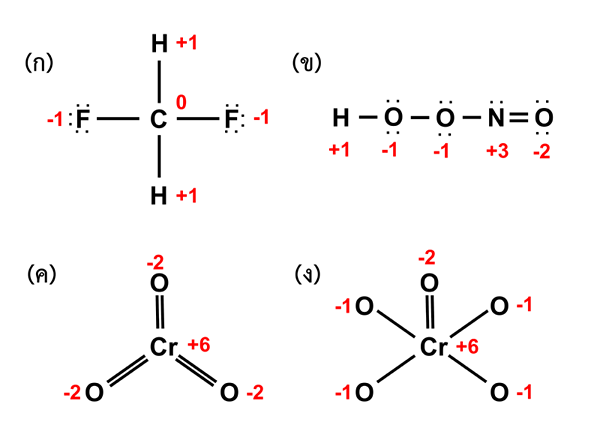
Gambar 02: Keadaan oksidasi dari senyawa yang berbeda
Penentuan keadaan oksidasi atom
Keadaan oksidasi atom tertentu dapat ditentukan dengan menggunakan aturan berikut.
- Keadaan oksidasi elemen netral selalu nol. Contoh: keadaan oksidasi natrium (NA) adalah nol.
- Total muatan senyawa harus sama dengan jumlah muatan masing -masing atom yang ada di senyawa itu. Contoh: Total muatan KCL adalah nol. Maka tuduhan K dan CL harus +1 dan -1.
- Keadaan oksidasi elemen grup 1 selalu +1. Elemen grup 1 adalah lithium, natrium, kalium, rubidium, cesium dan francium.
- Keadaan oksidasi elemen kelompok 2 selalu +2. Elemen grup 2 adalah berilium, magnesium, kalsium, strontium, barium dan radium.
- Muatan negatif diberikan pada atom yang memiliki elektronegativitas yang lebih tinggi daripada atom lain yang terikat padanya.
- Keadaan oksidasi hidrogen selalu +1 kecuali saat hidrogen terikat pada logam grup 1.
- Keadaan oksidasi oksigen adalah -2 kecuali saat itu dalam bentuk peroksida atau superoksida.
Apa perbedaan antara kovalensi dan keadaan oksidasi?
Keadaan kovalensi vs oksidasi | |
| Kovalensi adalah jumlah ikatan kovalen yang dapat dibentuk oleh atom dengan atom lainnya. | Keadaan oksidasi atom adalah jumlah elektron yang hilang, diperoleh atau dibagikan oleh atom dengan atom lain. |
| Muatan listrik | |
| Kovalensi tidak menunjukkan muatan listrik dari sebuah atom. | Keadaan oksidasi memberikan muatan listrik dari sebuah atom. |
| Ikatan Kimia | |
| Kovalensi menunjukkan jumlah ikatan kimia (ikatan kovalen) yang dapat dimiliki atom tertentu. | Keadaan oksidasi tidak memberikan perincian tentang ikatan kimia yang dibentuk oleh atom. |
| Keadaan elemen | |
| Kovalensi elemen murni tergantung pada jumlah elektron yang ada di cangkang elektron terluar dari atom dari elemen tersebut. | Keadaan oksidasi elemen murni selalu nol. |
Ringkasan - Kovalensi vs Keadaan oksidasi
Keadaan kovalensi dan oksidasi atom menggambarkan sifat kimia atom dalam senyawa kimia. Perbedaan antara kovalensi dan keadaan oksidasi adalah bahwa kovalensi atom adalah jumlah ikatan kovalen yang dapat dibentuk atom sedangkan keadaan oksidasi atom adalah jumlah elektron yang hilang atau diperoleh dengan atom ketika membentuk ikatan kimia.
Referensi:
1.“Kovalensi.”Kamus.com. Tersedia disini
2.“Keadaan oksidasi.”Wikipedia, Wikimedia Foundation, 5 Mar. 2018. Tersedia disini
3.“Struktur kimia-kovalen dan molekul."Com. Tersedia disini
Gambar milik:
1.'Covalent Bonds'by Bruceblaus - karya sendiri, (CC BY -SA 4.0) Via Commons Wikimedia
2.'Tugas Negara Oksidasi' oleh Saranphong Yimklan - Pekerjaan Sendiri, (Domain Publik) Via Commons Wikimedia


