Perbedaan antara substitusi radikal bebas dan penambahan radikal bebas
Itu Perbedaan utama antara substitusi radikal bebas dan penambahan radikal bebas adalah bahwa substitusi radikal bebas melibatkan penggantian kelompok fungsional dengan kelompok fungsional lain, sedangkan penambahan radikal bebas melibatkan penambahan kelompok fungsional baru ke molekul.
Radikal bebas bisa berupa atom, molekul, atau ion yang terdiri dari elektron valensi yang tidak berpasangan. Ada dua jenis utama reaksi radikal: substitusi radikal bebas dan reaksi penambahan radikal bebas.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu radikal bebas
3. Apa itu substitusi radikal bebas
4. Apa itu penambahan radikal bebas
5. Substitusi radikal bebas vs penambahan radikal bebas dalam bentuk tabel
6. Ringkasan - Substitusi Radikal Bebas vs Penambahan Radikal Bebas
Apa itu radikal bebas?
Radikal bebas dapat berupa atom, molekul, atau ion yang terdiri dari elektron valensi yang tidak berpasangan. Biasanya, elektron yang tidak berpasangan ini dapat membuat radikal bebas sangat reaktif secara kimia; Namun, mungkin ada beberapa pengecualian. Karena reaktivitasnya yang tinggi, sebagian besar radikal bebas cenderung dimerisasi secara spontan. Oleh karena itu, mereka memiliki masa hidup yang sangat singkat.
Apa itu substitusi radikal bebas?
Substitusi radikal bebas adalah jenis reaksi substitusi yang melibatkan radikal bebas sebagai perantara reaktif. Zat antara reaktif berumur pendek, energi tinggi, dan molekul reaktif tinggi. Molekul -molekul ini terbentuk selama reaksi kimia yang cenderung dikonversi dengan cepat menjadi molekul yang lebih stabil. Selain itu, reaksi substitusi adalah jenis reaksi kimia di mana satu kelompok fungsional dalam senyawa kimia cenderung digantikan oleh kelompok fungsional lain.

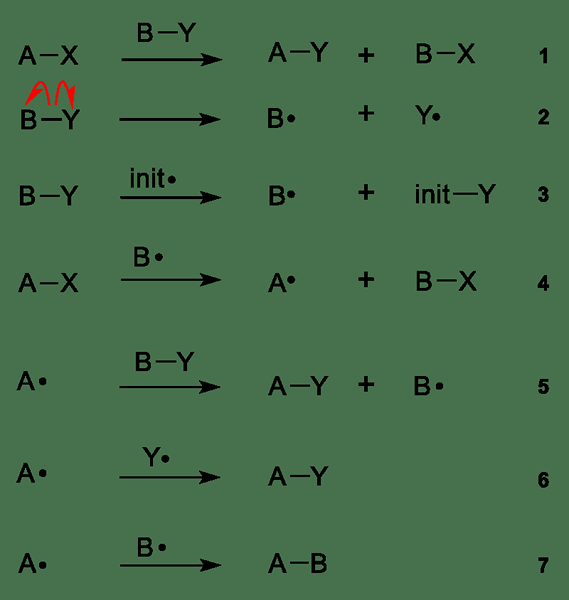
Gambar 01: Langkah berbeda dalam reaksi radikal bebas
Gambar di atas menunjukkan langkah -langkah reaksi radikal bebas secara umum; Langkah 2 dan 3 dinamai reaksi inisiasi di mana bentuk radikal bebas melalui homolisis. Homolisis dapat dicapai dengan menggunakan cahaya panas atau UV dan menggunakan inisiator radikal, e.G. peroksida organik, senyawa azo, dll. Langkah terakhir 6 dan 7 secara kolektif dinamai sebagai penghentian; Di sini, radikal cenderung bergabung kembali dengan spesies radikal lainnya. Namun, radikal terkadang bereaksi lebih lanjut di mana perambatan terjadi. Propagasi diberikan dari langkah 4 dan 5 pada gambar di atas.
Beberapa contoh reaksi substitusi radikal termasuk deoksigenasi Barton-McCombie, reaksi Wohl-Ziegler, reaksi Dowd-Beckwith, dll.
Apa itu penambahan radikal bebas?
Penambahan radikal bebas adalah jenis reaksi penambahan di mana kelompok fungsional ditambahkan ke senyawa melalui perantara reaktif radikal bebas. Jenis penambahan ini dapat terjadi antara spesies radikal dan non-radikal atau antara dua spesies radikal. Langkah -langkah dasar penambahan radikal bebas termasuk inisiasi, perambatan rantai, dan penghentian rantai.
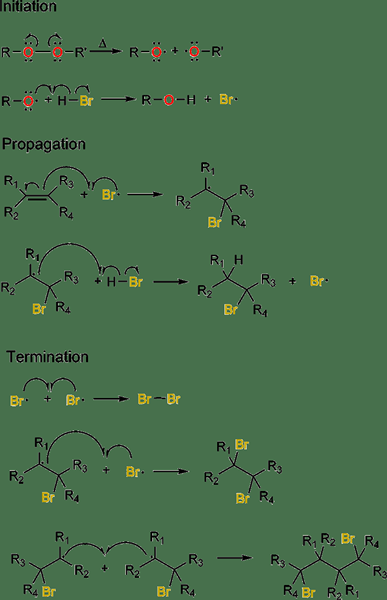
Gambar 02: Penambahan Radikal HBR pada Alkena
Selama proses inisiasi, inisiator radikal digunakan untuk inisiasi, di mana spesies radikal terbentuk dari prekursor non-radikal. Selama proses propagasi rantai, radikal bebas cenderung bereaksi dengan spesies non-radikal untuk menghasilkan spesies radikal baru. Langkah terakhir adalah penghentian rantai, di mana kedua radikal bereaksi satu sama lain, menciptakan spesies non-radikal. Contoh umum dari jenis reaksi ini termasuk arilasi meerwein.
Biasanya, reaksi penambahan radkal bebas didasarkan pada reagen yang memiliki ikatan lemah sehingga mereka dapat menjalani homolisis yang membentuk spesies radikal. Ketika ada ikatan yang kuat, mekanisme reaksi menjadi berbeda dari reaksi penambahan radikal bebas biasa.
Apa perbedaan antara substitusi radikal bebas dan penambahan radikal bebas?
Radikal bebas dapat berupa atom, molekul, atau ion yang terdiri dari elektron valensi yang tidak berpasangan. Perbedaan utama antara substitusi radikal bebas dan penambahan radikal bebas adalah bahwa substitusi radikal bebas melibatkan penggantian kelompok fungsional dengan kelompok fungsional lain, sedangkan penambahan radikal bebas melibatkan penambahan kelompok fungsional baru ke dalam molekul.
Gambar berikut mencantumkan perbedaan antara substitusi radikal bebas dan penambahan radikal bebas dalam bentuk tabel untuk perbandingan berdampingan.
Ringkasan -Substitusi Radikal Bebas vs Penambahan Radikal Bebas
Radikal bebas bisa berupa atom, molekul atau ion yang terdiri dari elektron valensi yang tidak berpasangan. Perbedaan utama antara substitusi radikal bebas dan penambahan radikal bebas adalah bahwa substitusi radikal bebas melibatkan penggantian kelompok fungsional dengan kelompok fungsional lain, sedangkan penambahan radikal bebas melibatkan penambahan kelompok fungsional baru ke dalam molekul.
Referensi:
1. “Apa itu substitusi radikal bebas?" Libreteks Kimia, Libretexts, 13 September. 2020, tersedia di sini.
Gambar milik:
1. “FreeradicalSubstitusigeneraldescr (1)” oleh V8Rik di Inggris Wikipedia (CC BY-SA 3.0) Via Commons Wikimedia
2. "Peroxide Free-Radical-Addition" oleh Bryn C-ditransfer dari EN (domain publik) melalui Commons Wikimedia


