Perbedaan antara ikatan hidrogen antarmolekul dan intramolekul
Perbedaan utama - antarmolekul vs ikatan hidrogen intramolekul
Ikatan hidrogen adalah bentuk gaya tarik antara molekul kutub tertentu. Ini adalah jenis ikatan yang lemah dari ikatan ionik atau kovalen, tetapi merupakan gaya tarik yang kuat bila dibandingkan dengan gaya dipol-dipol dan gaya van der Waal. Ikatan hidrogen terbentuk jika molekul polar memiliki atom elektronegatif yang kuat yang memiliki pasangan elektron tunggal (yang dapat bertindak sebagai donor elektron) yang terikat pada atom hidrogen (akseptor elektron). Karena atom yang sangat elektronegatif dapat menarik ikatan elektron par ke arah dirinya sendiri daripada atom hidrogen, atom hidrogen mendapatkan muatan positif parsial, menghasilkan pemisahan muatan yang kuat. Oleh karena itu, ikatan ikatan hidrogen umum yang membentuk ikatan kimia adalah ikatan O-H, ikatan N-H, dan ikatan F-H. Ada dua bentuk ikatan hidrogen yang dapat dibentuk; Ikatan hidrogen antarmolekul yang terjadi antara molekul kutub dan ikatan hidrogen intramolekul yang terjadi dalam molekul tunggal yang sama. Itu perbedaan utama Antara ikatan hidrogen antar molekul dan intramolekul adalah itu Ikatan hidrogen antarmolekul terjadi di antara dua molekul sedangkan ikatan hidrogen intramolekul terjadi dalam molekul tunggal.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa ikatan hidrogen antar molekul
3. Apa ikatan hidrogen intramolekul
4. Perbandingan berdampingan - ikatan hidrogen intramolekul vs antar molekul dalam bentuk tabel
5. Ringkasan
Apa ikatan hidrogen antar molekul?
Ikatan hidrogen antarmolekul terjadi antara molekul terpisah dalam suatu zat. Oleh karena itu, donor elektron dan akseptor elektron harus ada dalam dua molekul terpisah. Jika ada donor dan akseptor elektron yang tepat, molekul apa pun dapat membentuk ikatan hidrogen.

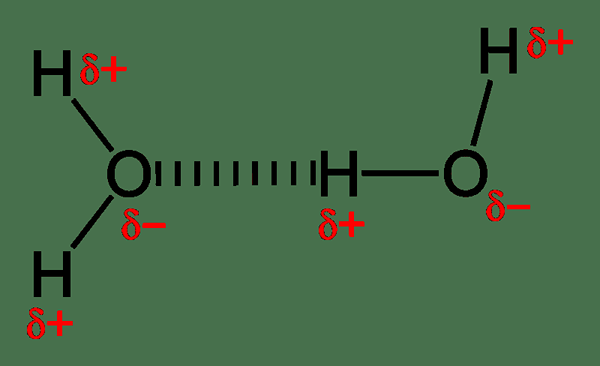
Gambar 01: Ikatan hidrogen antarmolekul dalam molekul air
Contoh umum untuk molekul yang dapat membentuk ikatan hidrogen antarmolekul adalah molekul air (H2HAI).Ikatan hidrogen di antara molekul air menyebabkan pembentukan struktur kaku saat air cair diubah menjadi es padat.
Apa ikatan hidrogen intramolekul?
Ikatan hidrogen intramolekul adalah yang terjadi dalam molekul tunggal.Jenis ikatan hidrogen ini muncul ketika dua kelompok fungsional yang mampu membentuk ikatan hidrogen satu sama lain hadir dalam molekul tunggal yang sama. Ini berarti donor elektron dan akseptor elektron harus hadir dalam molekul yang sama.
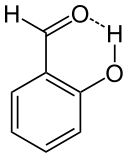
Gambar 02: Ikatan hidrogen intramolekul dalam salycylaldehyde
Selain itu, kedua kelompok fungsional ini harus diposisikan cukup dekat untuk ikatan hidrogen ini. Contoh paling umum dari molekul yang menunjukkan jenis ikatan hidrogen ini adalah salycylaldehyde (c7H6HAI2).
Apa perbedaan antara ikatan hidrogen antarmolekul dan intramolekul?
Ikatan hidrogen intramolekul antarmolekul vs | |
| Ikatan hidrogen antarmolekul terjadi antara molekul terpisah dalam suatu zat. | Ikatan hidrogen intramolekul adalah yang terjadi dalam satu molekul tunggal. |
| Komponen | |
| Ikatan hidrogen antarmolekul terbentuk di antara dua molekul. | Ikatan hidrogen intramolekul terbentuk di antara molekul terpisah. |
Ringkasan -Antarmolekul vs ikatan hidrogen intramolekul
Ikatan hidrogen adalah bentuk interaksi dipol-dipol. Tapi itu adalah tipe ikatan yang lemah. Ada dua bentuk ikatan hidrogen sebagai ikatan hidrogen antar molekul dan intramolekul. Perbedaan antara ikatan hidrogen antarmolekul dan intramolekul adalah bahwa ikatan hidrogen antarmolekul terjadi di antara dua molekul sedangkan ikatan hidrogen intramolekul terjadi dalam molekul tunggal.
Referensi:
1."Ikatan hidrogen.”Kimia Libretexts, Libretexts, 21 Juli 2016. Tersedia disini
2.“Ikatan hidrogen.”Wikipedia, Wikimedia Foundation, 14 Mar. 2018. Tersedia disini
Gambar milik:
1.'Hidrogen-Bonding-in-Water-2D' (Domain Publik) melalui Commons Wikimedia
2.'Salicylaldehyd Wasserstofffbrücke'by Neurotiker ⇌ - karya sendiri, (domain publik) via commons wikimedia


