Perbedaan antara redoks intramolekul dan reaksi redoks yang tidak proporsional
Itu perbedaan utama Antara redoks intramolekul dan reaksi redoks yang tidak proporsional adalah itu Reaksi redoks intramolekul terjadi ketika molekul tunggal mengalami oksidasi dan pengurangan dalam elemen kimia yang sama atau elemen kimia yang berbeda sedangkan reaksi redoks yang tidak proporsional melibatkan oksidasi dan pengurangan elemen kimia yang sama dalam substrat tunggal.
Reaksi redoks intramolekul dan reaksi redoks yang tidak proporsional adalah dua jenis reaksi kimia anorganik di mana reaksi oksidasi dan reduksi terjadi sejajar satu sama lain. Kedua reaksi kimia ini melibatkan oksidasi dan pengurangan setengah reaksi yang terjadi dalam senyawa kimia yang sama/ dalam molekul substrat tunggal. Kedua jenis berbeda satu sama lain sesuai dengan elemen kimia di mana setengah reaksi ini terjadi.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa reaksi redoks intramolekul
3. Apa reaksi redoks yang tidak proporsional
4. Perbandingan berdampingan - Redoks intramolekul vs reaksi redoks yang tidak proporsional dalam bentuk tabel
5. Ringkasan
Apa reaksi redoks intramolekul?
Reaksi redoks intramolekul adalah reaksi kimia yang melibatkan substrat tunggal di mana oksidasi dan reduksi terjadi pada elemen kimia yang sama atau dalam dua elemen kimia yang berbeda. Dengan kata lain, dalam beberapa reaksi redoks intramolekul, oksidasi dan reduksi terjadi pada elemen kimia yang sama sementara dalam reaksi redoks intramolekul lainnya, oksidasi dan reduksi terjadi pada dua elemen kimia yang berbeda yang berada dalam molekul yang sama. Jika oksidasi dan reduksi terjadi pada elemen kimia yang sama, maka kami menyebutkannya sebagai disproporsional.

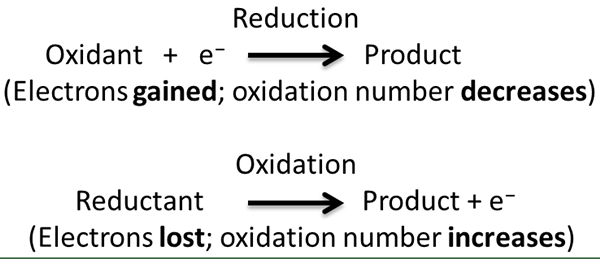
Gambar 01: Proses kimia reaksi redoks
Apa reaksi redoks yang tidak proporsional?
Reaksi redoks yang tidak proporsional adalah reaksi kimia di mana oksidasi dan reduksi terjadi pada elemen kimia yang sama dari molekul substrat tunggal. Dalam jenis reaksi ini, molekul substrat tunggal bekerja dua arah, mengoksidasi dan mengurangi setengah reaksi. Di sini, bagian dari molekul mengalami oksidasi sementara bagian lain dari molekul mengalami pengurangan; Namun, kedua bagian molekuler ini melibatkan elemen kimia yang sama di mana oksidasi atau reduksi terjadi. Contohnya adalah sebagai berikut:
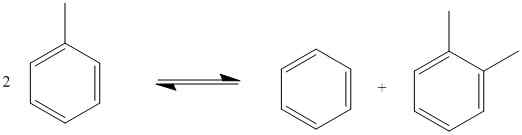
Gambar 02: Contoh reaksi redoks yang tidak proporsional
Contoh umum lain dari jenis reaksi kimia ini adalah disproporsional atom oksigen dalam hidrogen peroksida, molekul H2O2. Di sini, oksigen dalam molekul hidrogen peroksida mengalami oksidasi untuk membentuk gas oksigen, dan molekul yang sama mengalami pengurangan untuk membentuk molekul air.
Apa perbedaan antara redoks intramolekul dan reaksi redoks yang tidak proporsional?
Reaksi redoks adalah reaksi kimia di mana reaksi setengah oksidasi dan pengurangan setengah reaksi terjadi sejajar satu sama lain. Perbedaan utama antara redoks intramolekul dan reaksi redoks yang tidak proporsional adalah bahwa reaksi redoks intramolekul terjadi ketika molekul dua zat yang berbeda bereaksi satu sama lain sedangkan reaksi redoks yang tidak proporsional melibatkan oksidasi dan reduksi molekul tunggal tunggal.
Disproporsional C6H2(TIDAK2)3Ch3 untuk membentuk n2 Melalui reduksi dan C melalui oksidasi adalah contoh reaksi redoks intramolekul sementara disproporsional atom oksigen dalam molekul hidrogen peroksida adalah contoh reaksi redoks yang tidak proporsional.
Infografis di bawah ini merangkum perbedaan antara redoks intramolekul dan reaksi redoks yang tidak proporsional dalam bentuk tabel untuk perbandingan berdampingan.

Ringkasan -Redoks intramolekul vs reaksi redoks yang tidak proporsional
Reaksi redoks adalah reaksi kimia yang melibatkan reaksi oksidasi dan reduksi yang terjadi sejajar satu sama lain. Perbedaan utama antara redoks intramolekul dan reaksi redoks yang tidak proporsional adalah bahwa reaksi redoks intramolekul terjadi ketika molekul dua zat yang berbeda bereaksi satu sama lain sedangkan reaksi redoks yang tidak proporsional melibatkan oksidasi dan reduksi molekul tunggal tunggal.
Referensi:
1. Mott, Vallerie. “Jenis reaksi redoks." Lumen - Pengantar Kimia, Tersedia disini.
2. Helmenstine, Anne Marie. “Definisi Disproporsional dalam Kimia." Thoughtco, Tersedia disini.


