Perbedaan antara isotop dan isomer

Isotop vs isomer
Ada variasi antara atom yang berbeda. Juga, ada variasi dalam elemen yang sama. Isotop adalah contoh perbedaan dalam satu elemen.
Molekul atau ion yang memiliki formula molekul yang sama dapat ada dengan cara yang berbeda tergantung pada perintah ikatan, perbedaan distribusi muatan, cara mereka mengatur diri mereka sendiri di ruang dll; Ini dikenal sebagai isomer.
Isotop
Atom dari elemen yang sama bisa berbeda. Atom yang berbeda dari elemen yang sama ini disebut isotop. Mereka berbeda satu sama lain dengan memiliki jumlah neutron yang berbeda. Karena nomor neutron berbeda, jumlah massa mereka juga berbeda. Namun, isotop dari elemen yang sama memiliki jumlah proton dan neutron yang sama. Isotop yang berbeda hadir dalam berbagai jumlah, dan ini diberikan sebagai nilai persentase yang disebut kelimpahan relatif. Misalnya, hidrogen memiliki tiga isotop sebagai protium, deuterium dan tritium. Jumlah neutron dan kelimpahan relatif mereka adalah sebagai berikut.
1H - Tidak ada neutron, kelimpahan relatif 99.985%
2H- satu neutron, kelimpahan relatif adalah 0.015%
3H- Dua neutron, kelimpahan relatif adalah 0%
Jumlah neutron yang dapat ditahan oleh nukleus berbeda dari elemen ke elemen. Di antara isotop ini, hanya beberapa yang stabil. Misalnya, oksigen memiliki tiga isotop stabil, dan timah memiliki sepuluh isotop stabil. Sebagian besar waktu, elemen sederhana memiliki nomor neutron yang sama dengan nomor proton tetapi, dalam elemen berat, lebih banyak neutron daripada proton. Jumlah neutron penting untuk menyeimbangkan stabilitas inti. Ketika inti terlalu berat, mereka menjadi tidak stabil dan, oleh karena itu, isotop itu menjadi radioaktif. Misalnya, 238 U memancarkan radiasi dan meluruh ke inti yang jauh lebih kecil. Isotop mungkin memiliki sifat yang berbeda karena massa yang berbeda. Misalnya, mereka mungkin memiliki putaran yang berbeda, sehingga spektrum NMR mereka berbeda. Namun, jumlah elektron mereka serupa sehingga menimbulkan perilaku kimia yang serupa.
Spektrometer massa dapat digunakan untuk mendapatkan informasi tentang isotop. Ini memberikan jumlah isotop yang dimiliki suatu elemen, kelimpahan dan massa relatif mereka.
Isomer
Isomer adalah senyawa yang berbeda dengan formula molekul yang sama. Ada berbagai jenis isomer. Isomer dapat dibagi menjadi dua kelompok sebagai isomer konstitusional dan isomer stereo. Isomer konstitusional adalah isomer di mana konektivitas atom berbeda dalam molekul. Butana adalah alkana paling sederhana untuk menunjukkan isomerisme konstitusional. Butana memiliki dua isomer konstitusional, butana itu sendiri dan isobutene.
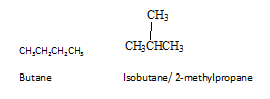
Dalam stereo-isomer atom terhubung dalam urutan yang sama, tidak seperti isomer konstitusional. Stereoisomer hanya berbeda dalam pengaturan atom mereka di luar angkasa. Stereoisomer dapat terdiri dari dua jenis, enansiomer dan diastereomer. Diastereomer adalah stereoisomer yang molekulnya bukan gambar cermin satu sama lain. Isomer trans cis 1,2-dikloroeten adalah diastereomer. Enantiomer adalah stereoisomer yang molekulnya adalah gambar cermin yang tidak dapat diawali satu sama lain. Enantiomer hanya terjadi dengan molekul kiral. Molekul kiral didefinisikan sebagai yang tidak identik dengan gambar cerminnya. Oleh karena itu, molekul kiral dan gambar cerminnya adalah enansiomer satu sama lain. Misalnya, molekul 2-butanol adalah kiral, dan gambar cerminnya adalah enansiomer.
| Apa perbedaan antara Isotop dan isomer? • Isotop adalah atom yang berbeda dari elemen yang sama. Isomer adalah senyawa yang berbeda dengan formula molekul yang sama. • Isotop berbeda satu sama lain karena jumlah neutron, sedangkan isomer berbeda satu sama lain karena pengaturan atom. • Isotop dari satu elemen memiliki perilaku kimia yang sama, tetapi sifat fisiknya mungkin berbeda. Isomer dengan formula kimia yang sama memiliki perbedaan dalam sifat kimia dan fisik (kecuali beberapa isomer). |


