Perbedaan antara hukum komposisi konstan dan hukum proporsi berganda
Itu perbedaan utama antara hukum komposisi konstan dan hukum proporsi ganda adalah itu Menurut hukum komposisi konstan, proporsi sampel yang sama selalu terdiri dari proporsi unsur yang sama dengan massa, sedangkan menurut hukum proporsi berganda, jika dua elemen mengikat satu sama lain membentuk lebih dari satu senyawa kimia, maka rasioo tersebut Antara massa elemen kedua yang digabungkan dengan massa tetap dari elemen pertama memiliki rasio bilangan bulat kecil.
Hukum komposisi konstan dan hukum proporsi ganda adalah teori dalam kimia fisik yang digunakan untuk menjelaskan stoikiometri dalam kimia. Stoikiometri adalah ukuran dari jumlah relatif reaktan dan produk dalam reaksi kimia.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa Hukum Komposisi Konstan
3. Apa hukum proporsi ganda
4. Perbandingan Berdampingan - Hukum Komposisi Konstan vs Hukum Proporsi Berbagai dalam Bentuk Tabel
5. Ringkasan
Apa Hukum Komposisi Konstan?
Hukum komposisi konstan menyatakan sampel senyawa akan selalu mengandung proporsi elemen yang sama dengan massa. Kita dapat menyebutkan hukum ini sebagai hukum proporsi yang pasti juga. Undang -undang ini menjelaskan bahwa senyawa yang diberikan akan selalu mengandung elemen yang sama dalam proporsi yang sama dengan massa.
Misalnya, baik itu air keran atau air laut, molekul air akan selalu mengandung elemen hidrogen dan oksigen dalam proporsi berikut. Formula kimia molekul air adalah H2O, dan massa molar molekul ini adalah 18 g/mol. Oleh karena itu, satu mol air mengandung 18 g H2O. Rasio antara H dan O dalam molekul air adalah 2: 1. Dengan demikian, fraksi massa hidrogen dalam air = (2g / 18g) x 100% = 11.11% dan fraksi massa oksigen = (16g/18g) x 100% = 88.89%. Fraksi ini konstan dan tidak berubah sesuai dengan sumber air dan metode pemisahan.
Hukum komposisi konstan tergantung pada fakta bahwa atom apa pun dari elemen yang sama (atom yang memiliki angka atom yang sama) mirip satu sama lain. Mempertimbangkan contoh di atas, asumsinya adalah bahwa atom hidrogen mirip dengan atom hidrogen lain dan sebaliknya. Tapi mungkin ada beberapa pengecualian. E.G. Komposisi isotop suatu elemen dapat bervariasi tergantung pada sumbernya. Oleh karena itu, stoikiometri menunjukkan variasi tergantung pada sumber elemen.
Apa hukum proporsi ganda?
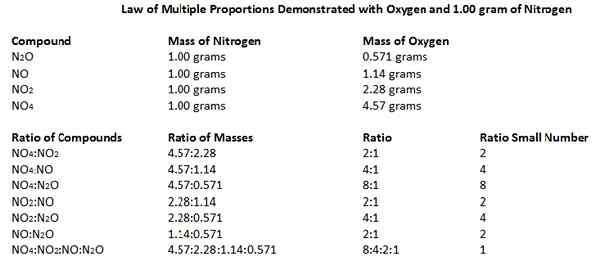
Hukum proporsi berganda menyatakan bahwa ketika dua elemen bergabung satu sama lain untuk membentuk lebih dari satu senyawa, maka bobot satu elemen yang bergabung dengan berat yang tetap dari yang lain berada dalam rasio bilangan bulat kecil kecil.

Kita dapat menyebut hukum ini juga hukum Dalton karena hukum tersebut dikembangkan oleh John Dalton pada tahun 1803. Mari kita pahami undang -undang ini menggunakan contoh.
Oksida nitrogen terdiri dari atom nitrogen dan oksigen. Kita dapat mengidentifikasi lima oksida nitrogen yang berbeda yang ada: n2O, tidak, n2HAI3, TIDAK2 dan N2HAI5. Mempertimbangkan rasio massa N dan O dalam senyawa oksida ini, 14 gram atom nitrogen bergabung dengan 8, 16, 24, 32 dan 40 gram oksigen sesuai dengan rasio massa, masing -masing. Jika kita mengambil angka -angka ini sebagai bilangan bulat kecil, maka rasio dapat diberikan sebagai 1: 1, 1: 2, 1: 3, 1: 4 dan 1: 5.
Apa perbedaan antara hukum komposisi konstan dan hukum proporsi ganda?
Menurut hukum komposisi konstan, proporsi sampel yang sama selalu terdiri dari proporsi elemen yang sama dengan massa, sedangkan menurut hukum proporsi berganda, jika dua elemen mengikat satu sama lain membentuk lebih dari satu senyawa kimia, maka rasio tersebut Antara massa elemen kedua yang digabungkan dengan massa tetap dari elemen pertama memiliki rasio bilangan bulat kecil. Jadi, ini adalah perbedaan utama antara hukum komposisi konstan dan hukum proporsi ganda.

Ringkasan -Hukum Komposisi Konstan vs Hukum Berbagai Proporsi
Menurut hukum komposisi konstan, proporsi sampel yang sama selalu terdiri dari proporsi elemen yang sama dengan massa, sedangkan menurut hukum proporsi berganda, jika dua elemen mengikat satu sama lain membentuk lebih dari satu senyawa kimia, maka rasio tersebut Antara massa elemen kedua yang digabungkan dengan massa tetap dari elemen pertama memiliki rasio bilangan bulat kecil. Dengan demikian, ini adalah perbedaan antara hukum komposisi konstan dan hukum proporsi ganda.
Referensi:
1. Helmenstine, Anne Marie. “Hukum Komposisi Konstan dalam Kimia."Thoughtco, Aug. 26, 2020, tersedia di sini.
Gambar milik:
1. “Demonstrasi Hukum Berbagai Proporsi” oleh Kenji Agari - Karya Sendiri (CC BY -SA 3.0) Via Commons Wikimedia


