Perbedaan antara lisin dan L-lisin
Perbedaan Utama - Lisin vs L -Lysine
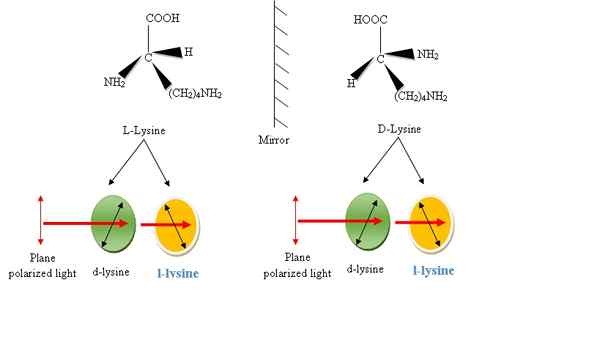
Lisin dan L-lisin keduanya adalah jenis asam amino, berbagi sifat fisik yang sama, ada beberapa perbedaan di antara mereka. Itu Perbedaan utama antara lisin dan L-lisin berada dalam kemampuan untuk memutar cahaya bidang terpolarisasi bidang. Lisin adalah asam α-amino esensial yang aktif secara biologis. Itu dapat terjadi dalam dua bentuk isomer karena kemungkinan membentuk dua enansiomer yang berbeda di sekitar atom karbon kiral. Ini dikenal sebagai L- dan D-form, analog dengan konfigurasi kidal dan kidal. L-dan D-form ini dikatakan aktif secara optik dan memutar cahaya terpolarisasi bidang dalam arti yang berbeda; searah jarum jam atau berlawanan arah jarum jam. Jika cahaya berputar lisin berlawanan arah jarum jam, maka cahaya menunjukkan levorotation, dan dikenal sebagai L-lisin. Namun, harus dicatat dengan cermat di sini bahwa label D- dan L-dari isomer tidak sama dengan label D- dan L-.
Apa itu lisin?
Lisin adalah An asam amino esensial yang tidak disintesis di tubuh kita dan harus dipasok oleh diet biasa. Oleh karena itu, lisin adalah asam amino esensial untuk manusia. Ini adalah senyawa organik yang penting secara biologis yang terdiri dari amina (-NH2) dan asam karboksilat (-cooh) gugus fungsional dengan formula kimia NH2-(Ch2)4-CH (NH2) -Cooh. Elemen kunci lisin adalah karbon, hidrogen, oksigen, dan nitrogen. Dalam biokimia, asam amino yang memiliki gugus amina dan asam karboksilat yang melekat pada atom karbon pertama (alpha-) dikenal sebagai Asam α-amino. Dengan demikian lisin juga dianggap sebagai asam amino amino. Struktur lisin diberikan pada Gambar 1.
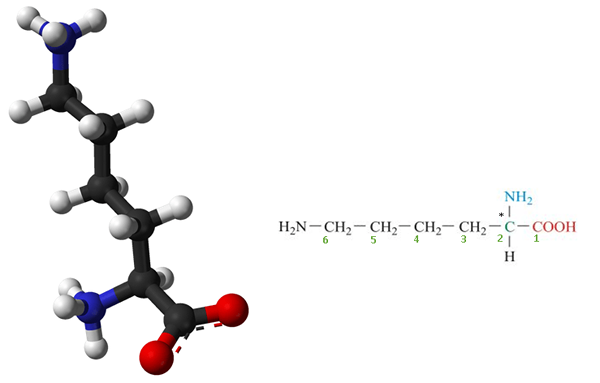
Gambar 1: Struktur molekul lisin (* atom karbon adalah atom karbon kiral atau asimetris dan juga mewakili atom alfa-karbon)
Lisin bersifat dasar karena mengandung dua gugus amino dasar dan satu gugus asam karboksilat asam. Oleh karena itu, ia juga membentuk ikatan hidrogen yang luas karena adanya dua kelompok amino. Sumber lisin yang baik adalah sumber hewan kaya protein seperti telur, daging merah, domba, babi, dan unggas, keju, dan ikan tertentu (seperti cod dan sarden). Lisin juga Kaya protein nabati Seperti kedelai, kacang, dan kacang polong. Namun, ini adalah asam amino yang membatasi di sebagian besar biji -bijian sereal tetapi berlimpah di sebagian besar pulsa dan kacang -kacangan.
Apa itu l-lysine?
Lisin memiliki empat kelompok yang berbeda di sekitar 2nd karbon, dan itu Struktur asimetris. Juga, lisin adalah asam amino aktif secara optik karena adanya atom karbon asimetris atau kiral ini. Dengan demikian, lisin dapat membuat stereoisomer yang merupakan molekul isomer yang memiliki formula molekul yang sama, tetapi berbeda dalam orientasi tiga dimensi atom mereka di ruang angkasa. Enantiomer adalah dua stereoisomer yang berhubungan satu sama lain dengan refleksi atau mereka adalah gambar cermin satu sama lain yang tidak dapat dituntun. Lisin tersedia dalam dua bentuk enansiomer yang dikenal sebagai L- dan D- dan enansiomer lisin diberikan pada Gambar 2.

Gambar 2: Enantiomer asam amino lisin. Kelompok-kelompok COOH, H, R dan NH2 diatur di sekitar atom C dengan cara searah jarum jam, enansiomer disebut L-form dan D-form sebaliknya. L- dan D- Hanya merujuk pada pengaturan spasial di sekitar atom karbon dan tidak merujuk pada aktivitas optik. Sementara L- dan D-bentuk molekul kiral memang memutar bidang cahaya terpolarisasi di arah yang berbeda, beberapa bentuk-L (atau D-Forms) memutar cahaya ke kiri (levo atau L-form) dan beberapa di sebelah kanan (Dextro atau D- form). L- dan D-form disebut isomer optik.
L-lisin dan D-lisin adalah enansiomer satu sama lain memiliki sifat fisik yang sama, kecuali untuk arah di mana mereka memutar cahaya terpolarisasi. Mereka memiliki hubungan gambar cermin yang tidak dapat ditumpahkan. Namun, nomenklatur D dan L tidak umum pada asam amino termasuk lisin. Mereka memutar cahaya terpolarisasi bidang dengan besarnya tetapi dalam arah yang berbeda. D dan L-isomer lisin yang memutar bidang terpolarisasi bidang dalam arah searah jarum jam disebut dekstrorotasi atau d-lysine dan yang memutar bidang yang terpolarisasi bidang dalam arah antiklokal disebutkan sebagai laevorotatory atau L-lysine (Gambar 2).
L-lysine adalah Bentuk lisin yang paling stabil. D-lisin adalah bentuk sintetis lisin dan dapat disintesis dari L-lisin dengan racemization. Ini digunakan dalam pemrosesan poli-d-lisin, yang digunakan sebagai bahan pelapis untuk meningkatkan perlekatan sel. L-lisin memainkan peran penting dalam tubuh manusia, dalam penyerapan kalsium, perkembangan protein otot, dan sintesis hormon, enzim, dan antibodi. Secara industri, L-lisin diproduksi oleh proses fermentasi mikroba menggunakan Corynebacterium glutamicum.
Apa perbedaan antara lisin dan l-lisin?
Lisin dan l-lisin memiliki sifat fisik yang sama, kecuali untuk arah di mana mereka memutar cahaya terpolarisasi. Akibatnya, L-lisin mungkin memiliki efek biologis dan sifat fungsional yang secara substansial berbeda. Namun, penelitian yang sangat terbatas telah dilakukan untuk membedakan efek biologis dan sifat fungsional ini. Beberapa perbedaan ini mungkin termasuk,
Mencicipi
L-lysine: L-form asam amino cenderung hambar.
D-lysine: D-Forms asam amino cenderung terasa manis.
Oleh karena itu L-lisin mungkin kurang/tidak lebih manis dari lisin.
Kelimpahan
L-lysine: Lorms L dari asam amino termasuk L-lisin adalah bentuk yang paling berlimpah di alam. Sebagai contoh, sembilan dari sembilan belas asam L-amino yang biasa ditemukan dalam protein adalah dekstrorotasi dan sisanya levorotatory.
D-lysine: Bentuk asam amino yang diamati secara eksperimental ditemukan terjadi sangat jarang.
Referensi: Solomon, T.W. Graham, dan graig b. Fryhle (2004). Kimia Organik (8th ed). Hoboken: John Wiley & Sons, Inc. Everhardus, a. (1984). Stereokimia, dasar untuk omong kosong canggih dalam farmakokinetik dan farmakologi klinis, Jurnal Farmakologi Klinis Eropa, 26, 663-668. Gambar milik: “L-lysine-monocation-from-hydrochloride-dihydrate-x-3d-bola” oleh Ben Mills-pekerjaan sendiri melalui Wikimedia Commons


