Perbedaan antara fraksi mol dan fraksi massa
Perbedaan utama - Fraksi mol vs fraksi massa
Fraksi mol dan fraksi massa adalah istilah yang digunakan untuk mengekspresikan rasio antara berbagai komponen dalam senyawa. Perbedaan utama antara fraksi mol dan fraksi massa adalah bahwa fraksi mol berkaitan dengan mol komponen yang berbeda dari suatu senyawa sedangkan fraksi massa berkaitan dengan massa komponen yang berbeda dalam suatu senyawa. Fraksi mol dapat dikonversi menjadi fraksi massa senyawa yang sama dan sebaliknya.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu fraksi mol
3. Apa itu fraksi massa
4. Kesamaan antara fraksi mol dan fraksi massa
5. Perbandingan berdampingan - fraksi mol vs fraksi massa dalam bentuk tabel
6. Ringkasan
Apa itu fraksi mol?
Fraksi mol adalah rasio antara jumlah komponen dalam campuran yang diekspresikan dengan jumlah mol. Ini adalah rasio antara mol dari konstituen dan jumlah mol dari semua konstituen dalam campuran. Itu bisa diberikan seperti di bawah ini.
Fraksi mol = mol dari konstituen/jumlah mol dari semua konstituen (massa campuran)
Atau
XSaya = nSaya / Ntotal
Fraksi mol dari semua komponen sama dengan 1 karena fraksi mol adalah rasio. Fraksi mol dapat digunakan untuk mengekspresikan persentase mol dengan mengalikan fraksi mol dari 100. Fraksi mol juga dapat disebut jumlah fraksi karena tahi lalat memberikan jumlah konstituen. Fraksi mol tidak satu unit karena merupakan rasio antara tahi lalat (unit dibatalkan).

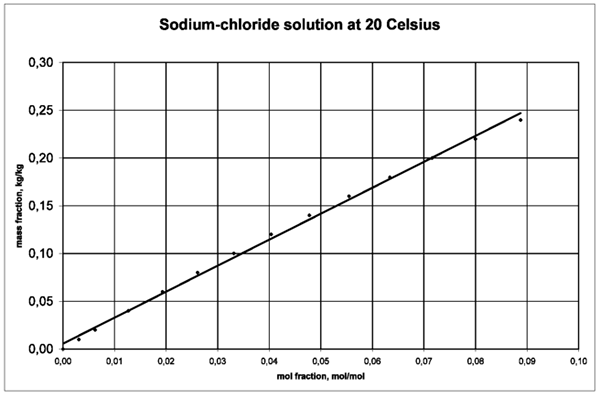
Gambar 01: Kepadatan NaCl sebagai fungsi dari fraksi mol
Perhitungan fraksi mol
Mari kita pertimbangkan masalah sampel untuk memahami apa itu fraksi mol.
Pertanyaan:
Temukan fraksi mol NaCl saat 0.1 mol NaCl dilarutkan dalam 100 gram air murni.
Menjawab:
Jumlah mol air = 100 g / 18 gmol-1
= 5.56 mol
Jumlah mol dari semua konstituen = 0.1 (NaCl) + 5.56 (h2HAI)
= 5.66 mol
Fraksi mol NaCl = 0.1 mol/ 5.66 mol
= 0.018
Apa itu fraksi massa?
Fraksi massa adalah rasio antara massa konstituen dan massa total campuran. Karena ini merupakan rasio antara massa, fraksi massa adalah unit-less (unit dibatalkan). Itu dapat diberikan sebagai persamaan (diberikan di bawah).
Fraksi massa = massa konstituen/jumlah massa dari semua konstituen (massa campuran)
Atau
WSaya = mSaya / Mtotal
Fraksi massa semua komponen sama dengan 1 karena fraksi massa adalah rasio. Fraksi massa komponen individu selalu lebih rendah dari 1. Fraksi massa juga dapat diberikan sebagai persentase massa. Di sini, fraksi massa dikalikan 100. Dalam perhitungan analisis unsur, fraksi massa mengacu pada rasio antara massa elemen kimia dan senyawa. Fraksi massa tidak tergantung pada suhu karena massa tidak berubah ketika suhu berubah.
Perhitungan yang melibatkan fraksi massa
Pertanyaan:
Temukan massa sukrosa dalam larutan sukrosa (500 g) di mana air memiliki fraksi massa 0.65.
Menjawab:
Total massa campuran = 500 g
Fraksi massa air = 0.65
Kemudian fraksi massa sukrosa = 1-0.65 = 0.35
Massa sukrosa = 0.35 x 500g
= 175 g
Apa kesamaan antara fraksi mol dan fraksi massa?
- Kedua istilah rasio ekspres.
- Baik fraksi mol dan fraksi massa adalah istilah tanpa unit.
- Keduanya memberikan nilai yang sama atau kurang dari 1.
- Keduanya tidak tergantung pada perubahan suhu.
Apa perbedaan antara fraksi mol dan fraksi massa?
Fraksi mol vs fraksi massa | |
| Fraksi mol adalah rasio antara mol dari konstituen dan jumlah mol dari semua konstituen dalam campuran. | Fraksi massa adalah rasio antara massa konstituen dan massa total campuran. |
| Komponen | |
| Fraksi mol dihitung menggunakan mol konstituen. | Fraksi massa dihitung menggunakan massa konstituen. |
Ringkasan - fraksi mol vs fraksi massa
Fraksi mol dan fraksi massa digunakan untuk mengekspresikan fraksi relatif dari berbagai konstituen dalam campuran. Keduanya adalah istilah tanpa unit karena rasio memiliki unit yang sama, dan dengan demikian unit dibatalkan. Perbedaan utama antara fraksi mol dan fraksi massa adalah bahwa fraksi mol berkaitan dengan mol komponen yang berbeda dari suatu senyawa sedangkan fraksi massa berkaitan dengan massa komponen yang berbeda dalam suatu senyawa.
Referensi:
1. “Fraksi mol.”Wikipedia, Wikimedia Foundation, 12 Mar. 2018, tersedia di sini.
2. "Fraksi mol", chemsteam, tersedia di sini.
3. “Fraksi massa (kimia).”Wikipedia, Wikimedia Foundation, 3 Mar. 2018, tersedia di sini.
Gambar milik:
1. "Salt Mole Fraction" oleh Jzana - karya sendiri (CC BY -SA 3.0) Via Commons Wikimedia