Perbedaan antara monatomik dan polyatomik
Monatomik vs polyatomic
Jumlah atom yang ada dalam ion tertentu atau molekul adalah apa yang berkontribusi pada perbedaan antara monatomik dan politisomik. Dua kata "mono" dan "poly" memberikan ide umum tentang molekul; "Mono" berarti "lajang" dan "poli" berarti "banyak.”Monatomik mengacu pada ion atau molekul yang memiliki atom tunggal. Polyatomic mengacu pada molekul atau ion yang memiliki dua atom atau lebih. Ada begitu banyak perbedaan fisik dan kimia antara monatomik dan polyatomik karena perbedaan jumlah atom. Umumnya unsur kimia monatomik kurang berlimpah dibandingkan dengan keberadaan molekul politisomik.
Apa itu monatomik?
Kata monatomik berasal dari dua kata "mono" dan "atom," memberikan arti "atom tunggal.Spesies kimia monatomik hanya mengandung satu atom dan mereka stabil bahkan jika ada sendiri. Ini dapat diterapkan pada gas dan ion. Sebagian besar gas mulia ada sebagai spesies kimia monatomik.
Ion Monatomik: Ion -ion ini dibentuk dengan kehilangan (ion positif) atau mendapatkan (ion negatif) elektron.
Ion positif: Na+, K+, Ca2+, AL3+
Ion negatif: Cl-, S2-, Br-, F-
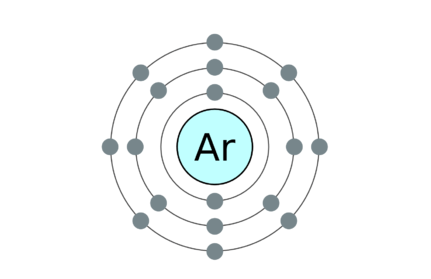
Molekul Monatomik: Gas mulia termasuk dalam kategori ini dan mereka sangat stabil; Oleh karena itu, secara kimia tidak aktif.

18: Argon 2, 8, 8
Apa itu polyatomic?
Kata polyatomik berasal dari dua kata "poli" dan "atom," banyak atom. Itu bisa menjadi atom homogen (o2, HG22+, HAI3, HAI22-) atau kombinasi atom heterogen (CN-, H2JADI4, Clo3-). Sebagian besar molekul dan ion ada sebagai sifat politisomik.
Ion polyatomic: "Ion molekuler" adalah nama lain untuk ion politisomik. Sebagian besar ion polyatomic adalah spesies kimia yang terikat secara kovalen atau kompleks logam.
Ion positif: NH4+, H3HAI+, Ph4+
Ion negatif: Cro42-, BERSAMA32-, Ch3MENDEKUT-, JADI42-, TIDAK3-
Molekul polyatomik: Mereka adalah molekul dengan dua atom atau lebih. Mereka tidak memiliki muatan positif atau negatif. Dengan kata lain, molekul -molekul ini netral secara elektrik. (H2JADI4, Ch3Cooh, na2BERSAMA3, NaCl, c2H4)
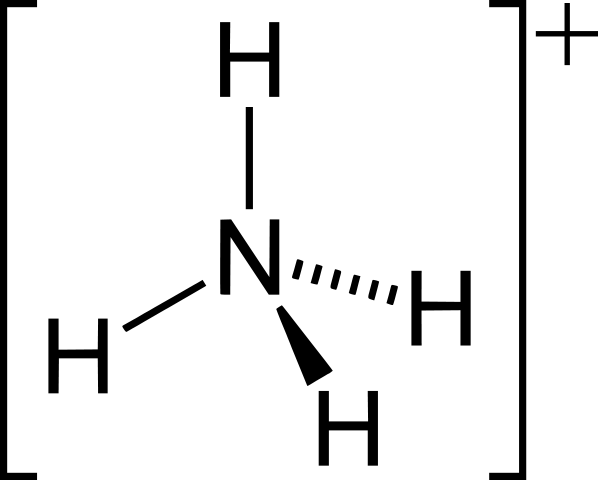
Amonium
Apa perbedaan antara monatomik dan politisomik?
• Jumlah atom:
• Elemen kimia monatomik mengandung Hanya satu atom.
• Senyawa kimia polyatomic memiliki dua atau lebih atom.
• Negara:
• Spesies kimia monatomik dapat berupa ion atau gas inert.
• Beberapa spesies polyatomic adalah ion dan beberapa adalah molekul.
• Properti
• Sebagian besar ion monatomik stabil dalam air.
• Molekul monatomik sangat stabil; Oleh karena itu, secara kimia tidak aktif.
• Sebagian besar ion polyatomic adalah kompleks terikat kovalen atau logam.
• Molekul polyatomic netral secara elektrik.
• Contoh untuk monatomik dan polyatomik:
• Contoh untuk Ion monatomik adalah na+, Ca2+, K+, Al3+ dan fe3+.
• Contoh untuk Molekul monatomik adalah gas mulia. Mereka helium (dia), neon (ne), argon (ar), krypton (kr), xenon (xe) dan radon (ra).
• Contoh untuk ion polyatomic adalah cro42-, BERSAMA32-, NH4+, H3HAI+.
• Contoh untuk Molekul polyatomic adalah kcl, kbro3, C6H5Cooh.
• Ukuran:
• Ukuran spesies kimia monatomik berbeda sesuai dengan cara mereka terbentuk. Misalnya, ketika ion positif terbentuk ukurannya berkurang dan ketika ion negatif terbentuk, ukurannya meningkat dari atom asli. Gas mulia memiliki ukuran terkecil dibandingkan dengan elemen lain dalam periode mereka di tabel periodik.
• Saat senyawa kimia polyatomic terbentuk, ukuran ion polyatomic atau molekul polyatomic menjadi lebih besar dari semua atom asli dalam senyawa. Karena, dua atau lebih atom bergabung untuk membentuk ion /molekul politisomik.
• Membentuk:
• Umumnya molekul monatomik dan ion adalah bola dalam geometri mereka.
• Geometri spesies kimia polyatomic bervariasi tergantung pada jumlah molekul dan pasangan tunggal yang ada dalam molekul. Karena jumlah atom meningkatkan struktur yang lebih kompleks dibentuk untuk mencapai stabilitas.
Gambar milik:
- Argon oleh Greg Robson (CC BY-SA 2.0 UK)
- Ammonium via Wikicommons (domain publik)


