Perbedaan antara nitrit dan nitrogen dioksida
Itu perbedaan utama antara nitrit dan nitrogen dioksida adalah bahwa Nitrit adalah anion sedangkan nitrogen dioksida adalah molekul.
Baik nitrit dan nitrogen dioksida memiliki jumlah atom nitrogen dan oksigen yang sama; satu atom nitrogen dan dua atom oksigen. Bahkan struktur senyawa itu serupa. Tapi, mereka berbeda satu sama lain sesuai dengan muatan listrik yang mereka tanggung atas mereka. Mari kita bahas lebih lanjut tentang mereka.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu nitrit
3. Apa itu nitrogen dioksida
4. Perbandingan berdampingan - nitrit vs nitrogen dioksida dalam bentuk tabel
5. Ringkasan
Apa itu nitrit?
Nitrit adalah anion yang memiliki formula kimia no-2. Senyawa ini memiliki dua ikatan kimia kovalen dengan panjang ikatan yang sama. Selain itu, anion ini adalah ion simetris. Oleh karena itu, ia dapat mengalami oksidasi atau reduksi. Akibatnya, ia dapat bertindak sebagai agen pereduksi dan agen pengoksidasi.

Gambar 01: Struktur ion nitrit
Massa molar dari anion ini adalah 46.01 g/mol. Setelah protonasi, anion ini membentuk asam nitrat yang merupakan asam lemah yang tidak stabil. Anion ini juga dapat membentuk garam dan kompleks koordinasi. Selain itu, ada nitrit organik yang terdiri dari ester asam nitrat.
Apa itu nitrogen dioksida?
Nitrogen dioksida adalah senyawa anorganik yang memiliki formula kimia NO2. Selain itu, ini adalah senyawa netral dengan muatan listrik nol. Massa molar senyawa ini adalah 46.05 g/mol. Itu terjadi sebagai gas yang muncul dalam warna oranye. Namun, ia memiliki bau pedas seperti dalam gas klorin.

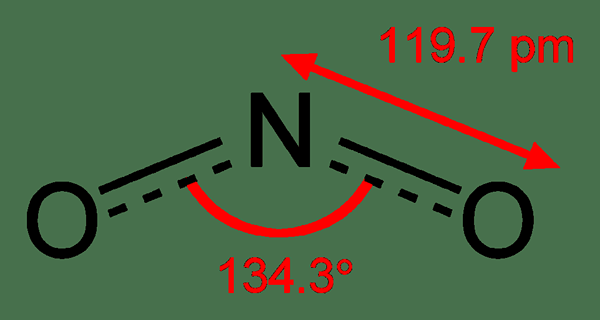
Gambar 02: Struktur kimia nitrogen dioksida
Apalagi senyawa ini adalah paramagnetik. Panjang ikatan antara atom nitrogen dan atom oksigen sama; Panjang ikatan setiap ikatan adalah 119.7 malam. Itu adalah agen pengoksidasi yang kuat. Itu dapat mengalami pengurangan juga.
Apa perbedaan antara nitrit dan nitrogen dioksida?
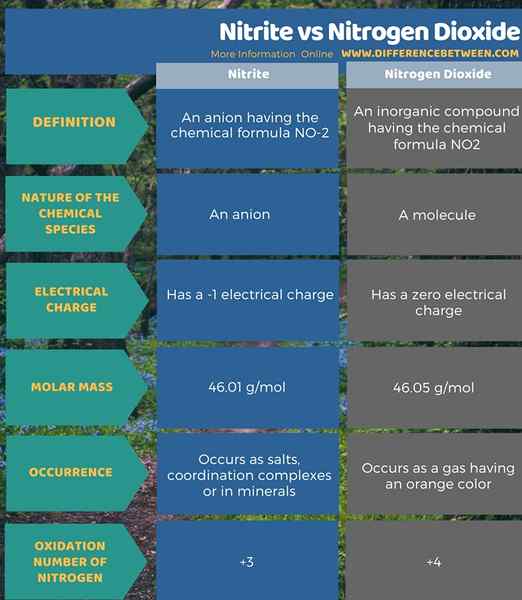
Nitrit adalah anion yang memiliki formula kimia no-2. Itu adalah anion. Massa molar dari anion ini adalah 46.01 g/mol. Atom nitrogen anion ini memiliki keadaan oksidasi +3. Itu dapat membentuk garam, kompleks cordination atau terjadi dalam mineral. Di sisi lain, nitrogen dioksida adalah senyawa anorganik yang memiliki formula kimia NO2, dan merupakan senyawa netral yang memiliki muatan listrik nol. Massa molar senyawa ini adalah 46.05 g/mol. Itu terjadi sebagai gas dengan penampilan warna oranye. Selain itu, atom nitrogen dari molekul ini memiliki keadaan oksidasi +4. Ini adalah perbedaan utama antara nitrit dan nitrogen dioksida.
Ringkasan -nitrit vs nitrogen dioksida
Baik nitrit dan nitrogen dioksida memiliki formula molekul yang sama tetapi mereka memiliki banyak perbedaan seperti yang dinyatakan di atas. Perbedaan utama antara nitrit dan nitrogen dioksida adalah bahwa nitrit adalah anion sedangkan nitrogen dioksida adalah molekul.
Referensi:
1. “Nitrite.”Wikipedia, Wikimedia Foundation, 3 Juli 2018. Tersedia disini
2. "Nitrogen dioksida.”Wikipedia, Wikimedia Foundation, 10 Juli 2018. Tersedia disini
Gambar milik:
1.'Nitriteion-resonance-hybrid'by yikrazuul-pekerjaan sendiri, (domain publik) melalui commons wikimedia
2.'Nitrogen-Dioxide-2D-Dimensions'By Ben Mills-Pekerjaan Sendiri, (Domain Publik) Melalui Commons Wikimedia


