Perbedaan antara oksida dan dioksida
Itu perbedaan utama antara oksida dan dioksida adalah itu Oksida adalah senyawa apa pun yang memiliki satu atau lebih atom oksigen yang dikombinasikan dengan elemen kimia lain, sedangkan dioksida adalah oksida yang mengandung dua atom oksigen dalam molekulnya.
Istilah oksida adalah istilah umum yang menggambarkan keberadaan atom oksigen dalam suatu senyawa. Di sini, atom oksigen ada dalam kombinasi dengan elemen kimia lain; kebanyakan logam dan bukan logam. Menurut jumlah atom oksigen dalam senyawa, kita dapat menamainya sebagai monoksida, dioksida, trioksida, dll. Oleh karena itu, dioksida adalah oksida yang mengandung dua atom oksigen per molekul.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu oksida
3. Apa itu dioksida
4. Perbandingan berdampingan -oksida vs dioksida dalam bentuk tabel
5. Ringkasan
Apa itu oksida?
Oksida adalah senyawa apa pun yang memiliki satu atau lebih atom oksigen dikombinasikan dengan elemen kimia lain. "Oksida" di sini adalah anion divalen (o2-). Biasanya, oksida logam mengandung dianion ini di mana atom oksigen dalam keadaan oksidasi -2. Kecuali untuk gas inert ringan (termasuk helium, neon, argon dan krypton), oksigen dapat membentuk oksida dengan semua elemen lainnya.
Dalam pembentukan oksida, logam dan bukan logam dapat menunjukkan keadaan oksidasi terendah dan tertinggi. Beberapa oksida adalah senyawa ionik; Logam alkali, logam tanah alkali dan logam transisi membentuk oksida ionik ini. Senyawa lain memiliki sifat kovalen; Logam dengan keadaan oksidasi tinggi dapat membentuk oksida kovalen. Selain itu, bukan logam membentuk senyawa oksida kovalen.
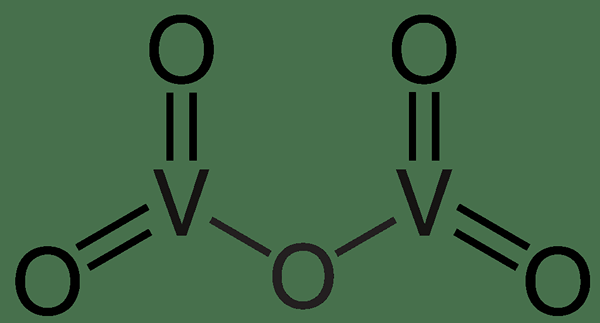
Gambar 01: Vanadium (V) oksida
Pada gambar di atas, atom logam vanadium memiliki valensi 5 (total valensi adalah 10 untuk dua atom vanadium) dengan demikian, lima atom oksigen (dengan valensi 2 per setiap atom oksigen) yang terikat pada mereka.
Selain itu, beberapa senyawa organik juga bereaksi dengan oksigen (atau agen pengoksidasi) untuk menghasilkan oksida, e.G. amina oksida, fosfin oksida, sulfoksida, dll. Lebih lanjut, jumlah atom oksigen dalam senyawa menentukan apakah itu monoksida, dioksida atau trioksida.
Menurut sifatnya, dimungkinkan juga untuk mengkategorikannya sebagai oksida asam, basa, netral dan amfoterik. Oksida asam dapat bereaksi dengan basa dan membentuk garam. Contoh: Sulfur trioksida (SO3). Oksida dasar bereaksi dengan asam dan membentuk garam. Contoh: Sodium oksida (NA2O). Netral tidak menunjukkan sifat asam atau basa; Dengan demikian mereka tidak membentuk garam setelah bereaksi dengan asam atau basa. Mis: Carbon monoxide (CO). Oksida amfoterik memiliki sifat asam dan basa; Oleh karena itu, mereka bereaksi dengan asam dan basa untuk membentuk garam. Mis: seng oksida (ZnO).
Apa itu dioksida?
Dioksida adalah oksida yang mengandung dua atom oksigen dalam molekulnya. Molekul harus mengandung elemen kimia dengan valensi 4 untuk membentuk dioksida. Itu karena satu atom oksigen menunjukkan valensi 2. Misalnya, dalam karbon dioksida, valensi karbon adalah 4.

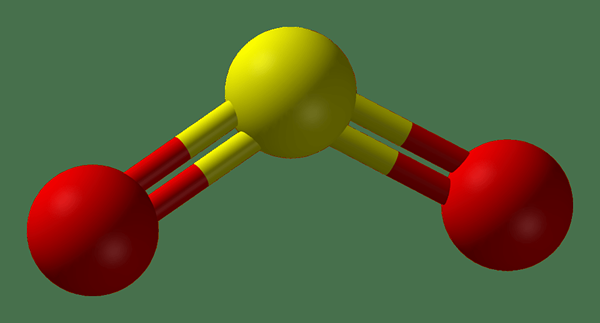
Gambar 02: Struktur bola dan tongkat sulfur dioksida
Beberapa contoh dioksida
- Karbon dioksida (CO2)
- Nitrogen dioksida (tidak2)
- Oksigen (o2)
- Kuarsa atau silikon dioksida (sio2)
Apa perbedaan antara oksida dan dioksida?
Dioksida adalah jenis oksida. Perbedaan utama antara oksida dan dioksida adalah bahwa oksida adalah senyawa apa pun yang memiliki satu atau lebih atom oksigen yang dikombinasikan dengan elemen kimia lain, sedangkan dioksida adalah oksida yang mengandung dua atom oksigen dalam molekulnya. Saat mempertimbangkan valensi oksida, valensi oksigen adalah 2, dan valensi elemen lain dapat bervariasi; Namun, untuk dioksida, valensi oksigen adalah 2 dan valensi elemen lain pada dasarnya 4 adalah 4. Jadi, kita bisa mempertimbangkan ini juga sebagai perbedaan antara oksida dan dioksida.

Ringkasan -oksida vs dioksida
Oksida adalah istilah umum yang kami gunakan untuk menyebutkan senyawa apa pun yang mengandung atom oksigen dalam kombinasi dengan elemen lain. Selain itu, sesuai dengan jumlah atom oksigen, kita dapat menyebutkannya sebagai monoksida, dioksida, trioksida, dll. Perbedaan utama antara oksida dan dioksida adalah bahwa oksida adalah senyawa apa pun yang memiliki satu atau lebih atom oksigen yang dikombinasikan dengan elemen kimia lain, sedangkan dioksida adalah oksida yang mengandung dua atom oksigen dalam molekulnya.
Referensi:
1.“Oksida." Wikipedia, Wikimedia Foundation, 2 Juni 2019, tersedia di sini.
Gambar milik:
1. “Vanadium (V) Oxide” oleh Kemikungen - karya sendiri (domain publik) melalui Commons Wikimedia
2. “Sulphur-Dioxide-3D-Balls” oleh Ben Mills-karya sendiri (domain publik) melalui Commons Wikimedia


