Perbedaan antara fenil dan benzil

Fenil vs Benzyl
Baik fenil dan benzil berasal dari benzena, dan umumnya bingung oleh siswa kimia. Fenil adalah molekul hidrokarbon dengan formula C6H5, sedangkan benzil adalah c6H5Ch2; CH ekstra2 Grup melekat pada cincin benzena.
Fenil
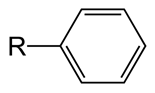
Fenil adalah molekul hidrokarbon dengan formula C6H5. Ini berasal dari benzena, oleh karena itu, memiliki sifat yang sama dengan benzena. Namun, ini berbeda dari benzena karena kurangnya atom hidrogen dalam satu karbon. Jadi berat molekul fenil adalah 77 g mol-1. Fenil disingkat pH. Biasanya fenil melekat pada gugus fenil, atom, atau molekul lain (bagian ini dikenal sebagai substituen, kelompok R seperti pada gambar). Atom karbon fenil adalah sp2 hibridisasi seperti di benzena. Semua karbon dapat membentuk tiga ikatan sigma. Dua ikatan sigma dibentuk dengan dua karbon yang berdekatan, sehingga akan menimbulkan struktur cincin. Ikatan sigma lainnya dibentuk dengan atom hidrogen. Namun, dalam satu karbon, di atas ring, ikatan sigma ketiga dibentuk dengan atom atau molekul lain daripada atom hidrogen. Elektron dalam orbital p tumpang tindih satu sama lain untuk membentuk awan elektron yang didelokalisasi. Oleh karena itu, fenil memiliki panjang ikatan C-C yang serupa antara semua karbon, terlepas dari memiliki ikatan tunggal dan rangkap bergantian. Panjang ikatan C-C ini sekitar 1.4 Å. Cincin ini planar dan memiliki sudut 120 ° antara ikatan di sekitar karbon. Karena kelompok substituen fenil, polaritas dan sifat kimia atau fisik lainnya berubah. Jika substituen menyumbangkan elektron ke awan elektron yang terdelokalisasi, yang dikenal sebagai kelompok donasi elektron (e.G. -Och3, NH2). Jika substituen menarik elektron dari awan elektron, ia dikenal sebagai substituen penarikan elektron. (E.G. -TIDAK2, -Cooh). Kelompok fenil stabil karena aromatiknya, sehingga mereka tidak mudah menjalani oksidasi atau pengurangan. Selanjutnya, mereka hidrofobik dan non-polar.
Benzil
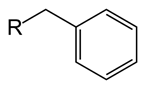
Formula benzil adalah c6H5Ch2. Ini juga merupakan turunan dari benzena. Dibandingkan dengan fenil, benzil memiliki ch2 Grup melekat pada cincin benzena. Bagian molekuler lain (kelompok R seperti yang digambarkan dalam gambar) dapat dilampirkan pada gugus benzil melalui ikatan ke CH2 atom karbon. Kelompok benzil disingkat sebagai "bn". Berat molekul gugus benzil adalah 91 g mol-1. Karena ada cincin benzena, kelompok benzil aromatik. Dalam mekanisme kimia organik, kelompok benzil dapat dibentuk baik sebagai radikal, karbokation (c6H5Ch2+) atau karboanion (c6H5Ch2-). Misalnya, dalam reaksi substitusi nukleofilik, radikal benzlik atau intermediate kation terbentuk. Ada stabilisasi yang lebih tinggi dari perantara ini dibandingkan dengan radikal atau kation alkil. Reaktivitas posisi benzili mirip dengan posisi alilia. Kelompok benzil sering digunakan dalam kimia organik sebagai gugus pelindung, terutama untuk melindungi asam karboksilat atau kelompok fungsional alkohol.
Apa perbedaan antara fenil dan benzil?
• Formula molekul fenil adalah C6H5 sedangkan, di benzil, itu c6H5Ch2.
• Benzyl memiliki CH ekstra2 kelompok dibandingkan dengan fenil.
• Dalam fenil, cincin benzena secara langsung melekat pada molekul substituen atau atom, tetapi dalam benzil, ch2 kelompok membuat koneksi dengan molekul lain atau atom.


