Perbedaan antara amonium kuaterner dan amonia
Itu perbedaan utama Antara amonium dan amonia kuaterner adalah itu Molekul amonia kuaterner memiliki atom nitrogen sentral yang terikat pada empat kelompok alkil sedangkan molekul amonia mengandung satu pusat nitrogen yang terikat pada tiga atom hidrogen.
Amonium kuaterner adalah kation yang berasal dari molekul amonia normal. Di sini, tiga atom hidrogen dari molekul amonia diganti dengan gugus alkil yang sama atau berbeda, dan ada gugus alkil ekstra yang terikat dengan atom nitrogen melalui pasangan elektron tunggalnya.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu amonium kuaterner
3. Apa itu amonia
4. Perbandingan berdampingan - amonium kuaterner vs amonia dalam bentuk tabel
5. Ringkasan
Apa itu amonium kuaterner?
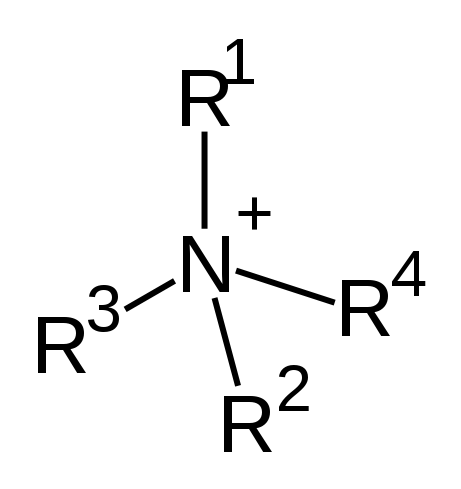
Amonium Kuarter adalah kation yang berasal dari molekul amonia, dan memiliki atom nitrogen sentral dengan empat gugus alkil yang diganti padanya. Oleh karena itu, formula kimia molekul ini dapat ditulis sebagai [N-R1R2R3R4]+. Struktur kimia kation ini adalah sebagai berikut:

Gambar 01: Struktur kimia kation amonium kuaterner
Kation ini disingkat sebagai quat. Mereka adalah ion polyatomic yang bermuatan positif. Ada beberapa ion yang dibentuk oleh molekul amonia termasuk amonia primer, sekunder dan tersier. Ini dinamai sesuai dengan jumlah kelompok alkil yang terikat pada atom nitrogen.
Senyawa amonium kuaterner yang paling umum adalah garam amonium kuaterner. Senyawa ini dapat disiapkan dengan alkilasi amina tersier di hadapan halokarbon. Secara umum, kation amonium kuaterner tidak reaktif terhadap oksidan yang kuat, asam kuat, dan elektrofil. Namun, kation ini mengalami degradasi di hadapan basis yang sangat kuat.
Apa itu amonia?
Amonia adalah senyawa anorganik yang memiliki formula kimia NH3. Ini adalah zat gas, dan itu adalah pnictogen hydride paling sederhana. Amonia terjadi sebagai gas tidak berwarna yang memiliki bau yang pedas dan menjengkelkan. Nama Amonia IUPAC adalah Azane.
Formula kimianya adalah NH3. Oleh karena itu, massa molar adalah 17.03 g/mol. Titik pencairan amonia adalah −77.73 ° C, dan titik didih adalah −33.34 ° C.
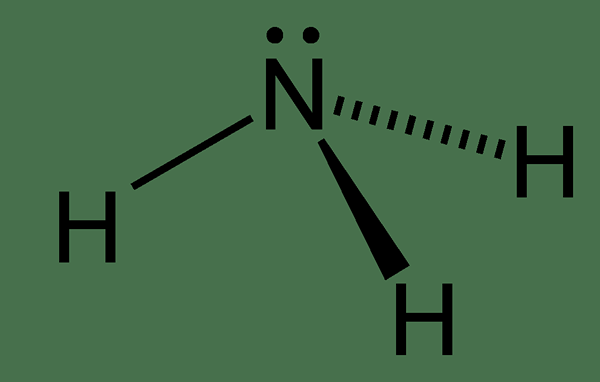
Gambar 02: Struktur molekul amonia
Saat mempertimbangkan terjadinya gas amonia, secara alami terjadi di lingkungan tetapi dalam jumlah jejak sebagai produk dari bahan hewan dan nabati nitrogen. Terkadang, kita juga dapat menemukan amonia di air hujan. Di dalam tubuh kita, ginjal mengeluarkan amonia untuk menetralkan asam berlebih.
Dalam struktur kimia molekul amonia, ia memiliki atom nitrogen yang terikat pada tiga atom hidrogen. Karena ada lima elektron dalam cangkang elektron terluar dari nitrogen, ada pasangan elektron tunggal pada atom nitrogen molekul amonia. Oleh karena itu, geometri molekul amonia adalah piramidal trigonal. Selain itu, kita dapat mencairkan senyawa ini dengan mudah. Ini karena mampu membentuk ikatan hidrogen antara molekul amonia karena ada ikatan N-H dan pasangan elektron sendirian juga.
Apa perbedaan antara amonium kuaterner dan amonia?
Amonium kuaterner adalah kation yang berasal dari molekul amonia. Perbedaan utama antara amonium kuaterner dan amonia adalah bahwa molekul amonia kuaterner memiliki atom nitrogen sentral yang terikat dengan empat kelompok alkil sedangkan molekul amonia mengandung satu pusat nitrogen yang terikat pada tiga atom hidrogen.
Tabel berikut merangkum perbedaan antara amonium kuaterner dan amonia.

Ringkasan -Amonium Kuarter vs amonia
Amonium kuaterner adalah kation yang berasal dari molekul amonia. Perbedaan utama antara amonium kuaterner dan amonia adalah bahwa molekul amonia kuaterner memiliki atom nitrogen sentral yang terikat dengan empat kelompok alkil sedangkan molekul amonia mengandung satu pusat nitrogen yang terikat pada tiga atom hidrogen.
Referensi:
1. “Senyawa amonium kuaterner." Senyawa amonium kuaterner - tinjauan umum | Topik ScienceDirect, Tersedia disini.
Gambar milik:
1. "Ammonia-2D" oleh Radio89-karya sendiri (CC BY-SA 3.0) Via Commons Wikimedia
2. “Kation Ammonium Kuarter” oleh fvasconcellos - karya sendiri (domain publik) melalui commons wikimedia


