Perbedaan antara natrium fosfat monobasik dan dibasic

Sodium phosphate monobasic vs dibasic | Sodium fosfat Dibasic vs Sodium phosphate monobasic | Monosodium fosfat vs disodium fosfat | Monosodium vs Disodium fosfat
Satu atom fosfor terikat dengan empat oksigen, untuk membentuk anion polyatomik -3. Karena ikatan tunggal dan ikatan rangkap, antara P dan O, fosfor memiliki keadaan oksidasi +5 di sini. Itu memiliki geometri tetrahedral. Berikut ini adalah struktur anion fosfat.
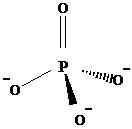
PO43-
Anion fosfat dapat digabungkan dengan kation yang berbeda, untuk membentuk banyak senyawa ionik. Natrium fosfat adalah garam seperti itu di mana tiga ion natrium terikat secara elektrostatistik dengan satu anion fosfat. Trisodium fosfat adalah kristal berwarna putih, yang sangat larut dalam air. Saat larut dalam air, ia menghasilkan larutan alkali. Natrium fosfat monobasik dan natrium fosfat dibasic adalah dua senyawa natrium dan fosfat lainnya. Untuk asam, kami mendefinisikan istilah monobasic sebagai “asam, yang hanya memiliki satu proton yang dapat disumbangkan ke basa selama reaksi asam basa."Demikian juga, dibasic untuk asam berarti memiliki dua proton, yang dapat disumbangkan ke basa. Tetapi ketika mempertimbangkan kedua istilah ini tentang garam, artinya sangat berbeda. Garam monobasik mengacu pada garam, yang hanya memiliki satu atom logam yang tidak tervital. Dan garam dibasic berarti memiliki dua ion logam yang tidak tervivalen. Dalam hal ini, ion logam yang univalen adalah kation natrium. Karena ini adalah garam, mereka mudah larut dalam air dan menghasilkan larutan alkali. Senyawa ini tersedia secara komersial dalam bentuk hidro dan anhidrat. Sodium fosfat monobasik dan dibasic bersama -sama sangat penting dalam sistem biologis sebagai buffer. Selanjutnya, secara medis keduanya digunakan sebagai pencahar salin, untuk mengobati sembelit.
Sodium fosfat monobasic
Natrium fosfat monobasik atau monosodium fosfat memiliki formula molekul NAH2PO4. Massa molar senyawa adalah 120 g mol-1. Anion dalam molekul ini bukan anion fosfat trivalen, tetapi h2PO4- anion. Anion ini berasal dari ion fosfat di mana dua hidrogen terikat dengan dua oksigen negatif. Atau, di sisi lain ia berasal dari penghapusan satu proton dari asam fosfat (h3PO4). Anion fosfat dan h2PO4- Anion berada dalam keseimbangan, di media berair. Natrium fosfat monobasic tersedia sebagai kristal tidak berwarna atau bubuk putih. Itu mudah larut dalam air, tetapi jangan larut dalam pelarut organik seperti alkohol. PKA dari ini adalah antara 6.8-7.20. Senyawa ini dapat dibuat saat asam fosfat bereaksi dengan garam natrium seperti natrium halida.
Dibasic Sodium Fosfat
Senyawa ini juga dikenal sebagai disodium fosfat dan memiliki formula molekul Na2HPO4. Massa molar senyawa adalah 142 g mol-1. Ketika dua kation natrium menggantikan atom hidrogen dalam asam fosfat, natrium fosfat dibasic diperoleh. Jadi di laboratorium kita dapat membuat senyawa ini dengan bereaksi dua ekuivalen natrium hidroksida dengan satu setara dengan asam fosfat. Senyawa ini adalah padatan kristal putih, dan mudah larut dalam air. PH larutan berair ini adalah nilai dasar, yaitu antara 8 dan 11. Garam ini digunakan untuk keperluan memasak, dan sebagai pencahar.
| Apa perbedaan antara Natrium fosfat monobasik dan natrium fosfat dibasic? • natrium fosfat monobasic memiliki formula kimia nah2PO4, dan natrium fosfat dibasic memiliki formula kimia Na2HPO4. • Berat molekul natrium fosfat dibasic lebih tinggi dari natrium fosfat monobasik. • Saat natrium fosfat dibasic larut dalam air, kebusukan lebih tinggi pada medium daripada saat natrium fosfat monobasik larut dalam air. |


