Perbedaan antara spesies dan fase dalam larutan
Itu perbedaan utama Antara spesies dan fase dalam larutan adalah itu Spesies larutan mengacu pada komponen kimia yang ada dalam larutan sedangkan fase dalam larutan mengacu pada bentuk zat yang tampak berbeda yang ada dalam larutan.
Solusi adalah campuran pelarut dan zat terlarut. Zat terlarut dibubarkan dalam pelarut. Beberapa zat terlarut larut dalam pelarut seperti mereka sementara yang lain larut melalui ionisasi. Oleh karena itu, spesies yang ada dalam larutan tergantung pada kemampuan ionisasi senyawa dalam pelarut. Ada dua jenis solusi sebagai solusi homogen dan solusi heterogen, tergantung pada fase masalahnya.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa spesies dalam larutan
3. Apa fase dalam solusi
4. Perbandingan berdampingan -Spesies vs fase dalam larutan dalam bentuk tabel
5. Ringkasan
Apa spesies dalam larutan?
Spesies dalam larutan mengacu pada komponen kimia yang terbentuk dari pembubaran zat terlarut dalam pelarut saat membentuk larutan. Beberapa spesies larut dalam pelarut seperti mereka. Sebagai contoh, disolusi glukosa membentuk larutan glukosa berair, yang mengandung molekul glukosa yang belum mengalami perubahan apa pun. Di sini, spesies kimia dalam larutan adalah molekul glukosa.
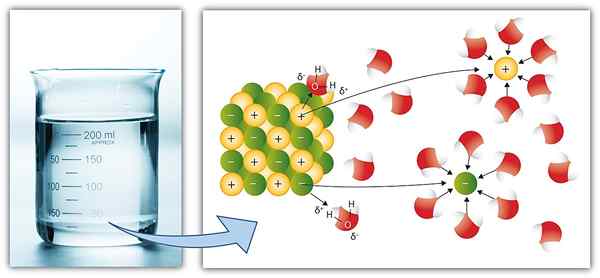
Terkadang, senyawa ionik larut dalam pelarut melalui ionisasi. Itu berarti; Senyawa ini terdisosiasi menjadi komponen ioniknya setelah pembubaran dalam pelarut. Dalam hal ini, spesies kimia yang ada dalam larutan adalah komponen ionik, bukan molekul yang dilarutkan. Oleh karena itu, spesies dalam larutan dapat bervariasi tergantung pada kemampuan ionisasi zat terlarut.

Gambar 01: Spesies ionik dalam air
Saat menjelaskan sifat -sifat larutan, penting untuk mengetahui spesies kimia yang ada dalam larutan. Misalnya, ketika kami mengekspresikan konsentrasi larutan, kami biasanya merujuk pada konsentrasi zat terlarut atau ion yang terlarut. Selain itu, titik didih dari larutan, kelarutan komponen lain dalam larutan, dan banyak sifat larutan lainnya tergantung pada spesies yang ada dalam larutan.
Apa fase dalam solusi?
Fase dalam larutan mengacu pada ada atau tidak adanya satu atau lebih fase materi dalam larutan yang sama. Di sini, kami dapat mengkategorikan solusi menjadi dua jenis sebagai solusi homogen dan solusi heterogen.

Gambar 02: Susu adalah solusi yang heterogen
Solusi homogen juga disebut solusi fase tunggal karena memiliki semua materi dalam fase yang sama. Itu berarti, zat terlarut dan pelarut berada dalam fase yang sama, dan kami tidak dapat mengamati fase yang berbeda dalam solusi ini. Sebaliknya, solusi yang heterogen adalah solusi bertahap multipel. Itu adalah; Solusi ini memiliki dua atau lebih fase dalam solusi yang sama. Misalnya, emulsi memiliki fase cair dan padat dalam larutan yang sama.
Apa perbedaan antara spesies dan fase dalam larutan?
Perbedaan utama antara spesies dan fase dalam larutan adalah bahwa spesies larutan mengacu pada komponen kimia yang ada dalam larutan, sedangkan fase dalam larutan mengacu pada bentuk zat yang terlihat berbeda dalam larutan. Selain itu, molekul atau ion adalah komponen dari suatu spesies dalam suatu larutan, sedangkan fase cair dan padat adalah komponen dari suatu spesies dalam suatu larutan.
Infografis berikut merangkum perbedaan antara spesies dan fase dalam larutan.

Ringkasan -Spesies vs Fase dalam Solusi
Solusi adalah campuran pelarut dan zat terlarut. Zat terlarut dibubarkan dalam pelarut. Spesies dalam larutan dan fase dalam larutan adalah istilah penting saat mengekspresikan sifat -sifat larutan. Perbedaan utama antara spesies dan fase dalam larutan adalah bahwa spesies larutan mengacu pada komponen kimia yang ada dalam larutan, sedangkan fase dalam larutan mengacu pada bentuk zat yang terlihat berbeda dalam larutan.
Referensi:
1. Helmenstine, Anne Marie. “Perbedaan antara campuran heterogen dan homogen."Thoughtco, Jan. 29, 2020, tersedia di sini.
2. “Aktivitas termodinamika."Wikipedia, Wikimedia Foundation, 4 Okt. 2019, tersedia di sini.
Gambar milik:
1. “Sodium Chloride Disolution” oleh Andy Schmitz - 2012 Book Archive (CC oleh 3.0) Via Commons Wikimedia
2. "Susu Kecil Lucu" oleh Hobvias Sudoneighm (CC dengan 2.0) Via Flickr


