Perbedaan antara isotop stabil dan radioisotop
Perbedaan utama - isotop stabil vs radioisotop
Isotop adalah bentuk yang berbeda dari elemen kimia yang sama yang memiliki massa atom yang berbeda. Ini berarti isotop dari elemen kimia tertentu memiliki jumlah atom yang sama tetapi massa atom yang berbeda. Ini karena isotop ini memiliki jumlah neutron yang berbeda dalam inti atomnya. Beberapa isotop stabil sedangkan beberapa tidak stabil. Isotop yang stabil adalah bentuk elemen kimia yang terjadi secara alami. Isotop stabil ini dapat terjadi secara alami dalam bentuk atom atau dalam kombinasi dengan atom lainnya. Isotop yang tidak stabil menjalani peluruhan radioaktif sampai mereka mendapatkan keadaan yang stabil. Isotop ini dikenal sebagai radioisotop. Perbedaan utama antara isotop stabil dan radioisotop adalah bahwa isotop stabil tidak mengalami peluruhan radioaktif sedangkan radioisotop mengalami peluruhan radioaktif.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa isotop stabil
3. Apa itu radioisotop
4. Perbandingan berdampingan - isotop stabil vs radioisotop dalam bentuk tabel
5. Ringkasan
Apa isotop stabil?
Isotop stabil adalah bentuk yang berbeda dari elemen kimia yang sama, memiliki inti yang stabil. Atom -atom ini memiliki jumlah atom yang sama (jumlah proton dalam inti atom) karena mereka termasuk dalam elemen kimia yang sama, tetapi massa atom berbeda satu sama lain karena mereka memiliki jumlah neutron yang berbeda dalam inti atomik.
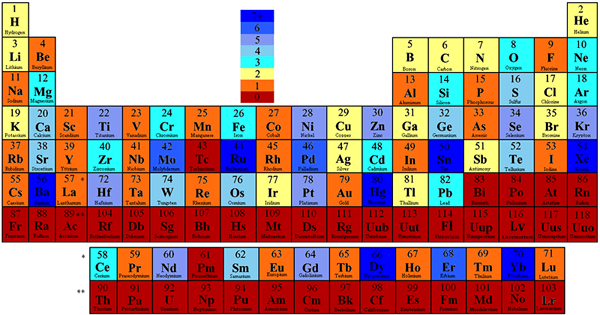
Isotop stabil adalah non-radioaktif karena stabilitas inti atom. Oleh karena itu, atom -atom ini tidak memancarkan radiasi. Elemen kimia tertentu dapat memiliki lebih dari satu isotop stabil. Tetapi dalam beberapa elemen kimia, semua isotop tidak stabil; Oleh karena itu, mereka radioaktif.

Gambar 1: Tabel periodik diwarnai berdasarkan jumlah isotop stabil
Stabilitas inti atom tergantung pada dua faktor dasar:
- Rasio antara proton dan neutron
- Jumlah proton dan neutron
"Angka ajaib" adalah konsep kimia yang digunakan untuk menentukan stabilitas inti atom tertentu. Ini memberikan jumlah elektron yang ada dalam isotop stabil. Nomor ajaib dapat berupa jumlah proton atau bahkan jumlah neutron yang ada dalam nukleus.
Nomor ajaib: 2, 8, 20, 28, 50, 82 dan 126
Jika jumlah atom isotop sama dengan salah satu dari angka di atas, maka itu adalah isotop yang stabil. Selain itu, jika isotop memiliki 114 proton, itu adalah isotop yang stabil. Selain itu, jika ada 126 atau 184 neutron yang ada, mereka juga isotop stabil. Selain itu, jika rasio antara proton dan neutron dalam atom bahkan angka, maka isotop ini kemungkinan besar adalah isotop yang stabil.
Apa itu radioisotop?
Radioisotop adalah isotop unsur kimia yang tidak stabil yang mengalami peluruhan radioaktif. Isotop ini mengalami peluruhan radioaktif karena mereka memiliki inti atom yang tidak stabil. Sebagian besar elemen kimia memiliki satu atau lebih isotop radioaktif sedangkan beberapa elemen kimia hanya memiliki isotop radioaktif (mis: uranium).
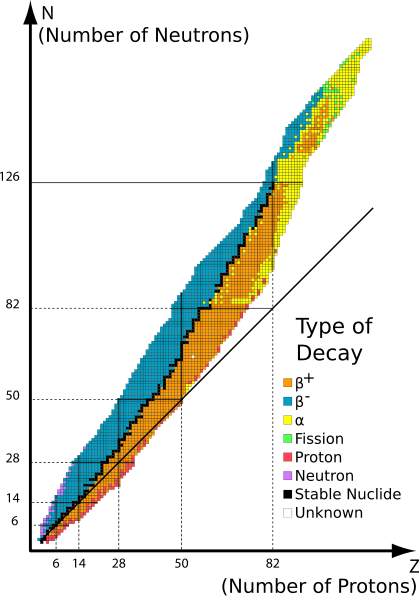
Gambar 2: Radioisotop yang berbeda dan peluruhan radioaktifnya
Isotop radioaktif tidak stabil karena beberapa alasan:
- Kehadiran sejumlah besar neutron dalam inti atom dibandingkan dengan jumlah proton
- Dalam radioisotop ini, neutron dikonversi menjadi proton dan elektron selama peluruhan radioaktif.
- Adanya sejumlah besar proton dalam nukleus atom
- Dalam radioisotop ini, proton dikonversi menjadi neutron dan positron.
- Adanya sejumlah besar proton dan elektron
- Radioisotop ini mengalami peluruhan alpha di mana dua proton dan dua neutron dipancarkan sebagai partikel alfa
Apa perbedaan antara isotop stabil dan radioisotop?
Isotop stabil vs radioisotop | |
| Isotop stabil adalah bentuk yang berbeda dari elemen kimia yang sama, memiliki inti yang stabil. | Radioisotop adalah isotop unsur kimia yang tidak stabil yang mengalami peluruhan radioaktif. |
| Stabilitas | |
| Isotop stabil sangat stabil dan tidak mengalami peluruhan radioaktif. | Radioisotop sangat tidak stabil dan mengalami peluruhan radioaktif untuk mendapatkan keadaan yang stabil. |
| Proton | |
| Kehadiran 114 proton membuat isotop isotop yang stabil. | Kehadiran sejumlah besar proton membuat isotop menjadi radioisotop. |
| Neutron | |
| Kehadiran 126 atau 184 neutron membuat isotop isotop stabil. | Jumlah neutron dalam jari -jari atom lebih tinggi dari jumlah proton. |
Ringkasan -isotop stabil vs radioisotop
Isotop adalah atom dari elemen kimia yang sama yang memiliki bilangan atom yang identik tetapi massa atom yang berbeda. Beberapa isotop stabil sedangkan yang lain tidak stabil. Isotop yang stabil adalah bentuk yang terjadi secara alami dari unsur -unsur kimia tersebut. Isotop yang tidak stabil juga disebut radioisotop karena isotop ini mengalami peluruhan radioaktif untuk mendapatkan keadaan yang stabil. Perbedaan utama antara isotop stabil dan radioisotop didasarkan pada kemampuan mereka untuk mengalami peluruhan radioaktif.
Referensi:
1. “Rasio isotop yang stabil.”Wikipedia, Wikimedia Foundation, 27 Feb. 2018, tersedia di sini.
2. “Apa itu radioisotop?”Foro Nuclear, Tersedia Di Sini.
3. Britannica, editor Encyclopaedia. “Nomor ajaib.”Encyclopædia Britannica, Encyclopædia Britannica, Inc., 12 Juli 2017, tersedia di sini.
Gambar milik:
1. “Tabel Berkala dengan Sejumlah Isotop Stabil” oleh Nergaal di Wikipedia Inggris (CC BY-SA 3.0) Via Commons Wikimedia
2. "Table Isotopes EN" oleh Table_isotopes.SVG: Napy1kenobiderivative Work: Sjlegg (Talk) - Table_isotopes.SVG (CC BY-SA 3.0) Via Commons Wikimedia


