Perbedaan antara solusi padat substitusi dan interstitial

Itu perbedaan utama Antara solusi substitusional dan padat interstitial adalah bahwa Larutan padat substitusi melibatkan substitusi atom pelarut dengan atom zat terlarut, dalam pembentukannya. Sebaliknya, tidak ada perpindahan atom pelarut dengan atom zat terlarut dalam pembentukan solusi padat interstitial, sebaliknya, molekul zat terlarut memasuki lubang antara atom pelarut.
Solusi padat adalah solusi solid state dari satu atau lebih zat terlarut dalam pelarut yang sama. Di sana, dua atau lebih elemen terjadi di solid state. Kami menyebutnya solusi daripada senyawa karena struktur kristal pelarut tetap tidak berubah dengan penambahan zat terlarut. Dalam proses penguatan larutan padat, kekuatan logam murni dapat ditingkatkan melalui paduan elemen lain. Kita bisa melakukan ini dengan membentuk solusi yang solid. Bergantung pada elemen paduan, ada dua bentuk solusi padat sebagai solusi solid substitusi dan interstitial.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu solusi padat substitusi
3. Apa itu solusi padat interstitial
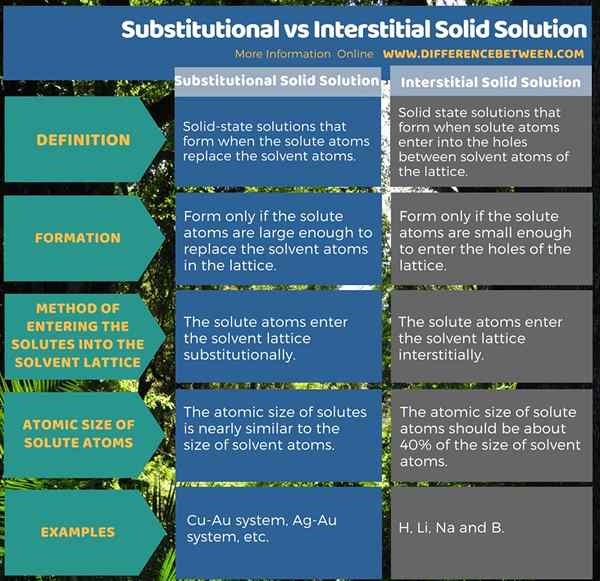
4. Perbandingan Berdampingan - Solusi Substitusi Vs Interstitial Interstitial dalam bentuk tabel
5. Ringkasan
Apa itu solusi padat substitusi?
Larutan padat substitusi adalah solusi solid-state yang terbentuk ketika atom zat terlarut menggantikan atom pelarut. Untuk membentuk solusi padat semacam ini, atom zat terlarut harus cukup besar untuk menggantikan atom pelarut di kisi. Atom zat terlarut dimasukkan ke dalam kisi secara substitusi melalui mengganti atom dalam posisi tertentu dari kisi. Di sini, beberapa elemen paduan memiliki atom terlarut yang dapat menggantikan atom pelarut hanya dalam jumlah kecil sementara ada beberapa elemen paduan yang dapat menggantikan atom pelarut di seluruh solusi padat.
Jenis solusi padat ini terbentuk saat atom zat terlarut dan pelarut memiliki ukuran atom yang hampir sama. Selain itu, suhu tinggi dapat meningkatkan penggantian ini. Selain itu, ada dua bentuk solusi padat substitusi yaitu; solusi solid yang dipesan dan tidak teratur. Bentuk solusi padat yang dipesan saat atom zat terlarut menggantikan atom pelarut di situs yang disukai dari kisi pelarut. Mis: Sistem Cu-au. Solusi padat yang tidak teratur terbentuk ketika atom zat terlarut secara acak mengganti atom pelarut di kisi.
Apa itu solusi padat interstitial?
Solusi padat interstitial adalah solusi keadaan padat yang terbentuk ketika atom zat terlarut masuk ke dalam lubang antara atom pelarut kisi. Di sana, atom zat terlarut cukup kecil untuk masuk ke dalam lubang ini. Kami menyebut lubang ini, situs interstitial.

Gambar 01: Solusi padat interstitial
Proses ini melemahkan ikatan antara atom pelarut. Dengan demikian, kisi cacat. Agar ini terjadi ukuran atom atom zat terlarut harus kurang dari 40% dari ukuran atom pelarut. Atom zat terlarut masuk ke kisi interstitual. Satu -satunya elemen yang mampu membentuk jenis solusi padat ini adalah H, Li, Na dan B.
Apa perbedaan antara larutan padat substitusi dan interstitial?
Larutan padat substitusi adalah solusi solid-state yang terbentuk ketika atom zat terlarut menggantikan atom pelarut. Jenis solusi padat ini hanya terbentuk jika atom zat terlarut cukup besar untuk menggantikan atom pelarut di kisi. Selain itu, ukuran atom zat terlarut hampir mirip dengan ukuran atom pelarut. Solusi padat interstitial adalah solusi solid state yang terbentuk ketika atom zat terlarut masuk ke dalam lubang antara atom pelarut kisi. Solusi solid ini hanya terbentuk jika atom zat terlarut cukup kecil untuk memasuki lubang kisi. Selain itu, ukuran atom atom zat terlarut harus sekitar 40% dari ukuran atom pelarut untuk membentuk jenis kisi ini. Ini adalah perbedaan utama antara larutan padat substitusi dan interstitial.
Ringkasan -Solusi Substitusi Vs Interstitial Solid
Solusi solid adalah solusi solid state yang memiliki dua atau lebih jenis elemen dalam campuran keadaan padat yang sama. Ada dua bentuk solusi padat sebagai solusi solid substitusi dan interstitial sesuai dengan cara bentuknya. Perbedaan antara larutan padat substitusi dan interstitial adalah bahwa dalam pembentukan larutan padat substitusi, ini melibatkan substitusi atom pelarut dengan atom zat terlarut sedangkan dalam pembentukan larutan padat interstitial, tidak ada perpindahan atom pelarut dengan atom terlarut dengan pelarut atom pelarut soluteal, , sebaliknya, molekul zat terlarut memasuki lubang antara atom pelarut.
Referensi:
1. “Penguatan Solusi Solid.”Wikipedia, Wikimedia Foundation, 19 Juni 2018. Tersedia disini
2. Pabrik Senjata Kecil (Kementerian Pertahanan) Ikuti. “Solusi yang solid."LinkedIn Slideshare, 18 Nov. 2013. Tersedia disini
Gambar milik:
1.'Interstitial Solute'by Isiamrut di English Wikipedia (CC BY-SA 3.0) Via Commons Wikimedia


